Clear Sky Science · zh
帕博利珠单抗联合阿扎胞苷的表观遗传修饰重塑铂耐药上皮性卵巢癌的肿瘤微环境:一项二期非随机临床试验
这项研究重要的原因
对于许多晚期卵巢癌患者,标准化疗最终失效,剩下的有效选项很少。这项研究探讨了一种新策略:将免疫治疗与一种可以“重编程”癌细胞的药物配对,希望将那些沉默、难以被识别的肿瘤转变为免疫系统可以发现并攻击的目标。评估这一方法的安全性、对肿瘤生长的控制效果以及对肿瘤内部的具体影响,可能会影响对这种致死性妇科癌症的未来治疗方向。
一种难治的卵巢癌类型
卵巢癌常在晚期确诊,且许多肿瘤对一种关键化疗药物——铂类——产生耐药。一旦出现耐药,对后续化疗的反应通常短暂。免疫检查点抑制剂通过解除免疫细胞的“刹车”已在若干癌种改变治疗格局,但在卵巢癌中的疗效有限。部分原因是许多卵巢肿瘤是“冷”的:它们含有相对较少的活跃免疫细胞,使得检查点抑制剂难以发挥作用。该试验的研究者提出,是否可以先改变癌细胞内基因的开关状态,从而“变暖”这些肿瘤。
将免疫治疗与表观遗传药物配对
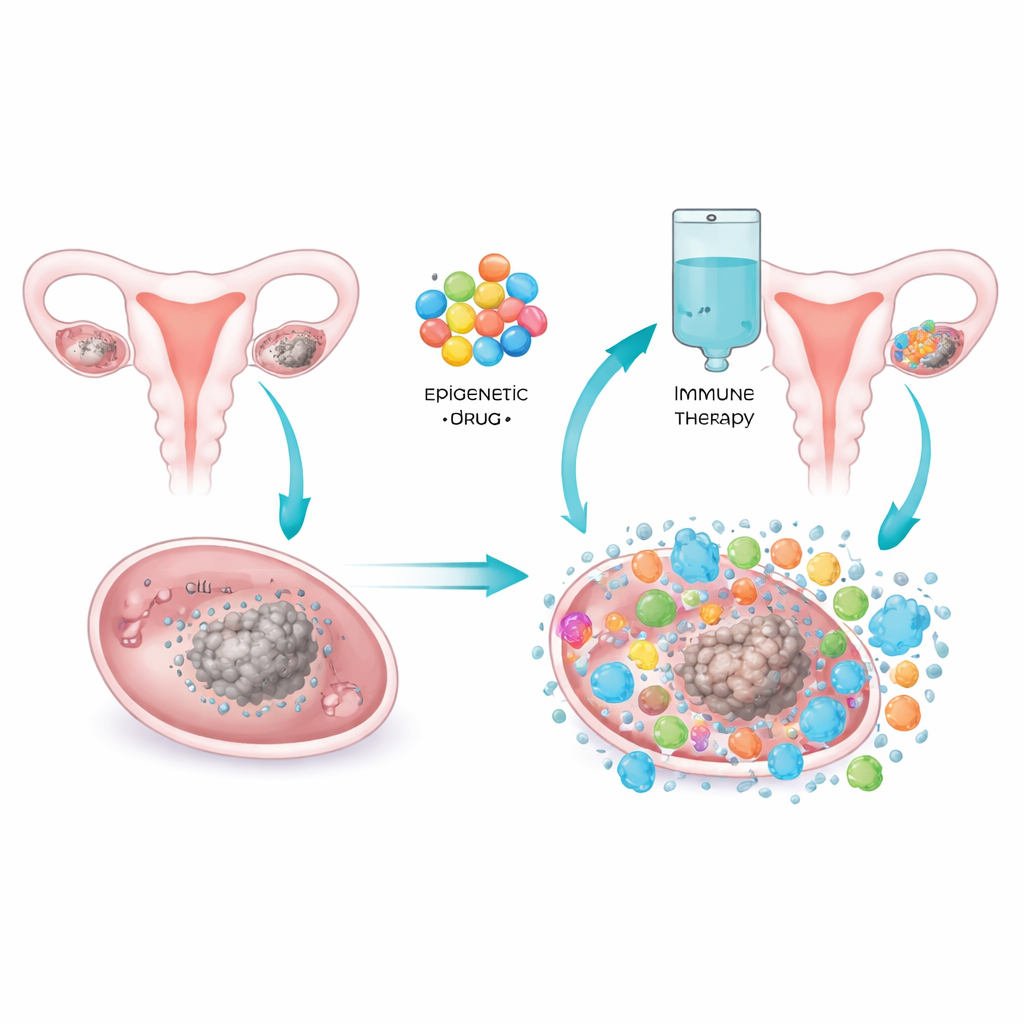
研究团队测试了帕博利珠单抗(一种广泛使用的免疫检查点药物)与口服阿扎胞苷的组合。阿扎胞苷影响DNA上的化学标记,这些标记帮助控制基因活性。通过改变这些标记,阿扎胞苷可以重新唤醒被沉默的基因并在肿瘤细胞内触发类似抗病毒的警报信号。在实验模型中,这种“病毒模拟”能将免疫细胞吸引到之前沉寂的肿瘤中。在这项二期临床试验中,34例铂耐药或铂难治的上皮性卵巢癌女性接受了帕博利珠单抗联合四种不同给药方案之一的口服阿扎胞苷。所有患者均有可测量的病灶,且已接受过标准手术和化疗。
患者中的情况如何
该组合被认为可耐受性中等。常见不良反应包括恶心、呕吐、腹泻、乏力、贫血和白细胞减少,尤其在阿扎胞苷剂量较高时更明显。这些问题大多可通过调整剂量来管理,且未发现超出单药已知范围的意外安全问题。就肿瘤缩小而言,仅一例患者出现部分缓解,且无完全缓解,总体缓解率约为3%。然而,大约一半的女性出现了肿瘤缩小或疾病稳定,疾病控制率为50%。少数患者持续用药超过一年,其中一名女性在改用单用帕博利珠单抗后仍处于缓解状态。
肿瘤环境如何被重塑
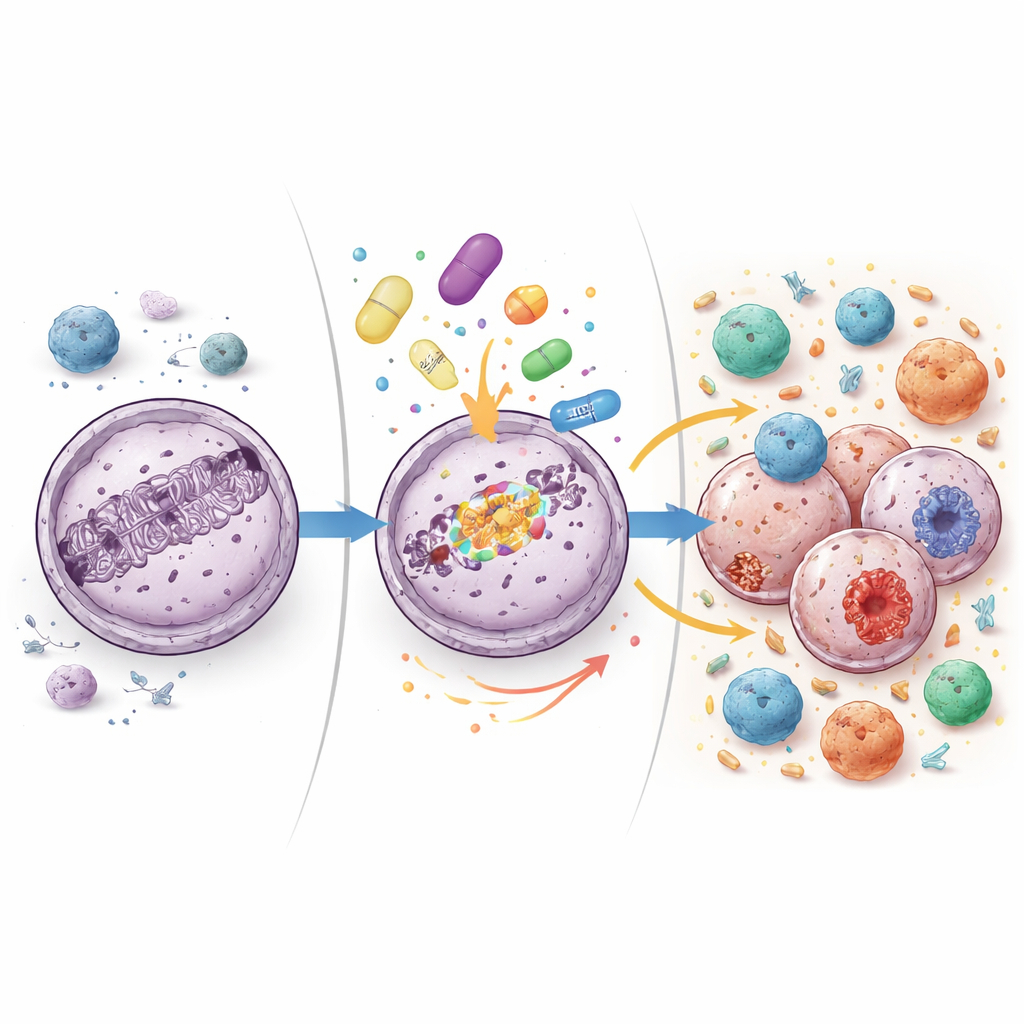
为了观察药物组合在肿瘤内部产生的作用,研究者在治疗前以及开始治疗约六周后采集了组织样本。他们测量了数百个免疫相关基因的活性水平,并对肿瘤RNA进行测序以评估更广泛的变化。治疗后,肿瘤在与炎症、干扰素信号以及向免疫细胞展示肿瘤片段相关的基因上表现出更高的活性。帮助免疫细胞进入并粘附到肿瘤的通路也更为活跃。与此同时,侵入肿瘤的T细胞,尤其是杀伤性亚型的相对数量增加。这些模式表明肿瘤周围环境从沉寂状态向更具炎症性、免疫识别能力更强的状态转变。
从应答者与免疫细胞指纹得到的线索
研究者还分析了那些显示获益迹象的患者模式,无论是血液标志物CA-125下降还是更持久的疾病控制。这些患者的肿瘤在基线时往往在炎症基因程序上具有更高的活性,治疗后表现出更强的适应性免疫反应增强——由识别特异性靶点的T细胞和B细胞驱动。通过从肿瘤RNA重构T细胞受体的重排,研究团队发现肿瘤内的T细胞群体在治疗期间经常发生变化,某些特定细胞克隆扩增或收缩。T细胞格局的这种重塑进一步表明该药物组合在肿瘤内部积极地重塑了免疫对抗态势。
这对患者意味着什么
对于铂耐药的卵巢癌患者而言,这种帕博利珠单抗与口服阿扎胞苷的组合并未显著提高影像学上肿瘤缩小的病例数,与单用免疫治疗相比并不突出。然而,它使约一半的受试者实现疾病控制,并产生了明确的分子证据,显示肿瘤变得更具炎症性并被更多免疫细胞占据。对于非专业读者来说,结论是这些药物似乎能够在这些本来沉寂的肿瘤内“唤醒”免疫系统,尽管在这组小样本、经过多次治疗的患者中,这并不总是转化为显著的肿瘤缩小。作者认为,通过优化剂量、改进阿扎胞苷的给药方式以及使用分子标志物筛选更可能响应的患者,这一“免疫加热”策略有望成为未来卵巢癌治疗的重要组成部分。
引用: Landon, B.V., Boland, J.L., Wahner Hendrickson, A.E. et al. Pembrolizumab and epigenetic modification with azacitidine reshapes the tumor microenvironment of platinum-resistant epithelial ovarian cancer: a phase 2 non-randomized clinical trial. Commun Med 6, 142 (2026). https://doi.org/10.1038/s43856-026-01404-0
关键词: 卵巢癌, 免疫治疗, 表观遗传治疗, 肿瘤微环境, 检查点抑制剂