Clear Sky Science · zh
经表面改造的双药负载肿瘤靶向脂质体纳米颗粒以克服多形性胶质母细胞瘤的治疗耐药性
此项脑癌研究的重要性
胶质母细胞瘤是最致命的脑癌类型之一。即便接受手术、放疗和化疗,大多数患者在确诊后存活时间也仅略超过一年。一个主要问题是常规药物往往难以到达脑内肿瘤,即便到达,肿瘤也会迅速适应并产生耐药性。本研究探索了一种新的方法,将多种药物“悄悄”穿过大脑的天然防线并在肿瘤内部富集,目的是使现有治疗(如放疗)更有效。
用于运送抗癌药物的微小“货车”
研究团队构建了超小的药物载体,称为肿瘤靶向脂质体。这些是由脂质形成的柔软囊泡,尺寸在纳米尺度,可在内部承载药物。团队在这些囊泡表面修饰了一种能识别并黏附胶质母细胞瘤细胞的特异性肽,以帮助颗粒更容易聚集到肿瘤而非健康组织。每个囊泡被设计为同时装载两种抗癌药:要么是依维莫司加长春瑞滨,要么是雷帕霉素加长春瑞滨。这样的组合旨在让两种药物以互补方式攻击肿瘤细胞,而脂质护壳则帮助药物在血液中存活并进入脑内。
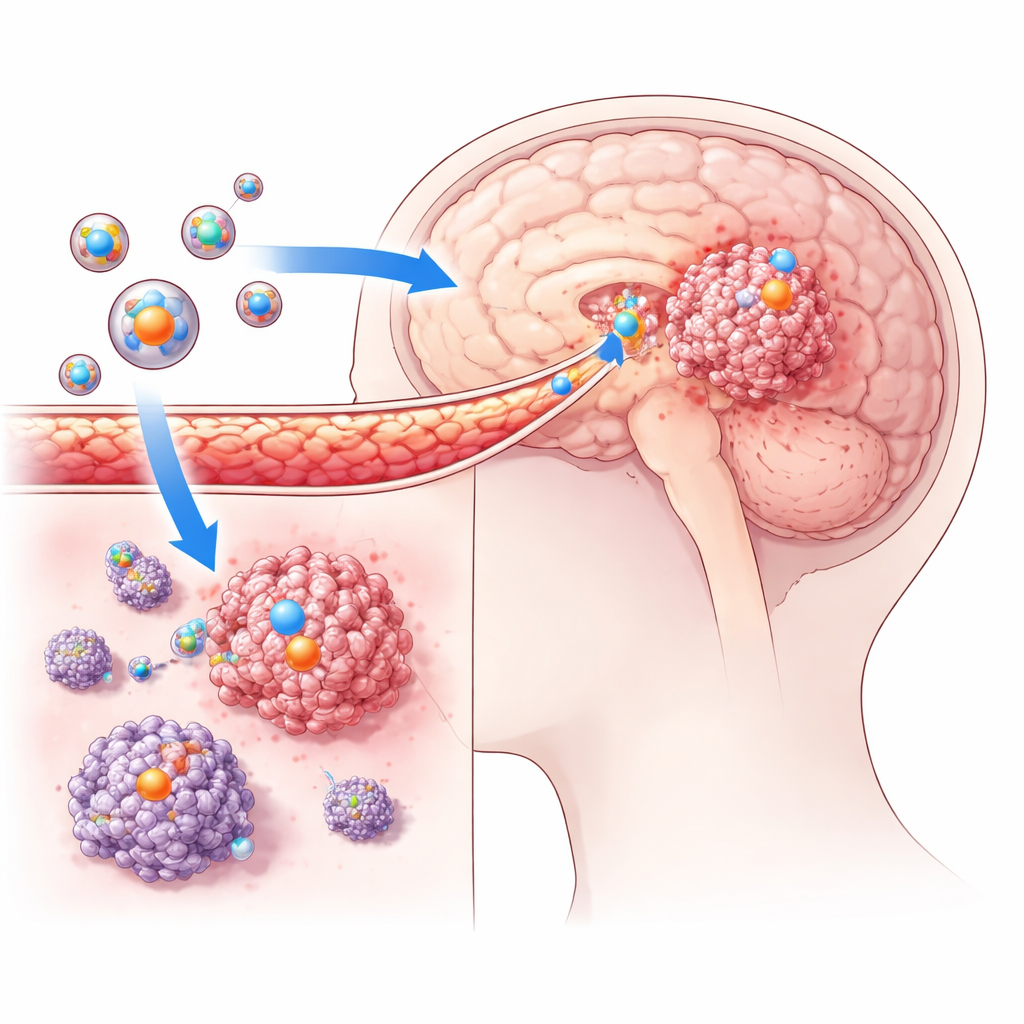
穿越大脑的保护屏障
研究人员在植入了人类胶质母细胞瘤细胞的小鼠模型中测试了这些脂质体能否真正到达脑内肿瘤。他们用荧光染料标记颗粒,并利用先进成像工具跟踪其行程。与非靶向脂质体相比,肿瘤靶向脂质体在脑肿瘤内显示出更强的信号,而在正常脑组织中的信号很弱。这证实了经工程改造的颗粒能够穿过血脑屏障并特异性地在癌细胞生长处积累。在细胞培养实验中,胶质母细胞瘤细胞对靶向脂质体的摄取远高于对照脂质体,进一步支持表面肽显著提高了肿瘤定位和进入的观点。
更强烈地打击肿瘤同时保护身体其他部位
科学家们首先比较了单药脂质体和双药脂质体在培养皿中杀灭癌细胞的效果。双药脂质体,尤其是依维莫司—长春瑞滨组合,比任一单药更具杀伤力,而且优于以非脂质体形式给药的相同药物。当与放疗联合时,效果更显著:癌细胞形成的克隆显著减少,迁移能力下降,并显示出更多损伤迹象。在小鼠脑肿瘤模型中,接受双药脂质体加放疗的动物肿瘤生长更慢、存活期更长,优于仅放疗、仅脂质体或常规替莫唑胺化疗组。重要的是,研究者未见明显的其他器官损伤,这表明将治疗集中于肿瘤可能降低副作用。
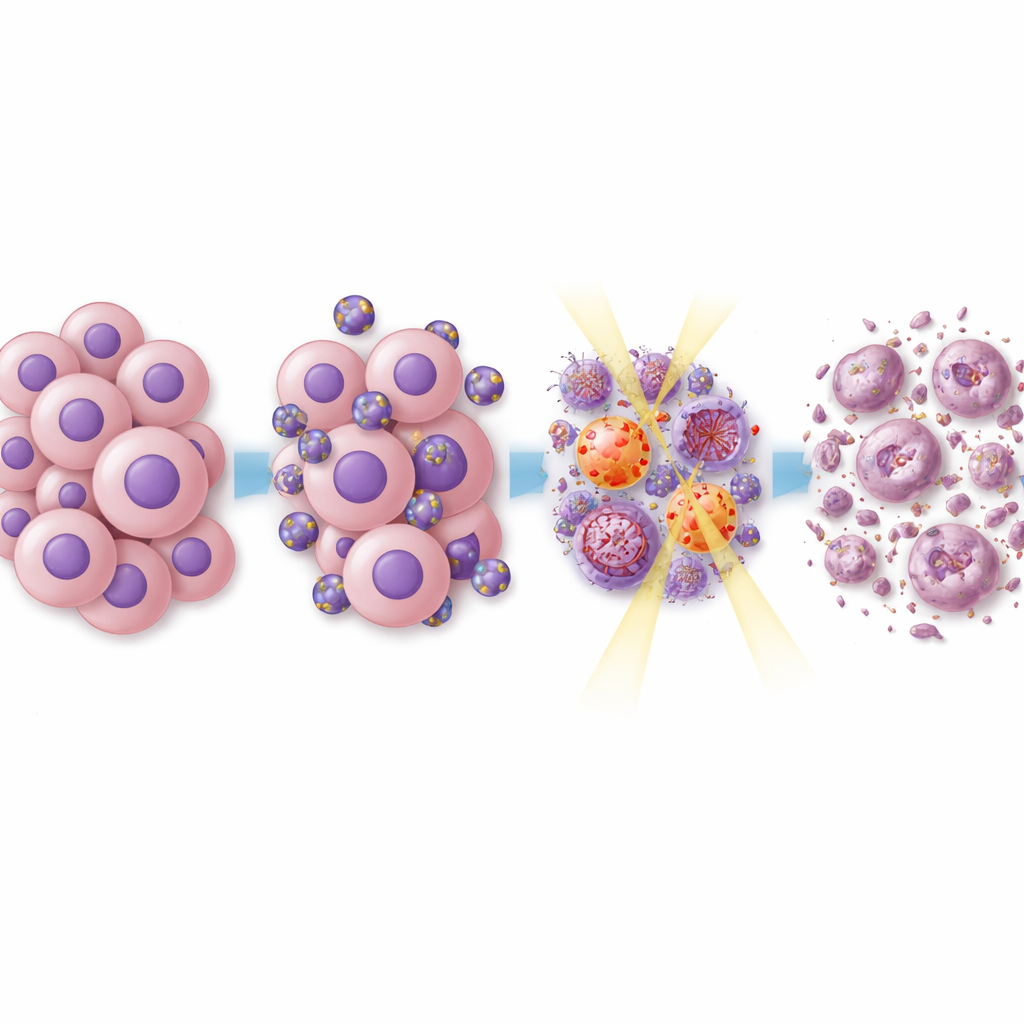
癌细胞内部发生了什么
为了解为何该策略能提高肿瘤对治疗的敏感性,团队检查了癌细胞内的关键信号系统。依维莫司和雷帕霉素已知能抑制名为mTOR的通路,该通路帮助细胞生长并抵抗压力。双药脂质体抑制了与mTOR相关的信号以及推动胶质母细胞瘤细胞分裂与迁移的其他生长路径。当加入放疗时,参与DNA损伤修复的蛋白也被抑制。这意味着肿瘤细胞修复放疗造成的基因损伤的能力下降,更容易走向死亡而非恢复。对被治疗肿瘤的基因表达详尽分析显示,与细胞周期控制、DNA修复和肿瘤与免疫系统相互作用相关的网络发生广泛变化,许多与治疗耐药相关的基因表达被下调。
这对未来患者可能意味着什么
这项工作表明,经过精心设计的肿瘤定向纳米颗粒能够将两种协同药物运送穿过大脑的保护屏障,在胶质母细胞瘤内富集,并增强放射治疗的效果。在小鼠中,该策略减慢了肿瘤生长并延长了生存期,且未见明显额外毒性。尽管这些结果仍处于临床前阶段,距离用于人体尚需大量测试,但该研究指出了一种将靶向药物递送与现有治疗结合以克服高度耐药性癌症的可行路径。如果在人体试验中获得类似益处,这种双药负载脂质体有朝一日可能为胶质母细胞瘤患者带来更长、更高质量的生存期。
引用: Angom, R.S., Rachamala, H.K., Nakka, N.M.R. et al. Surface-engineered dual drug-loaded tumor-targeted liposomal nanoparticles to overcome the therapeutic resistance in glioblastoma multiforme. Commun Med 6, 152 (2026). https://doi.org/10.1038/s43856-025-01279-7
关键词: 胶质母细胞瘤, 纳米颗粒, 脂质体, 脑癌治疗, 放疗增敏