Clear Sky Science · zh
血浆蛋白的结构特征可分类阿尔茨海默病状态
为什么记忆力下降需要血液检测
阿尔茨海默病在记忆问题明显出现之前往往已悄然发展,而现有早期检测方法可能具有侵入性、费用高或难以获取。本研究探讨了另一种思路:血液中循环蛋白三维形状的微小变化,能否揭示个体从健康老化到轻度记忆减退再到明确阿尔茨海默病的进程位置。如果成功,这类血液检测可简化筛查、支持更早期干预,并帮助研究者追踪谁会从新疗法中获益。
关注蛋白结构,而不仅仅是含量
大多数血液检测衡量的是某种分子的含量。这里的研究者则关注蛋白的形状。细胞内的质量控制系统维持蛋白正确折叠;随着年龄增长,这一系统可能失效,导致错误折叠的蛋白累积并损害脑细胞。团队设想,这种“蛋白家务”失调是否会在血液蛋白中留下结构指纹。他们从520名志愿者(包括认知正常者、轻度认知障碍(MCI)患者和阿尔茨海默病患者)采血,使用一种称为共价蛋白谱分析的化学技术标记蛋白中暴露的部位。暴露位点越多越容易被标记,从而给出一个主要独立于蛋白数量的蛋白结构数值读数。
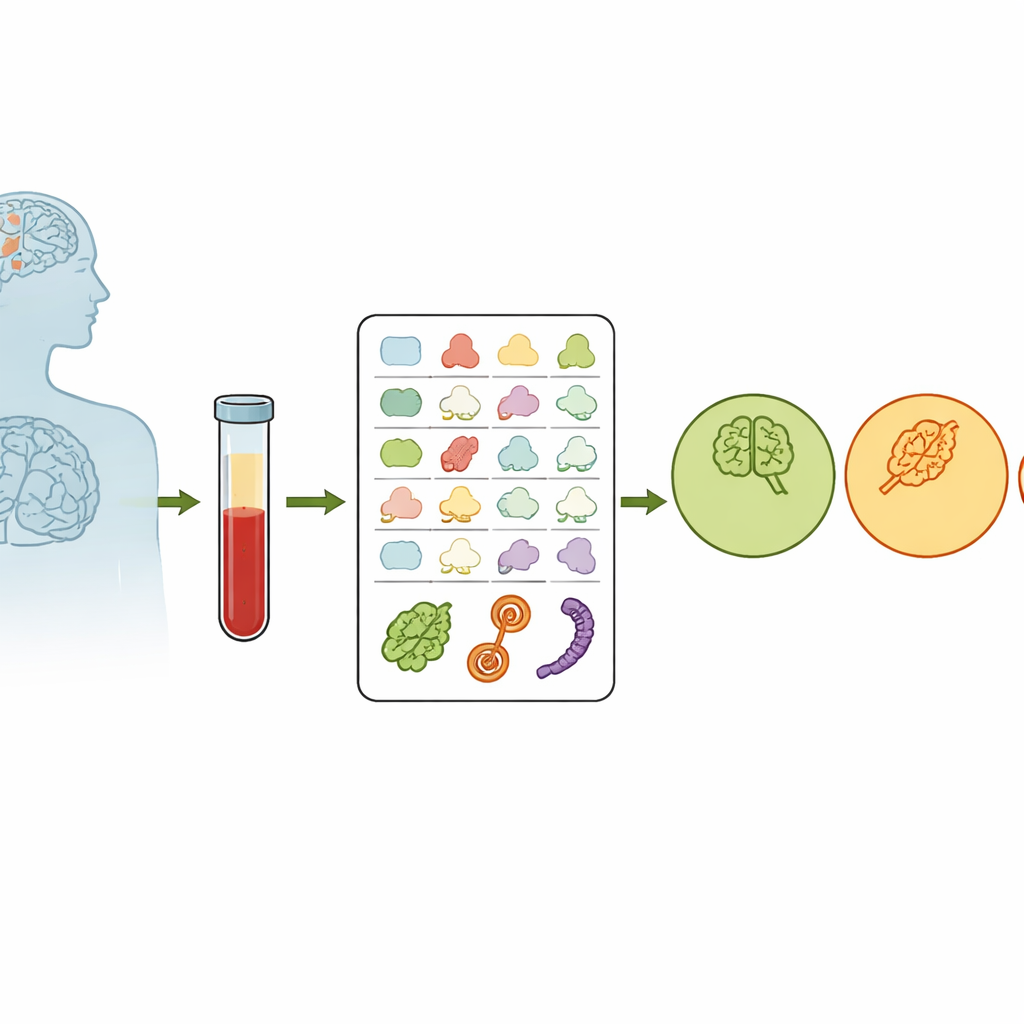
在血液中发现结构指纹
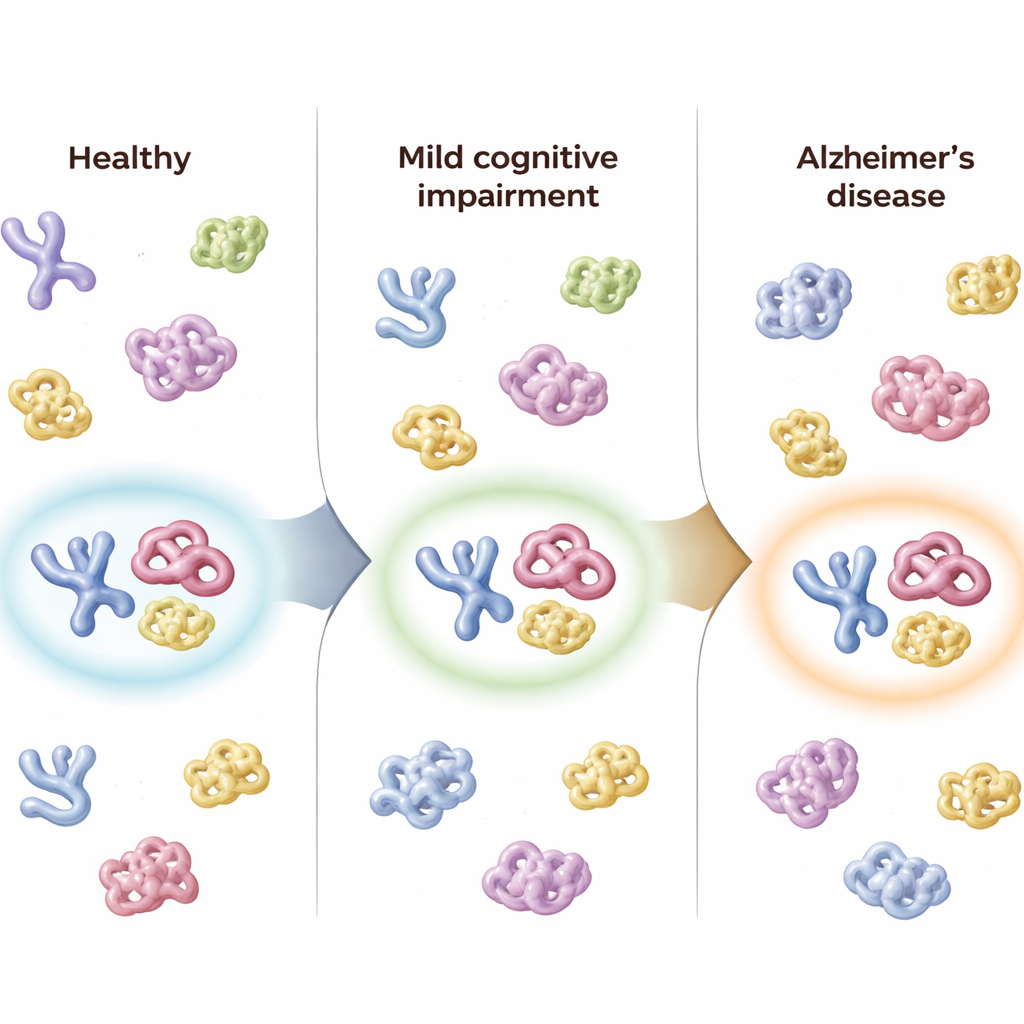
在近900个被标记的蛋白片段中,研究者观察到一种微妙但一致的趋势:从健康到MCI再到阿尔茨海默病,某些蛋白表面变得不那么暴露,并且个体间差异增大。这一模式与随着疾病进展蛋白折叠控制恶化的观点相符。团队还研究了阿尔茨海默病的一个主要遗传风险因子——APOE ε4 变体——如何影响蛋白结构。他们发现携带两份ε4等位基因的人在数种与APOE蛋白相互作用的蛋白中显示出独特的结构变化,这表明该风险基因不仅影响蛋白的存在与否,还改变了它们的折叠与排列方式。
将血液蛋白与情绪与行为联系起来
阿尔茨海默病影响远不止记忆;激越、抑郁和幻觉等症状常见且男女表现常有差异。研究者将12类神经精神症状的临床评分与蛋白结构测量结合分析。在两性中,更严重的症状通常伴随蛋白在结构上变得更“封闭”。一些蛋白,包括clusterin及若干与淀粉样蛋白堆积相关的蛋白,在男女中对症状严重程度的追踪类似,而另一些则表现出性别特异的模式。这些发现暗示,血液蛋白的结构或许不仅反映疾病的存在,也反映其在行为和情绪方面的具体表现。
用于分类病程的三蛋白面板
为将这些复杂测量转化为临床可用的工具,团队将结构数据输入18种不同的机器学习方法中。表现最好的模型基于深度学习,仅依赖来自C1QA、clusterin(也称CLUS)和载脂蛋白B(ApoB)的三个蛋白片段。仅用这三处片段的结构读数,该模型在独立测试集中约83%的情况下能正确将受试者分为健康、MCI或阿尔茨海默组。当问更简单的两类问题——例如区分健康与MCI,或MCI与阿尔茨海默——该面板的表现更强,准确率可与甚至优于许多当前基于蛋白含量而非结构的血液方法相当或更好。
随访人群随时间的变化
研究者还对50名参与者在约八个月内的随访样本进行了检测。在诊断恶化的人群中——例如从健康变为MCI,或从MCI进展为阿尔茨海默——三蛋白面板的综合得分朝同一方向变化,反映了疾病进展。相对地,临床状态未改变的个体其面板得分变化很小。该面板的总体“阿尔茨海默信心”评分与标准认知测试、日常功能测量、MRI上观察到的大脑萎缩以及已确立的脑脊液淀粉样蛋白与tau标志物密切相关,表明血液中的结构信号反映了潜在的大脑变化。
这对患者意味着什么
综合来看,该研究表明仅少数几种丰富血浆蛋白的微小、协调的形状变化即可可靠地指示个体是认知正常、轻度受损还是患有阿尔茨海默病。由于该检测使用血液而非脑脊液或影像学检查,原则上可推广用于常规筛查或在临床试验中选择与监测受试者。作者也提醒需要更大规模和更长期的研究,且相关化学技术仍属专门领域。尽管如此,他们的结果指出蛋白结构——而不仅是蛋白水平——是用于更早且更精准检测与追踪阿尔茨海默病的一个有前景的新信息来源。
引用: Son, A., Kim, H., Diedrich, J.K. et al. Structural signature of plasma proteins classifies the status of Alzheimer’s disease. Nat Aging 6, 597–611 (2026). https://doi.org/10.1038/s43587-026-01078-2
关键词: 阿尔茨海默病生物标志物, 痴呆血液检测, 蛋白折叠变化, 机器学习诊断, clusterin 与 C1QA