Clear Sky Science · zh
产后乳腺退化过程中衰老的诱导支持组织重塑并促进产后肿瘤发生
这对新妈妈为什么重要
分娩后,乳房需要迅速从产奶状态切换回静息状态。这个戏剧性的改造过程称为退化(involution),长期以来被认为与产后几年内乳腺癌风险短暂上升有关,但其生物学原因并不明确。这项小鼠研究表明,一种特殊的“退休”状态——细胞衰老,有助于断奶后的乳腺愈合——但相同的程序也可能被萌芽中的肿瘤利用以生长和扩散。理解这一双刃过程或能为保护女性免受产后乳腺癌提供新途径。
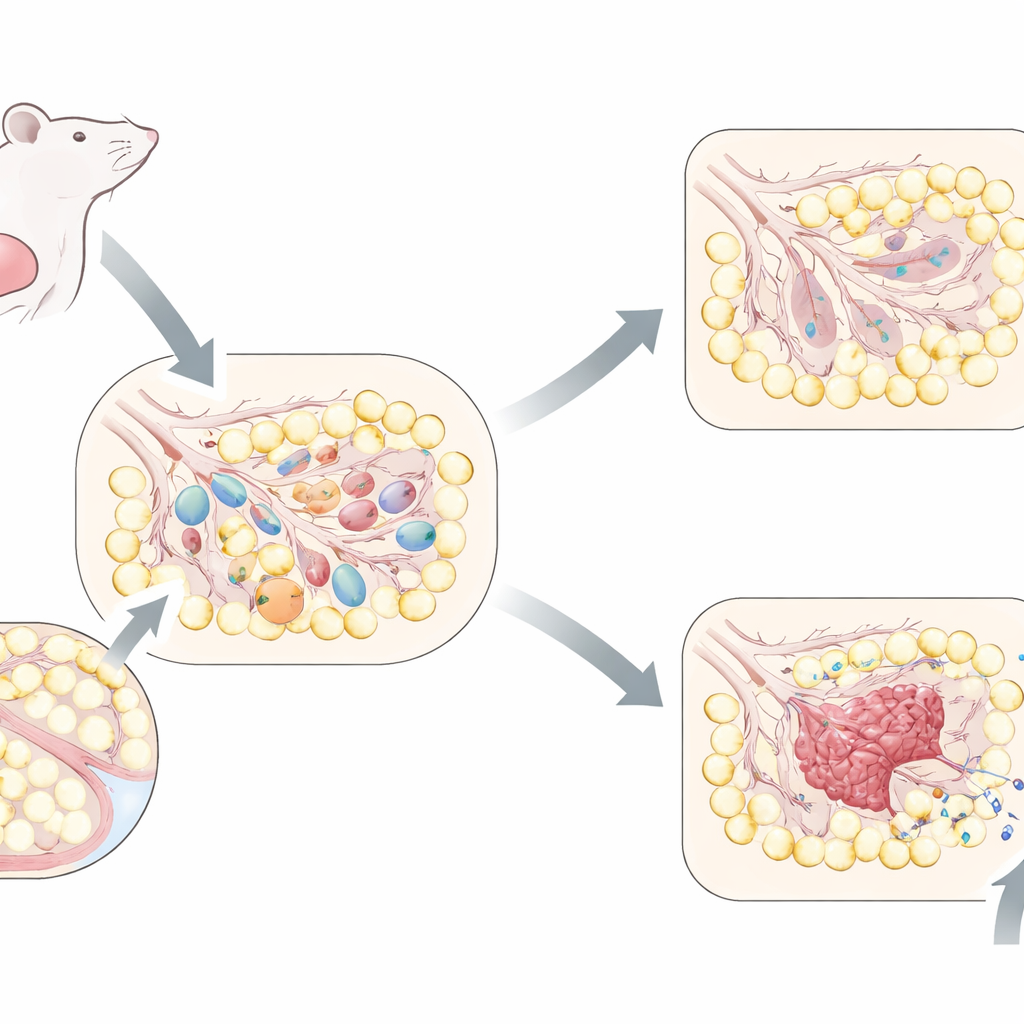
断奶后发生的剧烈重塑
在怀孕和哺乳期间,乳腺扩展为由许多产生并储存乳汁的小囊构成的致密网络。一旦停止哺乳,大多数产奶结构便不再需要。在小鼠中,组织经历一系列严格时序的变化:首先,许多产奶细胞死亡,随后脂肪细胞重新填充空间并重塑支撑结构。作者在多个时间点追踪了这一过程,发现断奶后几天,具有衰老特征的一阵细胞专门出现在产奶单位。这些细胞随着腺体恢复到孕前形态而逐渐消失,表明衰老是正常重塑过程中的短暂且程序化的一环,而非随年龄积累的现象。
帮助重塑乳房的“退休”细胞
衰老细胞常被视为衰老的元凶,因为它们停止分裂但释放大量可引发炎症或损伤邻近组织的信号分子。然而在此处,衰老细胞似乎具有建设性作用。研究者使用遗传工具仅在产奶细胞中破坏了关键的衰老开关基因p16,并使用一种选择性清除衰老细胞的药物。在这两种情况下,当衰老减少时,退化的早期阶段减慢:产奶结构比正常情况停留更久,脂肪细胞重新填充效率降低,腺体整体结构重置需要更长时间。团队还显示这些衰老细胞释放的信号能吸引一种称为巨噬细胞的免疫细胞,而巨噬细胞已知有助于清除死亡细胞并引导组织修复。在这种情境下,衰老表现得像一个临时的“工头”,协调断奶后的清理和重建工作。
有益修复如何成为癌症同谋
使衰老细胞成为强大修复协调者的特性,在存在癌变细胞时也会带来风险。产后乳腺癌比从未生育女性被诊断出的乳腺癌更易发生转移且更致命。在易患乳腺肿瘤的小鼠模型中,一次妊娠并随之发生退化会导致肿瘤更早出现。当研究者在退化期通过基因手段抑制衰老或用清除衰老细胞的药物ABT‑263清除衰老细胞时,肿瘤出现得更晚且更少。在体外培养的肿瘤类器官实验中,从富含衰老细胞的退化腺体收集的液体使癌细胞更具侵袭性,而来自衰老减少腺体的液体作用较弱。这些实验表明,衰老细胞通过其分泌因子的混合物,增加了邻近肿瘤起始细胞的可塑性和侵袭性。
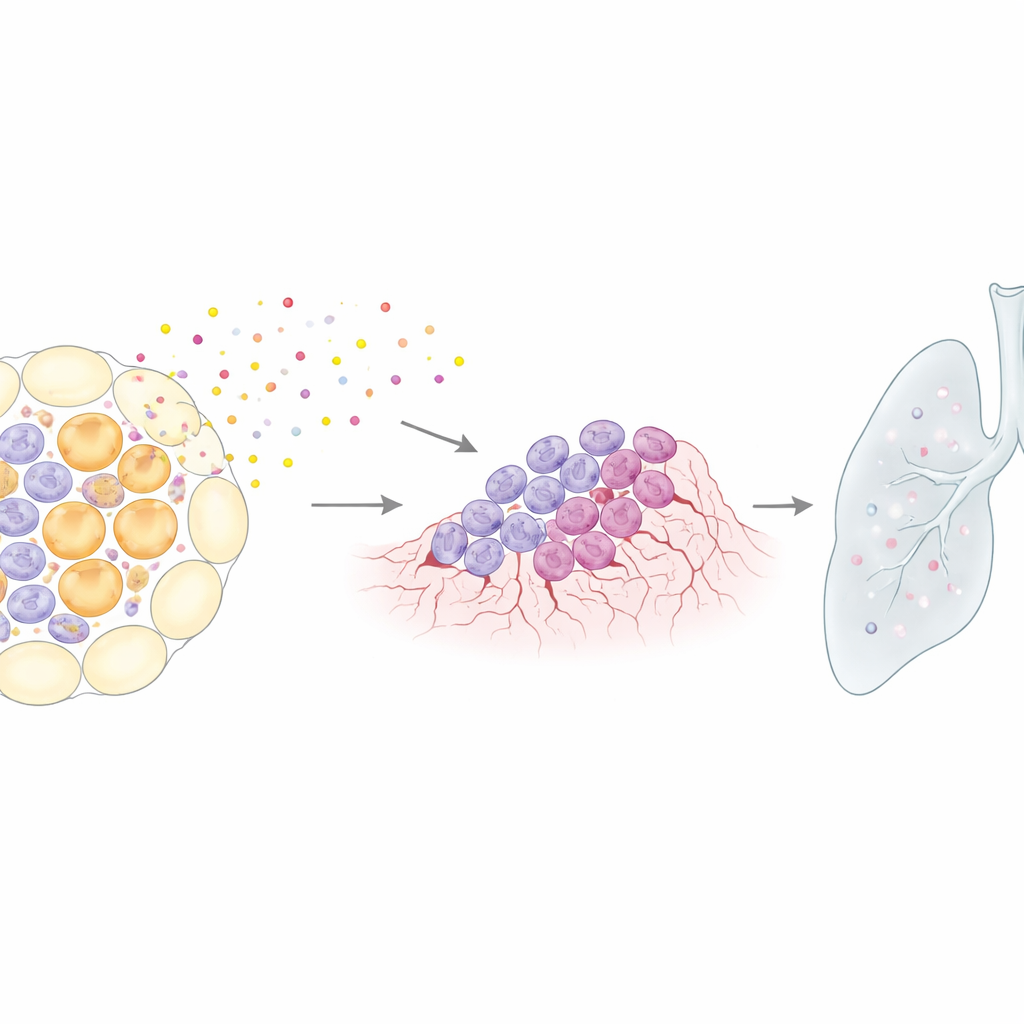
从局部变化到远处扩散
团队进一步检验这种由衰老驱动的环境是否会鼓励癌细胞超出乳腺迁移。他们将具有侵袭性的乳腺肿瘤细胞植入静息或退化期的乳腺。在退化的腺体中,肺转移常见,但在退化期用ABT‑263清除衰老细胞时,肺及其他器官的转移显著减少,尽管该药并未在非退化动物中直接损伤肿瘤细胞。这表明产后重塑期创造了一个短暂窗口,衰老细胞在其中帮助肿瘤播种并在远处定殖。有趣的是,当哺乳期间再次怀孕——从而延迟完全退化及其衰老波——妊娠后通常加速的肿瘤形成被削弱,这与衰老重塑阶段是高风险间隔的观点一致。
这对产后乳腺癌意味着什么
总体而言,研究揭示产后乳腺退化期间的衰老是一个受激素调控的程序化步骤,帮助腺体安全地从“奶厂”过渡回静息器官。然而,如果存在易癌或已异常的细胞,相同的衰老细胞可以通过大量信号分子促进肿瘤生长、侵袭和转移。对非专业读者而言,结论是:人体自身的伤口愈合工具在像产后这样的脆弱时刻可能被癌症劫持。未来,精心时机的针对衰老细胞或其释放信号的治疗,或许可以在保留正常组织修复益处的同时,降低产后乳腺癌风险的上升。
引用: Chiche, A., Djoual, L., Charifou, E. et al. Induction of senescence during postpartum mammary gland involution supports tissue remodeling and promotes postpartum tumorigenesis. Nat Aging 6, 541–559 (2026). https://doi.org/10.1038/s43587-025-01058-y
关键词: 产后乳腺癌, 细胞衰老, 乳腺退化, 肿瘤转移, 清除衰老细胞疗法