Clear Sky Science · zh
铂类化疗在肺癌和卵巢癌中产生耐药性的原因是可被靶向的TGFβ衰老分泌表型
当癌症治疗适得其反
铂类化疗是现代癌症治疗的重要工具,尤其用于肺癌和卵巢癌。其作用机制是造成肿瘤DNA的严重损伤,使癌细胞无法继续分裂。然而,许多患者的肿瘤在最初缩小后会复发,并且比之前更难以治疗。这项研究提出了一个简单却令人不安的问题:那些拯救生命的药物是否也会帮助存活下来的癌细胞反扑?作者发现,答案在于一类受损且类似衰老的细胞以及它们释放的强有力化学信号。
衰老癌细胞的双重身份
化疗并不会以相同方式对待所有肿瘤细胞。有些细胞会被直接杀死,而另一些进入一种称为细胞衰老的状态——永久停止分裂,但仍然存活。这些衰老细胞体积增大并开始分泌一组蛋白和信号分子,称为衰老相关分泌表型(SASP)。在体外的人类肺癌和卵巢癌细胞以及小鼠模型中,研究人员证明铂类药物(如顺铂和卡铂)会诱导产生尤其强效的衰老细胞。当将新鲜的癌细胞置于这些衰老细胞培养液中时,受处理的细胞比对照细胞生长更快、迁移能力更强,并形成更大、更具侵袭性的集落与球体。
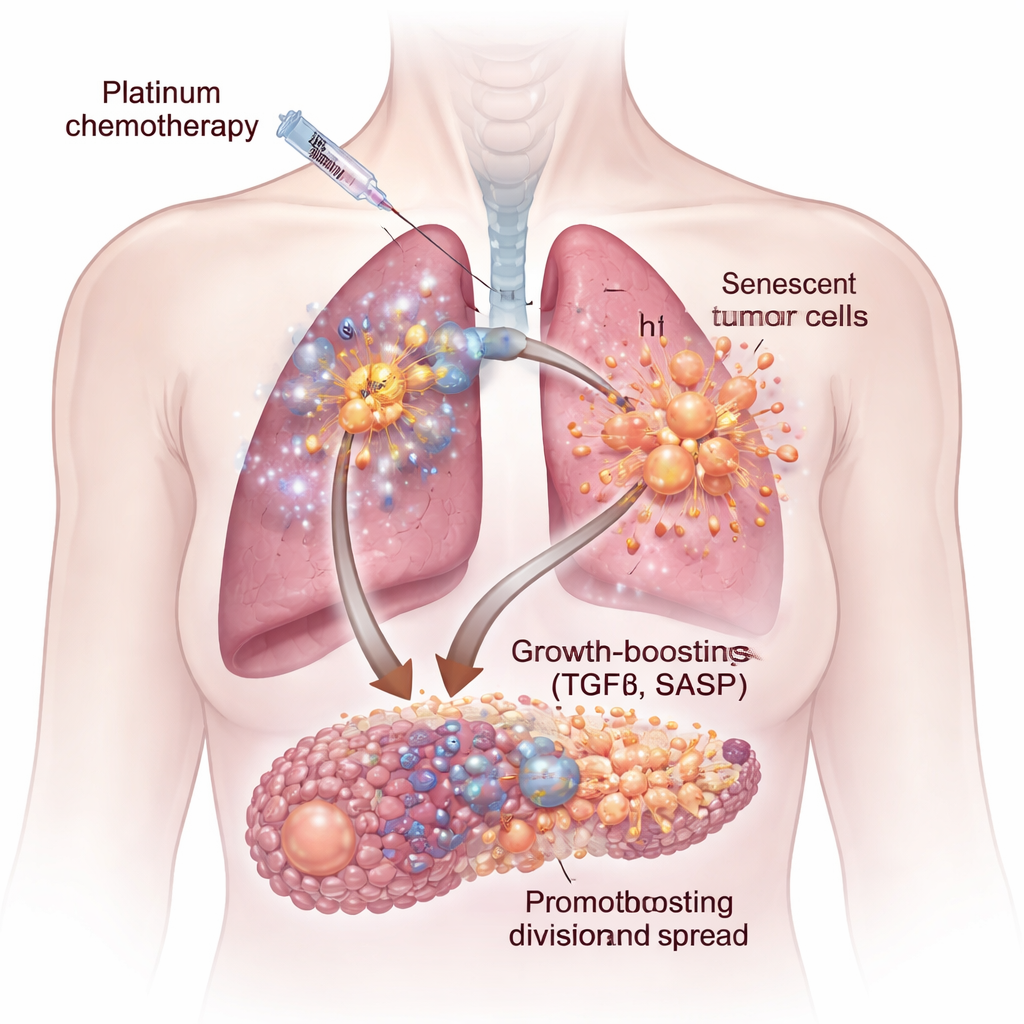
隐藏的促生长信号:TGFβ
并非所有化疗都会触发相同的有害分泌物。当研究组将铂类药物与另外两种常用药物多西他赛和帕博昔布比较时,只有铂处理的细胞产生的SASP显著促进肿瘤生长。通过结合基因表达分析、蛋白测定以及高通量微环境微阵列,他们锁定了一个关键元凶:转化生长因子-β(TGFβ)。由顺铂诱导的衰老细胞在多种TGFβ形式和相关通路上富集。向癌细胞中添加纯化的TGFβ可以复制用衰老细胞培养液观察到的生长促进效应,表明这一细胞因子家族是促肿瘤分泌表型的核心驱动因子。
信号如何重塑癌细胞
研究进而追踪了这些富含TGFβ的信号如何改变邻近肿瘤细胞的行为。TGFβ在受体TGFBR1的细胞表面结合后,会激活细胞内一系列蛋白链,尤其是已知调控细胞生长、代谢和存活的AKT和mTOR通路。在人类和小鼠的肺癌细胞中,暴露于顺铂来源的分泌物后,AKT及其下游靶点p70S6K的活化(磷酸化)形式迅速增加,并提升了细胞周期基因的表达。用药物galunisertib阻断TGFBR1或直接抑制mTOR,可在很大程度上关闭这一信号激增,并减少衰老分泌表型所诱发的额外增殖、集落形成和侵袭性球体生长。
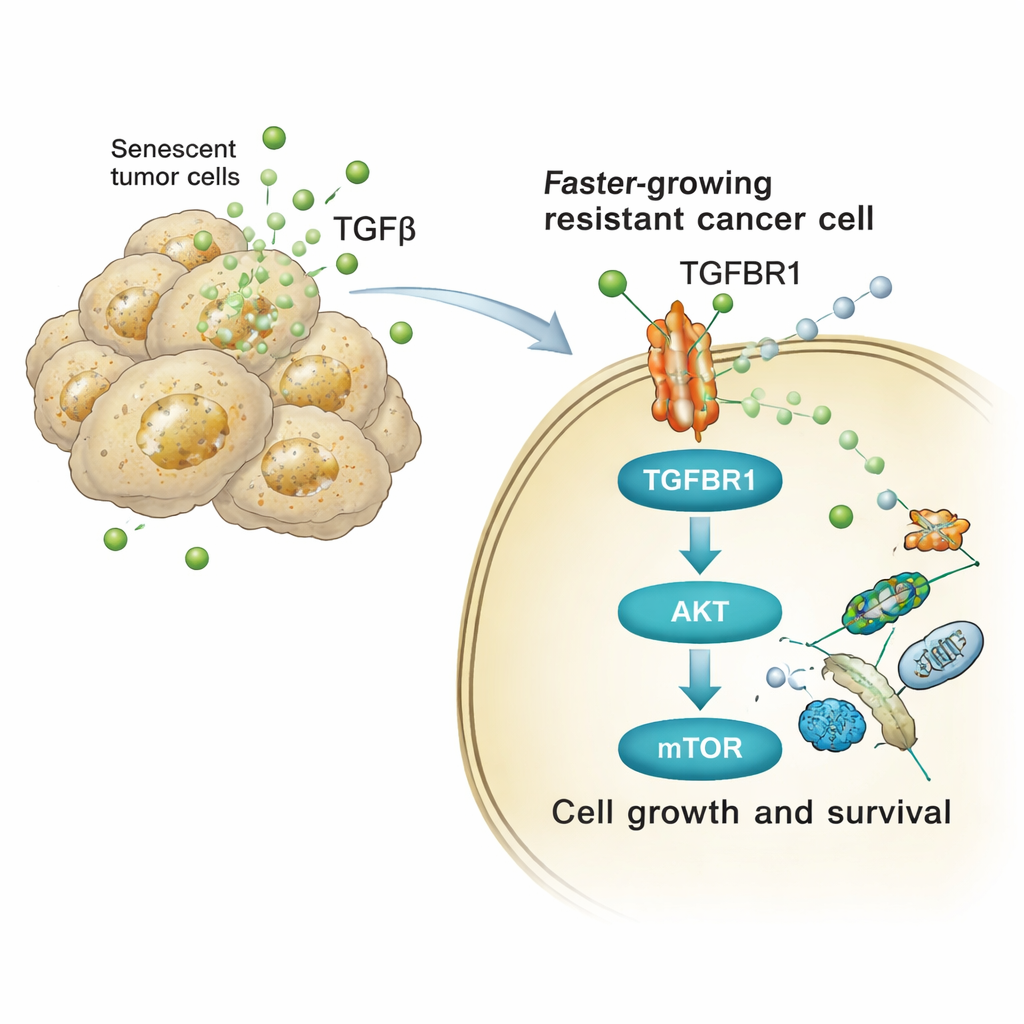
从小鼠到患者:共同的脆弱点
这些机制并非仅限于培养皿。在携带肺肿瘤的小鼠中,混合注入衰老与非衰老的癌细胞会导致肿瘤生长加速、存活期缩短,而清除衰老细胞或阻断TGFBR1则可遏制此效应。当对患有基因工程肺癌的小鼠给予常规顺铂治疗时,肿瘤中出现了衰老标志物的积累,同时在邻近仍在分裂的细胞中观察到较高的AKT/mTOR活性。将顺铂与TGFBR1抑制剂或清除衰老细胞的药物(senolytic)联合使用,则在降低肿瘤负担和延长存活方面优于单纯化疗,且未见明显额外毒性。关键的是,对接受铂类治疗后的人类肺癌和高级别浆液性卵巢癌样本的分析显示了类似模式:肿瘤微环境中衰老标志物增加,并在富含衰老细胞的区域伴随AKT/mTOR信号增强。
将弱点转为优势
对普通读者而言,核心结论是:铂类化疗可能留下一群受损但危险的“僵尸”细胞。这些衰老肿瘤细胞本身不再分裂,但会大量分泌富含TGFβ的信号,唤醒周围的癌细胞,帮助肿瘤复发并抵抗后续治疗。令人鼓舞的是,这一弱点是可以被针对的。在肺癌和卵巢癌的基础研究模型中,加入阻断TGFβ受体TGFBR1的药物或选择性清除衰老细胞的药物可以使铂类化疗更为有效并改善生存率,而未见明显额外毒性。该研究为未来将标准铂类治疗与senolytic或抗TGFβ策略联合的临床试验提供了理论依据,旨在在保留化疗益处的同时解除其由衰老驱动的隐性副作用。
引用: González-Gualda, E., Reinius, M.A.V., Macias, D. et al. Treatment resistance to platinum-based chemotherapy in lung and ovarian cancer is driven by a targetable TGFβ senescent secretome. Nat Aging 6, 368–392 (2026). https://doi.org/10.1038/s43587-025-01054-2
关键词: 化疗耐药, 细胞衰老, TGFβ 信号, 肺癌, 卵巢癌