Clear Sky Science · zh
巨噬细胞内的DNA损伤通过核抗原呈递驱动免疫自身反应
当细胞磨损把免疫系统变成对己方的攻击者
衰老会增加患自身免疫性疾病的风险,此类疾病中免疫系统开始攻击本应保护的机体。该研究探讨了一个令人意外的罪魁:存在于称为巨噬细胞的免疫细胞内的日常DNA损伤。通过追踪这些损伤如何改变巨噬细胞向其他免疫细胞展示的内容,研究者揭示了一个可能将衰老与像狼疮这样的疾病联系起来的缺失环节。
失控的身体守护者
巨噬细胞是前线防御者,会吞噬微生物和碎屑,然后将蛋白片段呈递给T细胞,帮助免疫系统决定攻击目标。研究团队设计的老鼠其巨噬细胞在关键DNA修复蛋白ERCC1-XPF上有缺陷,导致这些细胞携带持续的DNA损伤。随着这些小鼠变老,它们出现了自身免疫的标志性特征:肾脏的炎性灶、免疫复合物和补体蛋白的沉积、脾脏肿大以及与自然老年动物相似的高滴度抗核抗体。详细的免疫谱系分析显示浆细胞、活化T细胞和自然杀伤细胞的扩增,这些都是免疫系统长期刺激的征兆。
从破损的DNA到自我靶向的T细胞
巨噬细胞内的DNA损伤如何触发如此强烈的类自身免疫反应?研究者发现DNA断裂激活了这些细胞中的经典损伤反应通路,涉及ATM、ATR和DNA-PK等酶。该信号通路提高了表面MHC II的水平,MHC II是用于向CD4 T细胞呈递蛋白片段的分子展示架。当带有DNA损伤的巨噬细胞与T细胞共培养时,它们比正常巨噬细胞更强烈地驱动T细胞活化和干扰素-γ的产生。阻断MHC-II或干扰DNA损伤反应可以逆转大部分这一效应,在活体动物中,中和MHC-II的抗体或耗竭CD4 T细胞的处理则减少了肾脏炎症和自身抗体水平。
来自细胞核的自体蛋白被摆上舞台
为确切了解受损巨噬细胞向T细胞展示了什么,团队分离了结合在MHC-II上的肽并用质谱进行了分析。与正常或脂多糖刺激的细胞相比,DNA受损的巨噬细胞呈现出明显不同的肽组单。它们的MHC-II分子富集了来自核和核糖体蛋白的片段,而非主要来自膜和细胞外蛋白的片段,包括组蛋白和其他与DNA密切相关的成分。当将部分这些核肽合成并用于重新刺激工程小鼠的免疫细胞时,它们诱发了强烈的T细胞反应,表明这些来源于自体的片段确实具有免疫原性。
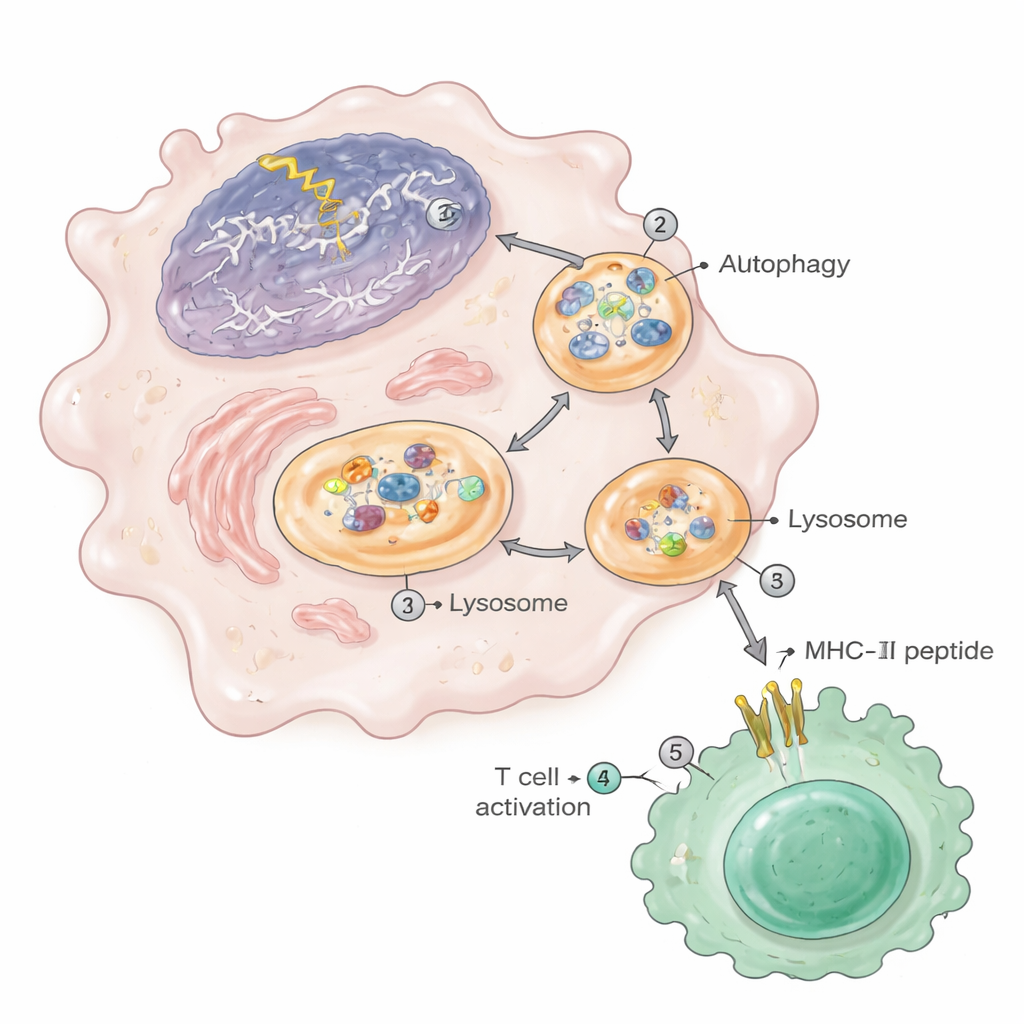
自噬:助长自身免疫的清理通路
核物质被送入MHC-II展示通路的过程在很大程度上依赖于自噬——细胞的内部回收系统。在DNA损伤下,自噬增强并将来自细胞自身细胞核的染色质片段运送到自噬体,随后与溶酶体融合,在那里蛋白被分解成肽。这些受损巨噬细胞的溶酶体中含有升高的核和核糖体蛋白水平。当研究者用药物阻断自噬或在同类髓系细胞中遗传性缺失一个关键自噬基因(Atg5)时,动物显示出更少的肾脏病变、较少的活化T细胞和浆细胞,以及出现在MHC-II上的核肽显著减少。在易罹患狼疮的小鼠、暴露于DNA损伤药物的人单核细胞系以及非常年老的小鼠的巨噬细胞中也观察到类似的染色质片段和增强的抗原呈递。
这对衰老和自身免疫性疾病意味着什么
综合来看,研究结果提出了一个简单但有力的观点:随着年龄增长,巨噬细胞中累积DNA损伤,这些细胞又通过自噬清除核碎片。在此过程中,它们无意中将核物质切割成肽,并把这些肽加载到MHC-II上,像对待外来物一样向T细胞展示。长期反复接触这些核的自身抗原会训练免疫系统对机体自身发生反应,促进自身免疫。通过明确这一从DNA损伤到自噬再到核抗原呈递的通路,研究突出了抑制与年龄相关自身免疫的新策略,例如增强DNA修复、精细调控自噬,或选择性阻断核自体肽的呈递,而不关闭免疫系统的重要防御功能。
引用: Niotis, G., Arvanitaki, E.S., Theodorakis, E. et al. DNA damage in macrophages drives immune autoreactivity via nuclear antigen presentation. Nat Aging 6, 393–413 (2026). https://doi.org/10.1038/s43587-025-01053-3
关键词: 衰老与自身免疫, DNA损伤, 巨噬细胞, 自噬, 抗核抗体