Clear Sky Science · zh
Senotoxins 通过脂质结合特异性、离子失衡和脂质组重塑靶向衰老细胞
为什么杀死“僵尸”细胞可以增强癌症治疗
随着年龄增长——或在接受像化疗这样强烈的治疗时——有些细胞停止分裂却拒绝死亡。这些被称为衰老细胞的“僵尸”细胞会分泌促炎分子,损害组织并可能助长肿瘤复发。本研究探讨了一种令人惊讶的新方法,利用来源于毒液的蛋白质选择性消除这些问题细胞,有望使癌症治疗更强效且更安全。
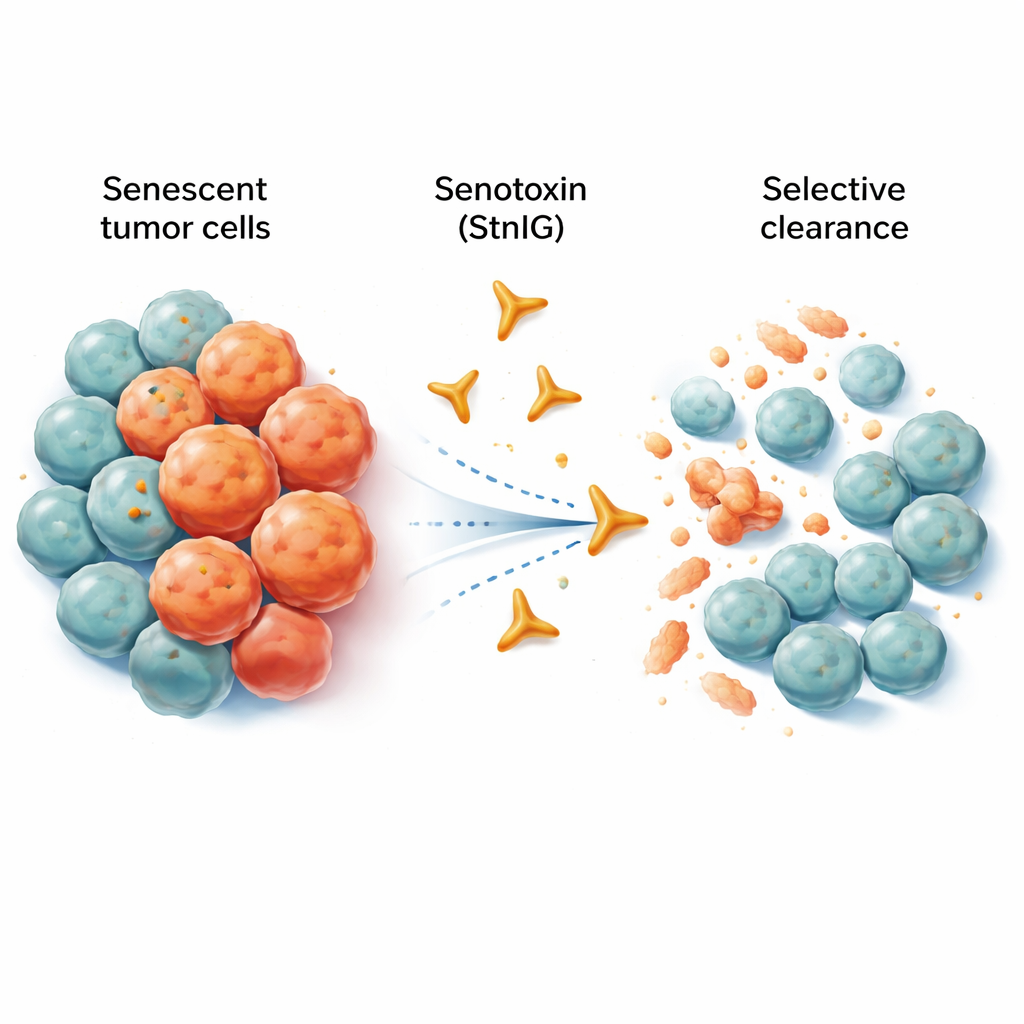
挥之不去的老细胞
衰老细胞就像退休但仍占着工位、扰乱办公室秩序的员工。它们不再增殖,但会释放混合的促炎信号,削弱邻近组织、促进衰老,甚至支持肿瘤生长和转移。化疗在杀死许多癌细胞的同时,常常在肿瘤内部及周围留下大量衰老细胞。这些残存细胞会助长慢性炎症、引发副作用,并最终促成复发。现有的实验性药物——称为清除衰老细胞的药物(senolytics)——旨在去除衰老细胞,但许多此类药物要么也会伤及健康细胞、要么有效剂量窗口很窄、要么难以被机体吸收。
把海葵毒液变成精准工具
研究者转向了自然界擅长杀伤细胞的武器:动物毒液。他们关注一种来自加勒比海海葵的成孔蛋白,称为 sticholysin I(StnI)。这种蛋白能在细胞膜上打出微小孔洞。团队发现,StnI 及其经过改造的版本 StnIG 在杀死衰老的癌细胞方面远胜于对非衰老细胞的作用。对多种经化疗药物诱导进入衰老状态的人类癌细胞(黑色素瘤、肝癌、肺癌和来源于神经的肿瘤)进行测试后,StnI,尤其是 StnIG,在远低于影响增殖细胞所需剂量下就能消灭这些衰老细胞。StnIG 的选择性优于一种领先的实验性清除衰老细胞药物 navitoclax,表明经过精细调控的毒素有望超越现有方法。
改变的细胞膜如何成为阿基里斯之踵
衰老细胞不仅在内部发生变化;它们的外膜——包裹细胞的脂性“皮肤”——也会重塑。在健康细胞中,某些脂质主要分布在膜的内侧,对外界隐藏。在衰老细胞中,这种平衡被打破,这些脂质被暴露到外表面。通过详细的化学分析和计算机模拟,团队表明 StnIG 能识别并黏附于这种改变的脂质景观。其结构特别适合锁定衰老细胞表面暴露的特定脂质。一旦结合,StnIG 会形成孔洞,使带电原子(离子)出现高度失衡的进出流动。
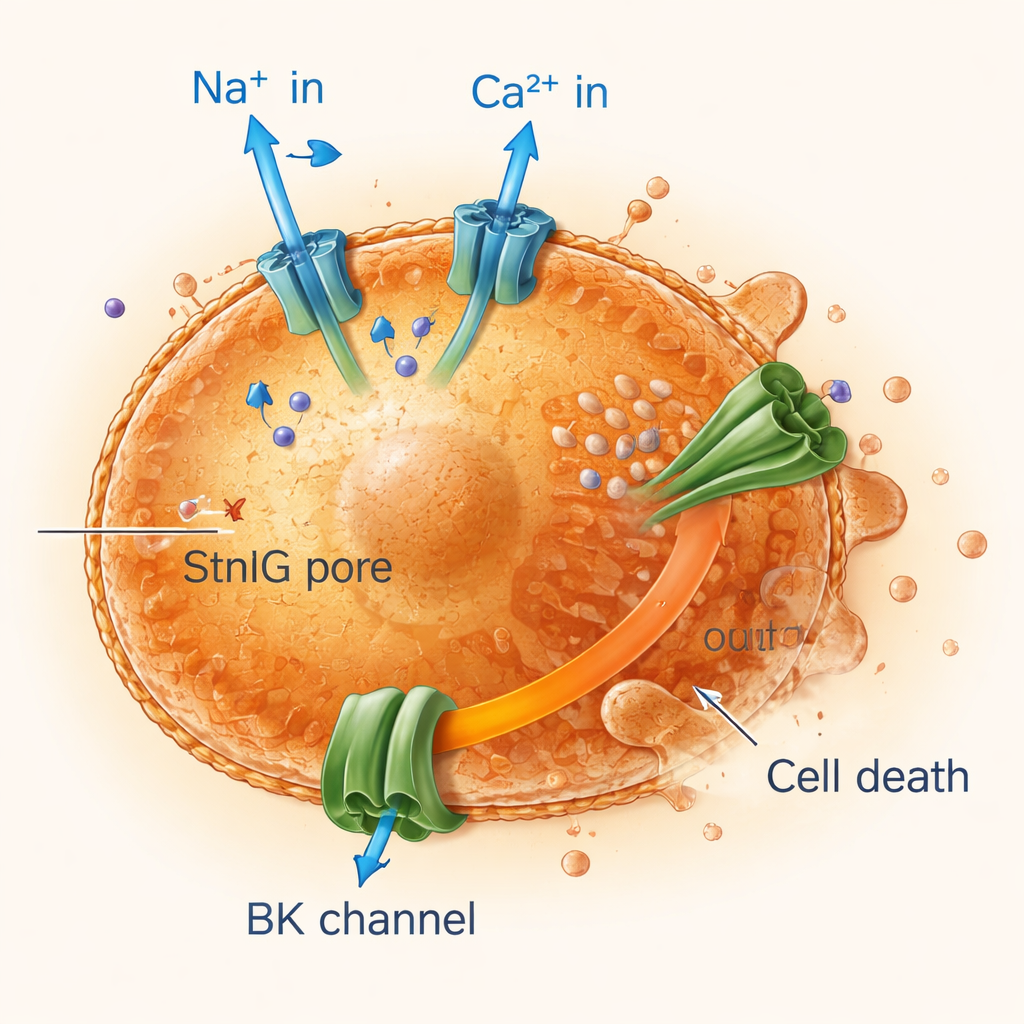
用离子失衡短路老化细胞
通过追踪跨膜电流和离子流动,研究者发现 StnIG 的孔允许钠和钙离子大量涌入衰老细胞,同时钾持续泄漏。钙的激增会开启大型钾通道,放大钾的流失,而钾对于维持细胞体积和生存至关重要。衰老细胞本已较健康细胞不那么灵活且更脆弱,无法应对这种持续的离子紊乱。它们的线粒体——细胞的动力工厂——失去膜电位,能量生成骤降,细胞经历程序性死亡,包括凋亡和一种伴随强烈炎症的死亡形式——焦亡。阻断钙进入或钾通道可以保护衰老细胞,证实这种离子扰动是毒素作用的核心。
从细胞培养皿到活体动物
团队随后测试该策略在活体中的效果。在携带人类衰老黑色素瘤细胞的斑马鱼胚胎中,低剂量 StnIG 与 navitoclax 同样有效地减少了这些细胞,且未见明显毒性。在黑色素瘤和肝癌的小鼠模型中,使用细胞周期抑制药(palbociclib)化疗可通过使许多癌细胞进入衰老状态来减缓肿瘤生长。当研究者间歇性追加 StnIG 时,肿瘤较单用化疗缩小或进入缓解的效果更佳,且与化疗加 navitoclax 的组合相当。重要的是,接受 StnIG 治疗的小鼠显示出有限的副作用,主要器官未见明显损伤,但携带衰老肿瘤的动物血钾升高——很可能反映随肿瘤细胞被清除时大量钾的释放。
这对未来癌症护理意味着什么
这项工作提出了“senotoxins”这一概念:受毒液启发并经工程改造的蛋白,通过利用衰老细胞独特的膜与离子处理特性来发挥作用。通过定位改变的脂质并强制产生致命的离子失衡,StnIG 能选择性清除有害的衰老细胞,同时保留大多数健康组织。与化疗合用时,这类 senotoxins 有望清除助长复发与慢性炎症的“僵尸”细胞,使癌症治疗更持久,并可能减轻一些长期副作用。
引用: Moral-Sanz, J., Fernández-Carrasco, I., Ramponi, V. et al. Senotoxins target senescence via lipid binding specificity, ion imbalance and lipidome remodeling. Nat Aging 6, 349–367 (2026). https://doi.org/10.1038/s43587-025-01030-w
关键词: 细胞衰老, 清除衰老细胞药物, 癌症治疗, 来源于毒液的药物, 离子通道