Clear Sky Science · zh
CAR 调整的 PIK3CD 碱基编辑增强了 T 细胞的抗肿瘤效能
重编程抗癌细胞
嵌合抗原受体(CAR)T 细胞疗法已彻底改变了部分血液癌症的治疗,但仍有许多患者复发或无效应。一个关键问题是这些工程化免疫细胞可能会衰竭或无法在体内长期存活。本研究提出了一个简单但有力的问题:与其完全重新设计 CAR,不如微调 T 细胞内部的“接线”,使其更长时间保持强大,同时确保安全,这是否可行?
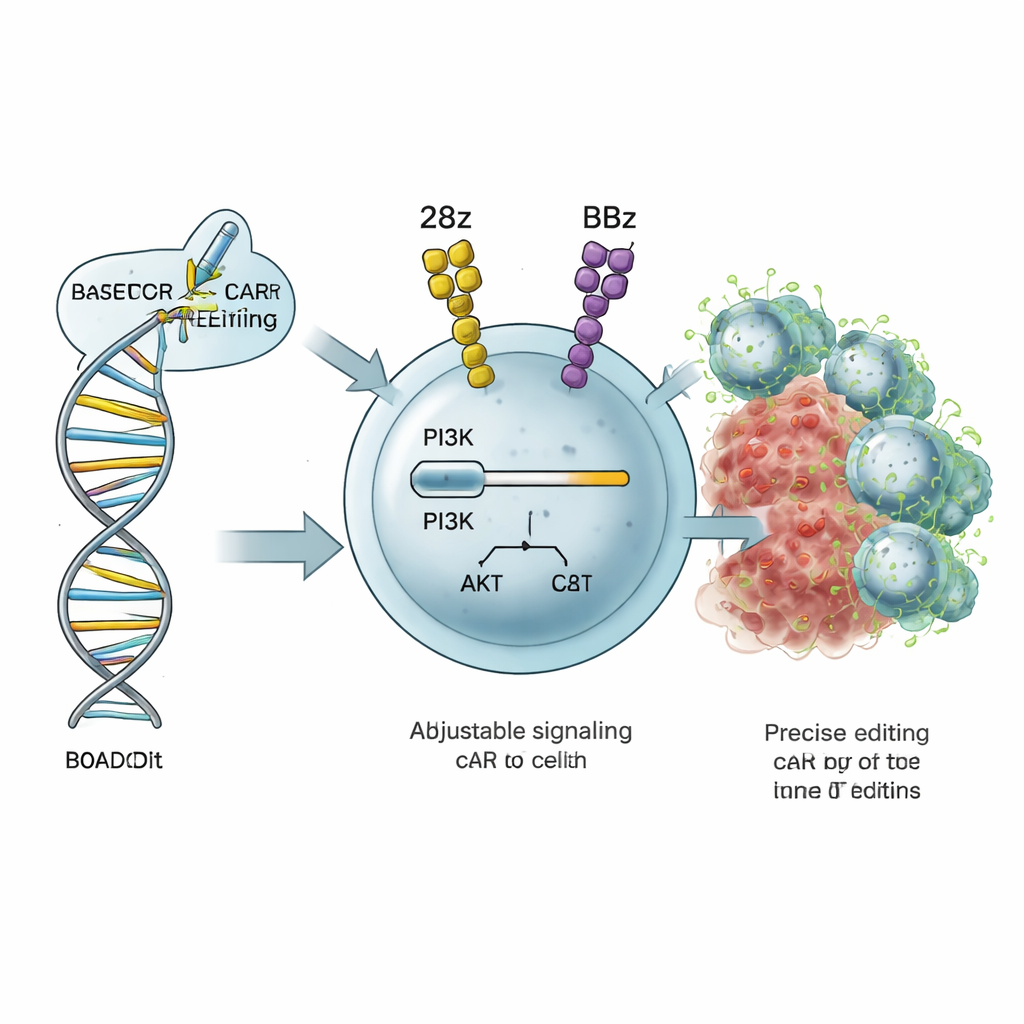
瞄准 T 细胞的音量旋钮
杀伤肿瘤的 T 细胞依赖内部信号回路来决定激活强度、分裂速度以及成为短寿命战斗细胞还是长寿记忆细胞。一个重要回路是 PI3K–AKT 通路,其中由 PIK3CD 基因编码的蛋白 PI3Kδ 像一个用于激活和代谢的音量旋钮。作者开发了一种称为 ROADSTAR 的策略,利用碱基编辑(CRISPR 基因组工程的一种高度精确形式)来改变 PIK3CD 中的单个“字母”。ROADSTAR 不是把通路完全打开或关闭,而是寻找能以最适合特定 CAR 设计的方式,轻微增加或减少信号的微小突变。
发现有益突变
团队构建了包含 34 种不同单字母改变的 PIK3CD 调控区文库,并将其导入已携带两种常见 CAR 设计之一的人类 T 细胞:28z(基于 CD28 分子)和 BBz(基于 4‑1BB)。这些 CAR 在刺激 T 细胞的方式上不同:28z 往往驱动强烈、快速的攻击但伴随衰竭,而 BBz 有利于更好的存活与记忆但攻击性可能较弱。经编辑的 CAR T 细胞通过反复暴露于白血病细胞进行“压力测试”。研究者通过深度测序追踪哪些突变使 CAR T 细胞在数周内胜出并超过未编辑的同类。
两种突变明显脱颖而出。在 BBz CAR T 细胞中,一种称为 E81K 的改变轻微增强了 PI3Kδ 活性,提升了 PI3K–AKT 通路下游的信号。在 28z CAR T 细胞中,另一种改变 L32P 则抑制了 PI3Kδ 活性。结构建模表明,两种编辑都微妙地改变了 PI3Kδ 与其调控伙伴的相互作用,微调信号强度而不是完全开关化。重要的是,对一种 CAR 设计有益的突变并非适用于另一种,这凸显出每种 CAR 架构都需要其特定的内部调谐。
更强、更健康、持续时间更长的 CAR T 细胞
当对这些有前景的编辑逐一测试时,E81K 使 BBz CAR T 细胞在遇到肿瘤细胞时更易被激活、增殖能力更强并在杀伤癌细胞(包括低抗原表达的靶标)方面显著更高效。这些细胞发育为效应记忆 T 细胞,兼具强大杀伤力与持久存活能力。在白血病和转移性神经母细胞瘤的小鼠模型中,E81K 编辑的 BBz CAR T 细胞比未编辑的 BBz 细胞更彻底且更持久地控制肿瘤,甚至能够抵御多轮肿瘤再挑战。详细的单细胞转录组和代谢谱分析显示,E81K 细胞具有增强的线粒体功能、更高的备用呼吸和糖酵解能力以及更少的衰竭迹象——本质上,它们更有能量且更具韧性。
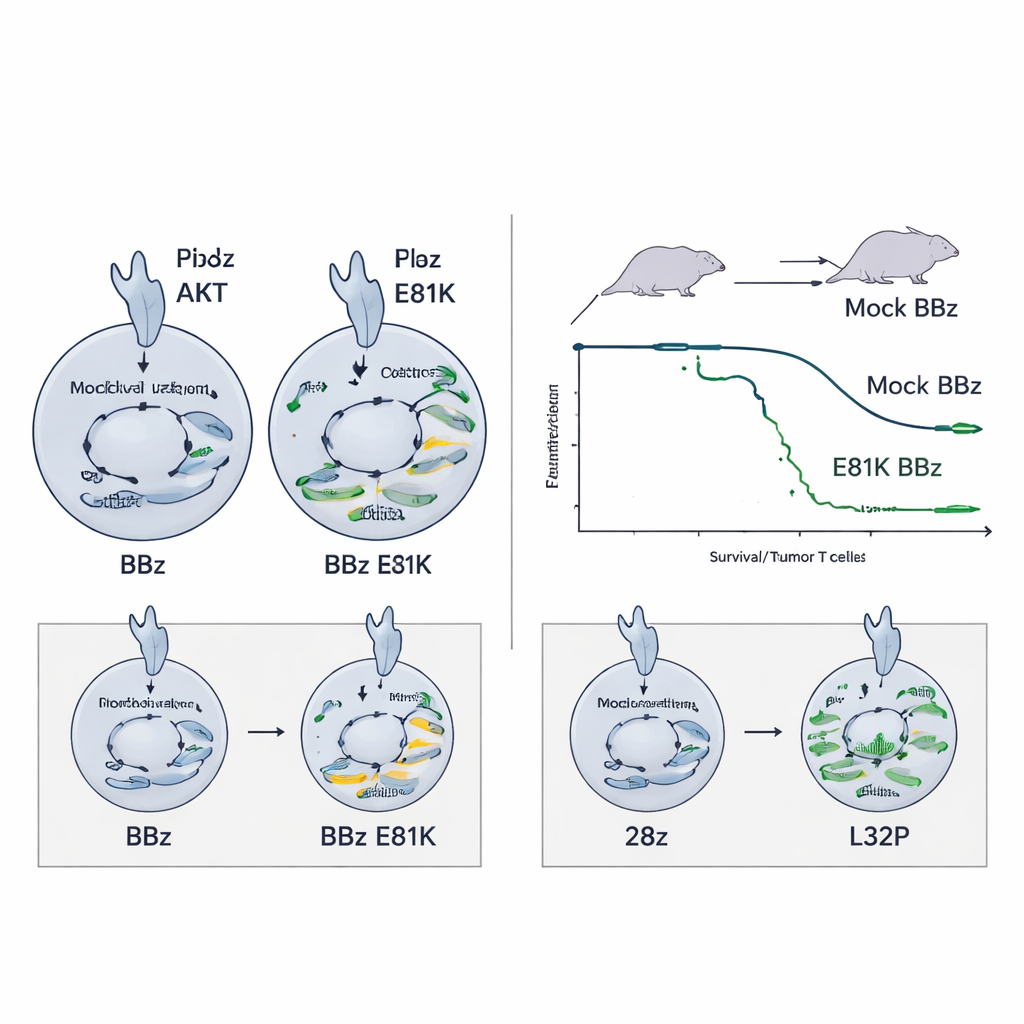
防止高度活跃 CAR 的衰竭
相同的 E81K 提升对已具有强烈信号的 28z CAR T 细胞并不有益——甚至可能有害:额外的 PI3K 活性提高了衰竭标志物而未改善功能。在这种情形下,L32P 突变更为合适:通过适度降低 PI3K–AKT 信号,L32P 编辑的 28z CAR T 细胞表现出较低的基线激活但保持高杀伤能力,并随着时间推移显示出更好的增殖。它们还维持了更不分化的、类记忆的状态,包括被认为支撑长期反应的干细胞样记忆池。在一个苛刻的神经母细胞瘤模型中,L32P 修饰的 28z CAR T 细胞较其未编辑同类改善了生存率。
安全性与未来前景
永久改变免疫信号的核心担忧是失控生长或继发性癌症的风险。因此,作者进行了广泛的安全性检查。E81K 编辑的 BBz CAR T 细胞在培养中没有异常增生的表现,在小鼠体内也未引起器官损伤或炎症危机,注入数月后未见淋巴瘤或组织侵袭的迹象。临床数据库同样显示这些特定的 PIK3CD 突变在 T 细胞白血病中并不富集。总体而言,该研究表明,精心选择的单字母基因组编辑可以作为调节 T 细胞行为的精密旋钮——增强抗肿瘤能力和持久性,同时尊重每种 CAR 的独特生物学。ROADSTAR 方法有望帮助打造新一代更有效且更可靠的 CAR T 疗法,适用于血液癌症并可能扩展到实体瘤。
引用: Bucher, P., Brückner, N., Kortendieck, J. et al. CAR-adapted PIK3CD base editing enhances T cell anti-tumor potency. Nat Cancer 7, 368–383 (2026). https://doi.org/10.1038/s43018-025-01099-7
关键词: CAR T 细胞, PI3K 信号传导, 碱基编辑, 癌症免疫疗法, T 细胞代谢