Clear Sky Science · zh
在类人脑干类器官中原位诱发H3.3K27M改变的弥漫性中线胶质瘤以剖析GD2 CAR T细胞功能
这项儿童脑癌研究的重要性
弥漫性中线胶质瘤是儿童期最致命的脑癌之一,常在脑干发生,危及非常小的儿童,而有效的治疗选择几乎不存在。由于肿瘤位于脑深处且很少进行手术,研究者可用的肿瘤组织有限,也难以安全地测试新疗法。本研究构建了一个逼真的“培养皿中微型脑干”模型,并用它在数周内观察一种有前景的免疫疗法——识别GD2的CAR T细胞——的行为,及其有时失效的原因。
在实验室中构建微型脑干
研究团队从人类干细胞出发,按步骤引导其生长为三维脑类器官,类似通常发生此类肿瘤的脑干区域——桥脑。通过精确控制生长信号的时序,他们制备出富含该区域常见支持细胞(即神经胶质细胞)的类器官。详细的基因组分析显示,细胞类型及其成熟度遵循与早期人类脑发育相似的模式,尤其是桥脑及相邻延髓的胶质谱系。这表明这些类器官可作为研究该癌症起始与生长的现实背景。
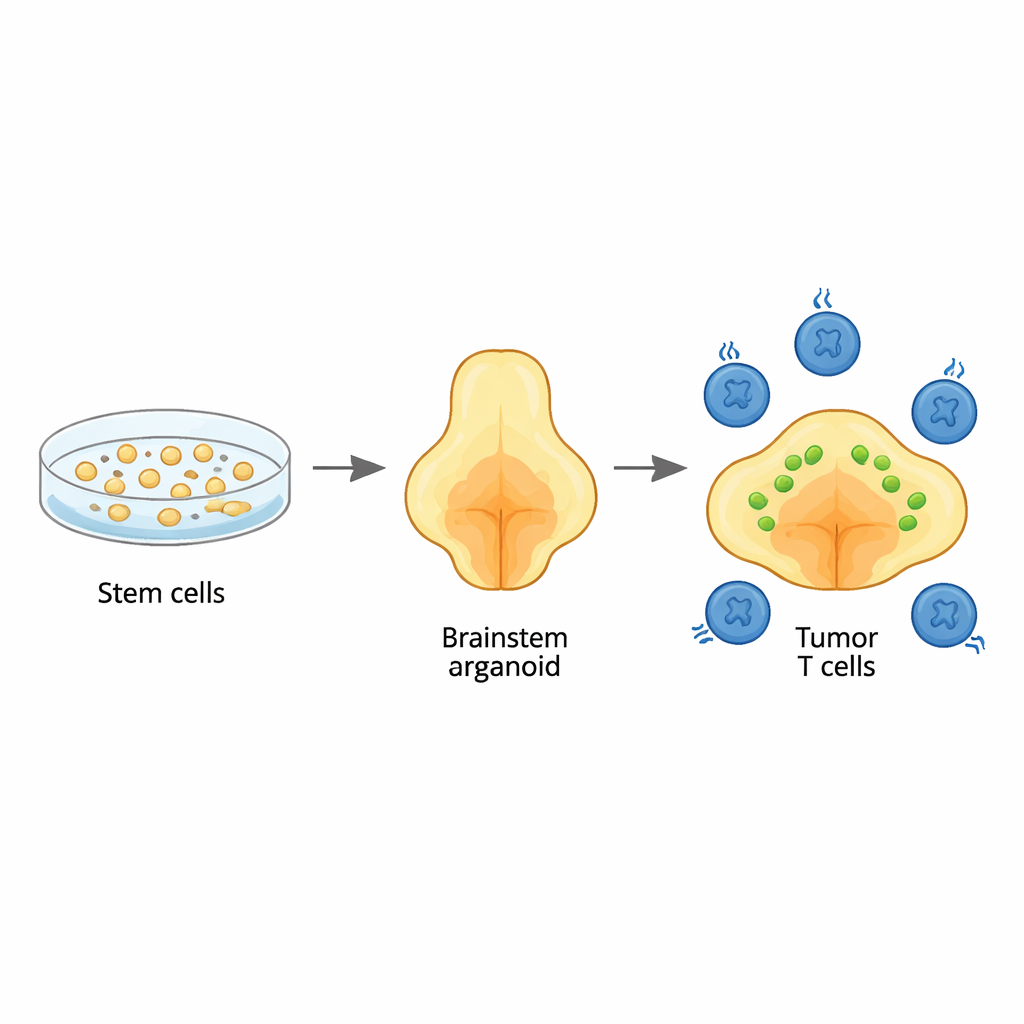
在类器官内再现儿童肿瘤
为模拟弥漫性中线胶质瘤,研究人员在早期类器官中引入了三处关键基因改变:组蛋白蛋白质的标志性突变(H3.3K27M)、肿瘤抑制基因TP53的丧失,以及生长受体PDGFRA的激活性改变。在非常早的发育阶段引入这些变异后,部分类胶质样细胞转化为肿瘤细胞。所形成的肿瘤在类器官内弥漫扩散,类似儿童脑干中的表现,并携带与患者肿瘤相同的广泛DNA和RNA特征。单细胞测序揭示了多种癌细胞状态的混合,包括与实际儿科肿瘤中发现的未成熟、具有桥脑特征的胶质细胞相匹配的细胞类型,强调该模型忠实再现了人类疾病。
观察免疫疗法随时间作战——并疲惫
在这一肿瘤-脑干模型建立后,团队加入了GD2 CAR T细胞——对患者T细胞进行工程改造以识别肿瘤细胞表面的GD2分子——并在最长一个月内追踪肿瘤体积和T细胞行为。一些类器官出现显著肿瘤缩小,另一些仅得到部分控制,反映了临床试验中的混合结果。对超过2万枚暴露于肿瘤的CAR T细胞进行单细胞RNA测序,揭示了出人意料的T细胞状态多样性。一部分细胞表现出高度细胞毒性“杀手”特征,另一部分被激活但未完全致死,而另有一类呈现疲惫表型,癌杀基因表达受抑且抑制性“刹车”分子高表达。疲惫的细胞与慢性感染和人类肿瘤中见到的衰竭T细胞非常相似,表明类器官系统能捕捉到由持续与癌细胞接触驱动的临床相关T细胞疲劳。
发现强效但短命的T细胞
进一步挖掘中,研究人员鉴定出一类以表面蛋白NCAM1标记的CAR T细胞,这类细胞在短期内尤其有效。当将这些NCAM1阳性细胞分离并单独使用时,它们在初期比NCAM1阴性同类更强力地控制肿瘤。然而,这些细胞也更容易陷入疲惫并更快减少,导致随时间控制能力减弱。这种即时效力与持久性的权衡有助解释CAR T疗法为何能产生戏剧性但短暂的应答,并提示通过预先选择或重塑T细胞亚群可优化治疗的持久性。
脑内免疫细胞如何削弱疗法
在真实的大脑中,肿瘤周围不仅有神经元和胶质细胞,还有作为脑内常驻免疫细胞的小胶质细胞。为了捕捉这一复杂层次,科学家将源自干细胞的小胶质细胞加入其类器官。这些细胞发生成熟,呈现出与弥漫性中线胶质瘤中发现的小胶质细胞相匹配的形态和基因表达模式,并产生与免疫抑制环境相关的分子。当在含有小胶质细胞的带瘤类器官中加入CAR T细胞时,T细胞更倾向于进入疲惫和低效应状态,肿瘤控制变差。同时,与治疗副作用相关的炎性因子(如IL-6)上升,表明该模型也可用于研究CAR T相关毒性。
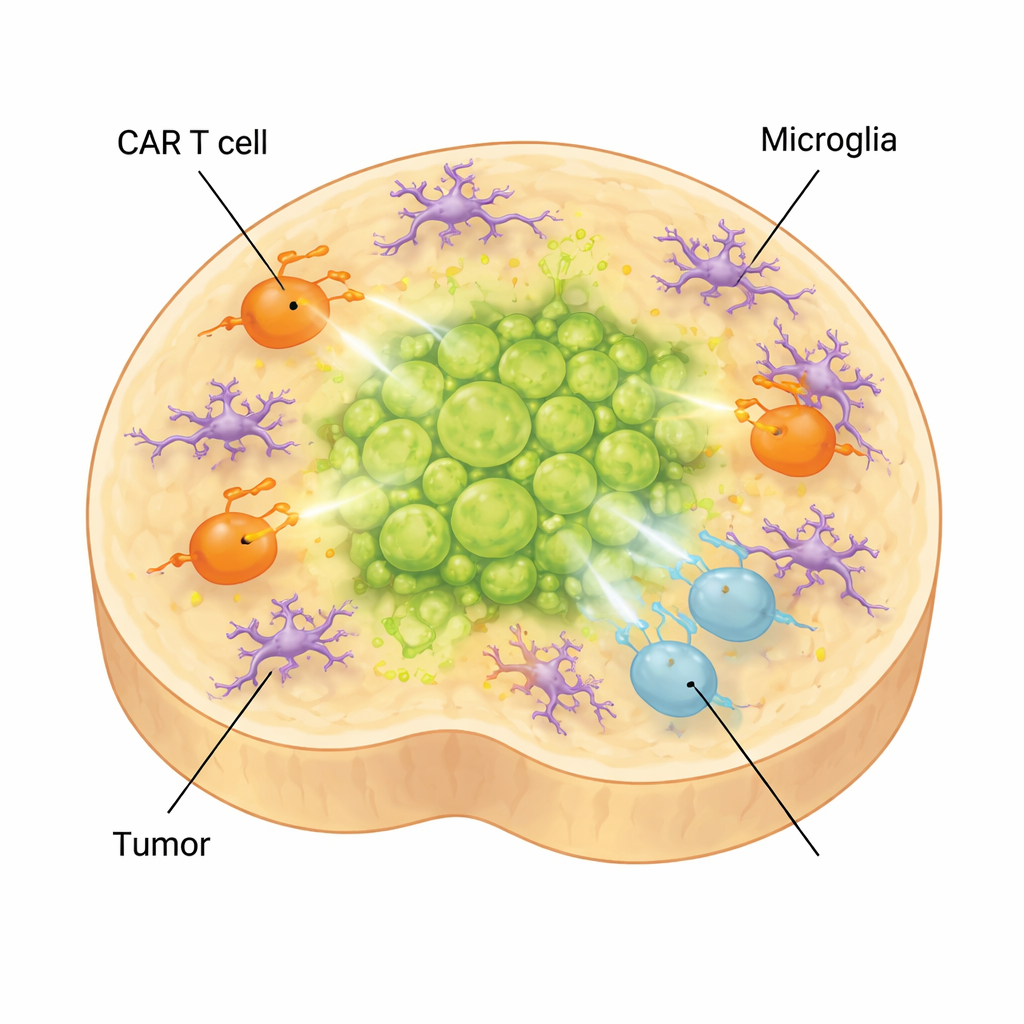
这对患儿意味着什么
对面对弥漫性中线胶质瘤的家庭而言,这项工作尚不能直接提供新疗法的治愈方案,但它提供了一个强有力的测试平台,加速迈向疗法的步伐。通过在培养皿中重建儿童的脑干环境和肿瘤,科学家现在可以实时观察不同肿瘤细胞、CAR T细胞类型和小胶质细胞在数周内如何相互作用。这使他们能够确定哪些工程化T细胞最为有效、它们何时以及如何耗竭,以及脑内常驻免疫细胞如何破坏其效能。最终,这类类器官模型可能为个体患者实现个性化,并在临床使用之前用于微调免疫疗法,从而提高未来CAR T细胞治疗对儿童既更安全又更有效的几率。
引用: Bessler, N., Wezenaar, A.K.L., Ariese, H.C.R. et al. De novo H3.3K27M-altered diffuse midline glioma in human brainstem organoids to dissect GD2 CAR T cell function. Nat Cancer 7, 316–333 (2026). https://doi.org/10.1038/s43018-025-01084-0
关键词: 弥漫性中线胶质瘤, 脑类器官, CAR T细胞, 儿童脑癌, 小胶质细胞