Clear Sky Science · zh
胞质DHODH的异位表达将从头嘧啶生物合成与线粒体电子传递解耦
为何打破细胞中一个隐蔽联系很重要
你体内的每个细胞都必须不断复制和修复DNA,这一过程需要持续供应称为嘧啶的化学“字母”。在大多数动物中,合成这些字母与线粒体——细胞的能量站——利用氧气燃烧燃料的方式紧密相连。这种耦合意味着当线粒体呼吸受损时,DNA的构件就会短缺,细胞难以生长。这里总结的研究表明,将面包酵母的单个基因借入哺乳动物细胞可以清晰地将这两种过程解耦。这一基因改造使哺乳动物细胞即便在线粒体受损时也能继续合成DNA字母,为探究并可能在未来治疗由能量代谢故障驱动的疾病开辟了新途径。
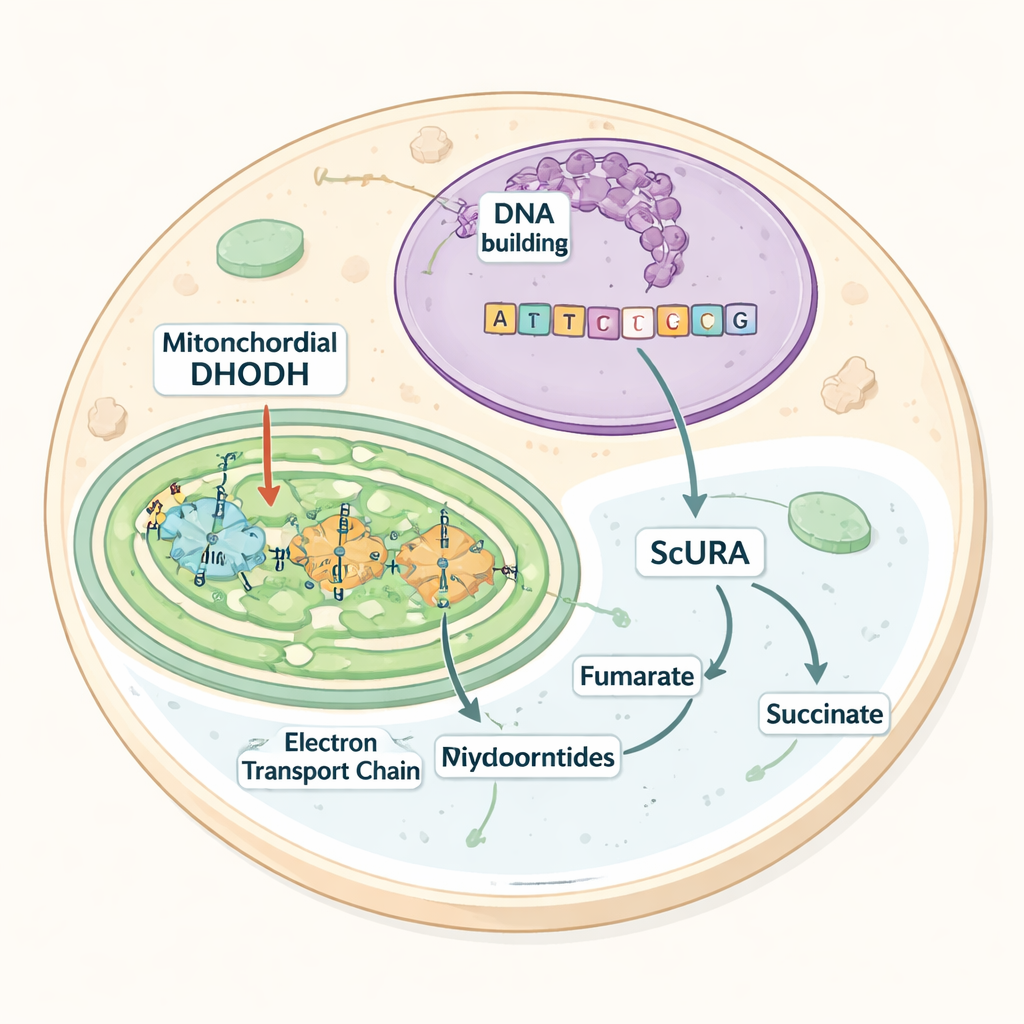
从酵母借来的工具
该研究聚焦于一种名为二氢乳清酸脱氢酶(DHODH)的酶,它在嘧啶合成中执行关键步骤。在哺乳动物中,DHODH位于线粒体内膜,并将电子传递给为呼吸链供能的载体分子。如果这条电子流被阻断——例如被药物抑制或由于遗传缺陷——DHODH会停滞,嘧啶合成中断,细胞便依赖于食物或外源补充的尿苷(一种现成的构件)。许多能在无氧条件下生存的微生物通过使用悬浮在细胞质中并使用不同电子受体的替代DHODH版本来避免这一瓶颈。作者探问是否可以在哺乳动物细胞中安装这样一个与氧无关的途径。
重接DNA字母的合成线路
研究者将酵母Saccharomyces cerevisiae的URA1基因引入人类细胞。URA1编码一种胞质酶,称为ScURA,它执行与线粒体DHODH相同的化学反应,但将电子传递给称为富马酸的分子,而不是传给线粒体载体。生化测试显示ScURA在胞质中形成具有活性的二聚体,并赋予细胞一种新的、对药物具有抗性的DHODH活性。在正常条件下,表达ScURA并未扰乱线粒体结构、呼吸或生长,这表明它更像是一条备用通路,而非额外负担。
能够无视线粒体障碍的细胞
为了检验这一备用途径是否可以替代天然系统,研究组化学阻断了DHODH本身或线粒体电子传递链——这些处理通常会阻止细胞分裂,除非提供尿苷。表达ScURA的细胞在没有任何外部补给的情况下仍然持续增殖,即便在强烈抑制呼吸复合体III或基因敲除内源性DHODH后也是如此。来自标记谷氨酰胺的氮和碳的详细示踪显示,表达ScURA的细胞在这些阻断下仍保持嘧啶核苷酸的合成。代谢物测量表明,ScURA细胞并未积累有毒前体,而是将电子引流到富马酸,生成琥珀酸,并细微地重塑三羧酸(TCA)循环,以支持胞质与线粒体之间的富马酸–琥珀酸穿梭。
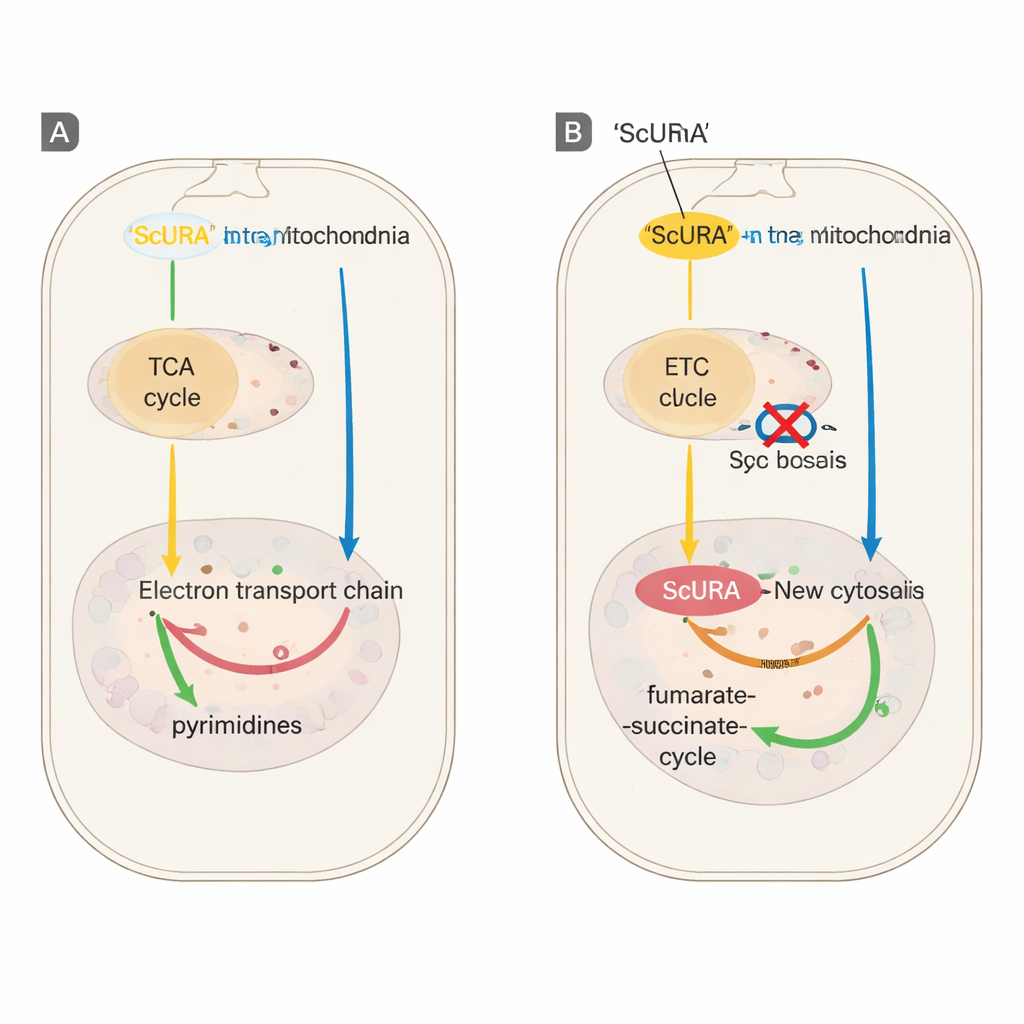
拯救受损能量工厂的细胞
作者随后在线粒体疾病的细胞模型中测试了ScURA。缺乏线粒体DNA或携带使呼吸复合体III或IV失能突变的细胞,通常依赖外源尿苷才能生长。一旦被改造表达ScURA,这些不同类型的突变细胞便能在没有尿苷的情况下增殖,尽管它们仍需要丙酮酸,表明仍存在对部分线粒体活性的需求。在基因表达水平上,ScURA还防止了通常随慢性电子传递抑制而发生的核糖体蛋白基因关闭——通过保持足够的嘧啶供给以维持RNA的合成。
对健康和疾病的意义
通过将嘧啶合成与线粒体呼吸清晰地分离,ScURA为研究者提供了一个强有力的新工具:在许多情境下,他们现在可以探问某一缺陷或药物效应究竟是源于能量产生丧失,还是源于DNA和RNA前体的短缺。从长远看,类似策略可能补充现有的线粒体疾病基因疗法,或帮助解释为何某些肿瘤如此依赖恢复其线粒体功能。尽管要将一种酵母酶转化为人类治疗需慎之又慎,这项研究证明,一个精心选择的单个基因就能改写进化长期交织在一起的基本代谢联系。
引用: Curtabbi, A., Jaroszewicz, S.N., Sanz-Cortés, R. et al. Ectopic expression of cytosolic DHODH uncouples de novo pyrimidine biosynthesis from mitochondrial electron transport. Nat Metab 8, 454–466 (2026). https://doi.org/10.1038/s42255-026-01454-7
关键词: 嘧啶代谢, 线粒体功能, 电子传递链, 代谢重塑, 线粒体疾病