Clear Sky Science · zh
进食调控的糖原代谢驱动肝脏节律性蛋白质分泌
肝脏的每日节律为何重要
我们大多数人关注吃什么,却很少注意肝脏何时默默地将重要蛋白质打包并释放到血液中。这项研究显示,肝脏的蛋白质“发货时间表”并非恒定:它遵循一种与进食时间和肝脏对储存糖(即糖原)的利用密切相关的日节律。理解这一计时系统有助于解释为何进餐时间、肥胖以及某些罕见的遗传疾病会扰乱激素、凝血因子和许多维持身体平衡的血液蛋白质的节律。
进餐为血液蛋白定下节拍
研究人员首先在受控的两种进食模式下,跟踪了健康男性在24小时内数百种血液蛋白的变化。在一种模式中,志愿者按常规进餐;在另一种模式中,相同的总热量在清醒时间内均匀分配。按常规进餐时,许多血液蛋白呈现明显的日间波动,常在清晨和下午晚些时候达到高峰。这些蛋白包括代谢激素、凝血因子、免疫蛋白以及主要由肝脏合成的转运蛋白。相反,当食物被缓慢、持续地摄入时,大多数这些节律被抹平。小鼠的类似实验(食物要么全天可得,要么仅在特定的昼夜窗口内提供)显示,改变进食时间能强烈重塑血液中哪些蛋白呈节律性及其高峰时相。
肝脏的分泌通路受时钟调控
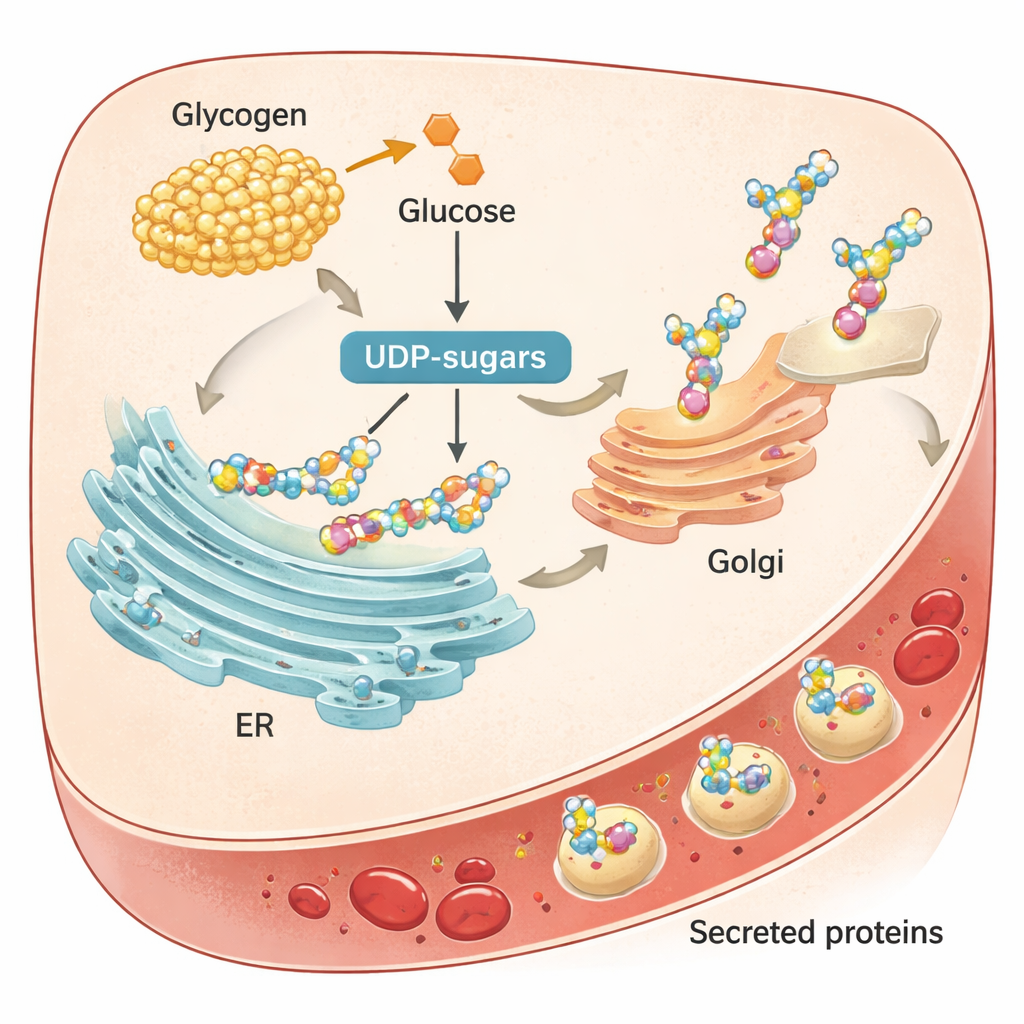
为弄清这些模式如何产生,研究团队深入观察肝脏。他们发现参与经典“分泌通路”的蛋白——新合成蛋白进入内质网(ER)、在高尔基体被修饰并随后释放——也在一天内呈升降变化。这个通路并非恒定的传送带,而是被昼夜时钟调谐。大多数有节律的血液蛋白携带将其标记为该通路目标的分子“信号肽”,在小鼠肝切片中阻断ER–高尔基体运输会显著减少蛋白质释放。相比之下,细胞损伤和蛋白质降解的标记并未表现出强烈的日变化,表明观测到的血液节律主要由分泌而非破坏驱动。
糖原:为蛋白质包装供能的储备糖
作者接着将这些时间效应与肝脏处理糖原的方式联系起来,糖原是肝脏的主要碳水化合物储备。进餐后,肝脏合成糖原;禁食时,糖原被分解,这一过程称为糖原分解(glycogenolysis)。分解产物进入“UDP-糖”路径,UDP-糖是用于将糖链附加到蛋白上的活化糖单元,这种修饰称为糖基化。在小鼠中,UDP-糖水平随昼夜强烈振荡,与合成和分解糖原的酶的活性同步。当团队用药物抑制关键的肝糖原分解酶PYGL时,糖原堆积,禁食期间血糖下降,UDP-糖供应减少。这导致肝脏蛋白的糖基化减少、内质网出现应激迹象,以及若干重要蛋白质分泌到血液中的减少。
应激信号与疾病关联
干扰糖原分解不仅仅减慢了蛋白输出;它还触发了细胞的质量控制报警系统。用阻断PYGL的药物处理的肝细胞激活了未折叠蛋白反应(UPR),这是一组内质网应激通路,能增强蛋白降解并选择性地改变哪些蛋白被分泌。在肥胖小鼠中,糖原处理自然改变,正常的糖原日波动被削弱,呈节律的血液蛋白数量减少。对正常小鼠实施能有效降低热量的限时进食也产生了类似影响。最后,在一项大规模的人类遗传研究中,携带与糖原贮积病或先天性糖基化障碍相关基因变体的人表现出许多血液蛋白水平的改变,进一步强化了糖原代谢、蛋白糖基化与分泌之间的联系。
这对日常健康意味着什么
对非专业读者而言,结论是肝脏有一个定时的血液蛋白出口系统,利用储存的糖作为为正确包装和释放提供动力的燃料。当进食模式、内部生物钟或糖原处理相关基因被扰乱时,这一时刻表会紊乱,改变血液中激素、凝血因子和免疫蛋白的水平。这些变化可能有助于解释为何进餐时间、肥胖和某些罕见代谢疾病与广泛的健康问题相关。研究表明,不仅我们吃什么,何时进食也能影响肝脏的日常“发货”节律——医生在解读血液检测结果时,或许也需考虑一天中的时间和进食安排。
引用: Weger, M., Mauvoisin, D., Hoyle, D. et al. Feeding-regulated glycogen metabolism drives rhythmic liver protein secretion. Nat Metab 8, 327–349 (2026). https://doi.org/10.1038/s42255-026-01453-8
关键词: 昼夜节律, 肝糖原, 蛋白质分泌, 进餐时间, 代谢