Clear Sky Science · zh
解开全球人群与疾病相关组织中致2型糖尿病的分子机制
为何了解糖尿病根源很重要
2型糖尿病影响着全球数以亿计的人,但我们对哪些体内分子开关是真正引发疾病而非仅仅伴随出现仍知之甚少。这项研究深入DNA并考察多个器官,明确哪些基因和蛋白质实际上会推动血糖走向糖尿病,哪些则起到保护作用。通过纳入多样化血统的人群并检视若干关键组织,研究人员将我们推向更精确的预防策略和治疗方法,使其对更多人群有效,而非仅限于欧洲血统的人。
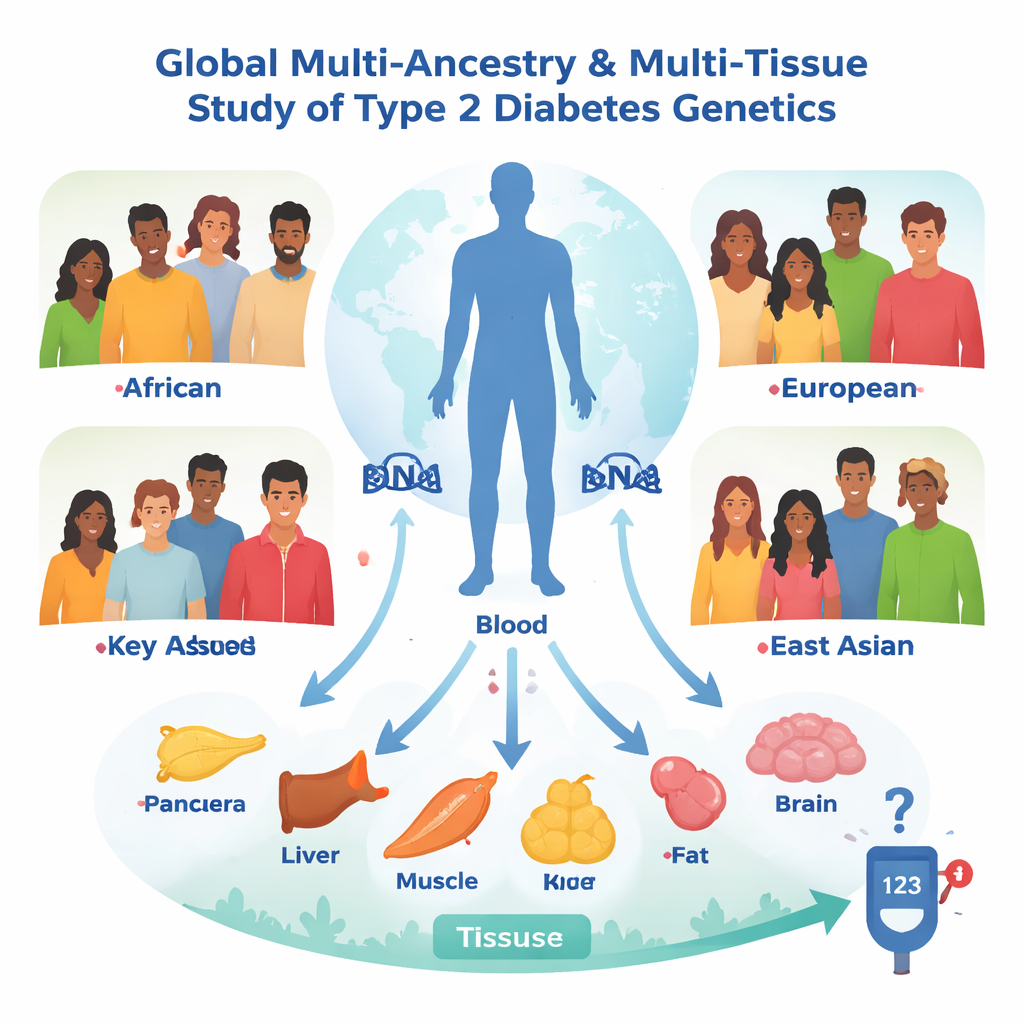
在全球与体内多方位观察
团队起始于2.5万多人(注意:原文为超过250万人)汇集的遗传数据,由2型糖尿病全球基因组倡议提供。他们没有仅仅问哪些DNA变体与糖尿病有关,而是提出了更有力的问题:哪些变体会改变体内特定基因或蛋白的表达,这些改变又是否进而改变糖尿病风险?为此,他们使用了一种称为孟德尔随机化的统计方法,将天然存在的遗传差异视为一种内生的随机对照试验。他们分析了来自欧洲、非洲、混杂美洲和东亚四个血统群体中超过2万项基因活性测量和1600多种血液蛋白,并在与血糖调控密切相关的七种组织中重复这些分析,包括胰腺、产生胰岛素的胰岛、肝脏、肌肉和不同的脂肪库。
发现能提高或降低风险的分子杠杆
通过追溯这些遗传通路,研究者鉴定出335个基因和46种血液蛋白——其基因预测水平对2型糖尿病风险具有因果影响,并在独立队列中验证了其中许多发现。他们发现的一些分子杠杆已为人所知,例如参与胰岛细胞胰岛素释放的基因MTNR1B,以及影响胰腺和脂肪细胞凋亡的BAK1。也有一些是新近或较少被重视的参与者,包括与脂肪组织发育和胰岛素抵抗相关的蛋白CPXM1,以及参与线粒体功能的基因HIBCH。总体上,他们编目出923个基因和46种蛋白,这些基因或蛋白在至少一种组织中活性发生变化时,会改变患糖尿病的概率。
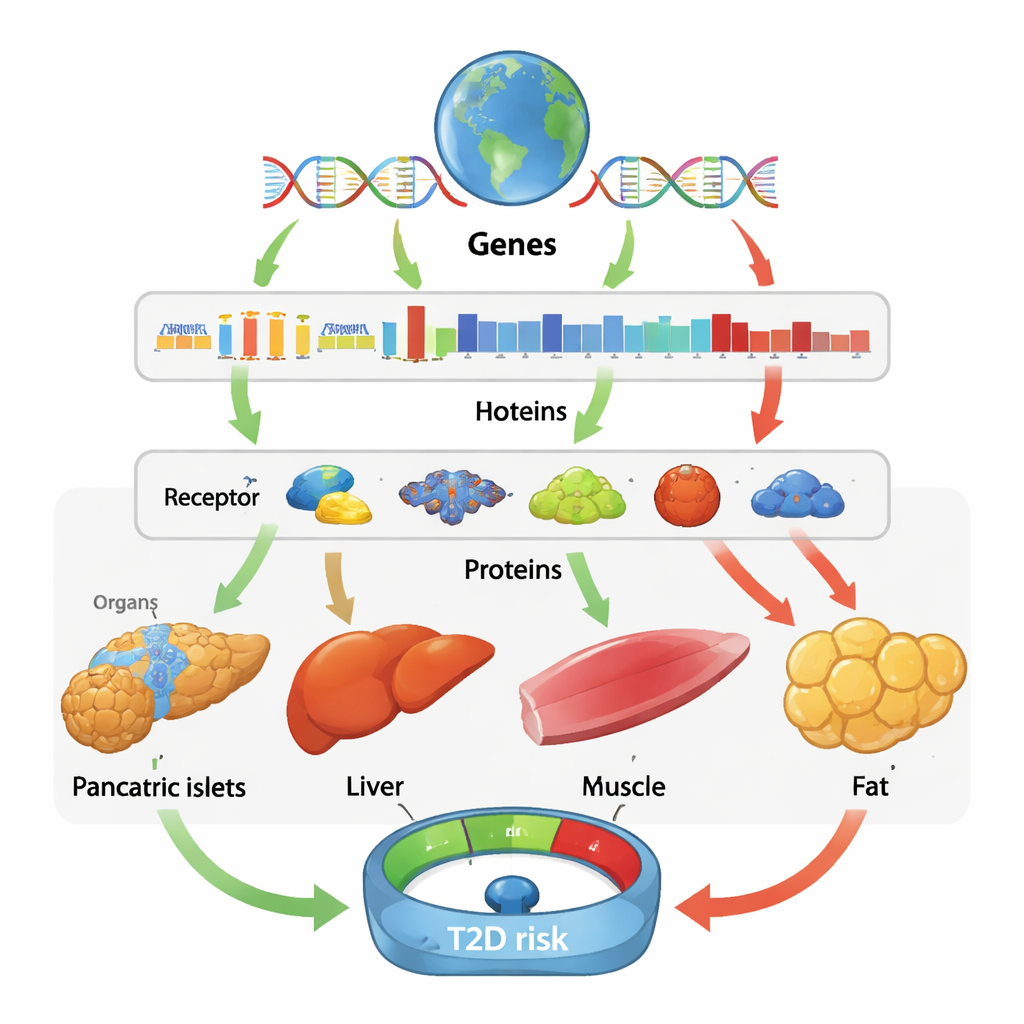
相同基因在不同组织和人群中讲不同故事
一个显著的教训是基因效应常常高度依赖组织。例如,胰腺和胰岛中更高的BAK1活性似乎会增加糖尿病风险,可能通过促进产生胰岛素的细胞丧失,而在脂肪和肌肉中更高的BAK1则似乎具有保护作用。HIBCH也显示出类似的混合模式:在某些组织中其活性增加会降低糖尿病风险,而在另一些组织中则会提高风险。这些发现表明,仅观察血液可能会错过器官内部发生的重要生物学过程,同一种分子在一种组织中可能有益而在另一种组织中有害。相比之下,当团队比较不同血统的结果时,效应大小差异相对较小,这表明许多潜在的因果机制在全球范围内是共享的,尽管某些信号——例如在东亚或非洲群体中特有的保护性或风险蛋白——仅通过非欧洲数据才能检测到。
将新发现与已知糖尿病生物学相连
为了检验他们的方法是否具有生物学意义,作者将其因果基因与来自人类研究和小鼠实验的糖尿病相关基因的策划列表进行了交叉比对。具有最强先验证据的基因在其分析中显示出因果效应的可能性远高于随机选择的基因。此外,这些因果效应出现的组织与已知的疾病机制相吻合:与β细胞功能衰竭相关的基因在胰岛中最重要,而与代谢综合征相关的基因则在内脏(深层腹部)脂肪中表现出最强效应。这种一致性支持了该统计流程确实在定位机制,而非仅发现相关性。
这对未来治疗与预防的意义
对非专业读者来说,关键结论是这项工作把冗长、抽象的DNA变体列表转化为更清晰的地图,指出实际驱动2型糖尿病的特定基因、蛋白和器官。通过区分因果与结果并揭示相同分子在不同组织中的相反作用,它为药物开发者提供了更精确的靶点,并警示单一方案可能带来的反效果。更重要的是,通过有意识地纳入多样化人群,该研究有助于确保未来基于这些见解开发的药物或风险评分更有可能在广泛人群中有效,而不仅限于欧洲血统的人群。
引用: Bocher, O., Arruda, A.L., Yoshiji, S. et al. Unravelling the molecular mechanisms causal to type 2 diabetes across global populations and disease-relevant tissues. Nat Metab 8, 506–520 (2026). https://doi.org/10.1038/s42255-025-01444-1
关键词: 2型糖尿病, 遗传机制, 多血统基因组学, 组织特异性基因表达, 因果推断