Clear Sky Science · zh
层粘蛋白A/C调控的半胱氨酸硫代代谢通量通过表观基因组重编程调节干细胞命运
细胞“骨架”如何与代谢对话
为什么有些细胞保持年轻且具有多能性,而另一些细胞则衰老或锁定为错误的身份?这项研究揭示了细胞内部一段出人意料的对话:塑造DNA的核“支架”与含硫营养物半胱氨酸之间的相互作用。研究表明,这种对话会引导干细胞走向健康的命运或过早衰老——暗示细胞“吃什么”以及如何代谢这些营养物,有朝一日可能被调控以预防某些遗传疾病,甚至延缓部分衰老过程。
核壳的隐秘作用
在每个细胞深处,DNA被压靠在称为核层(nuclear lamina)的蛋白网格上,部分由称为层粘蛋白A和C(lamin A/C)的蛋白构成。这些层粘蛋白不仅赋予细胞核形状,它们还参与决定哪些基因被封闭、哪些保持可及。作者在小鼠胚胎干细胞的最可塑(或称“朴素”)状态下研究,发现层粘蛋白A/C通常抑制两种代谢酶CBS和CTH,这两者参与半胱氨酸的合成与分解。当层粘蛋白A/C存在且功能正常时,这些酶受控,半胱氨酸的代谢保持较低水平,从而维持干细胞稳定、年轻的状态。 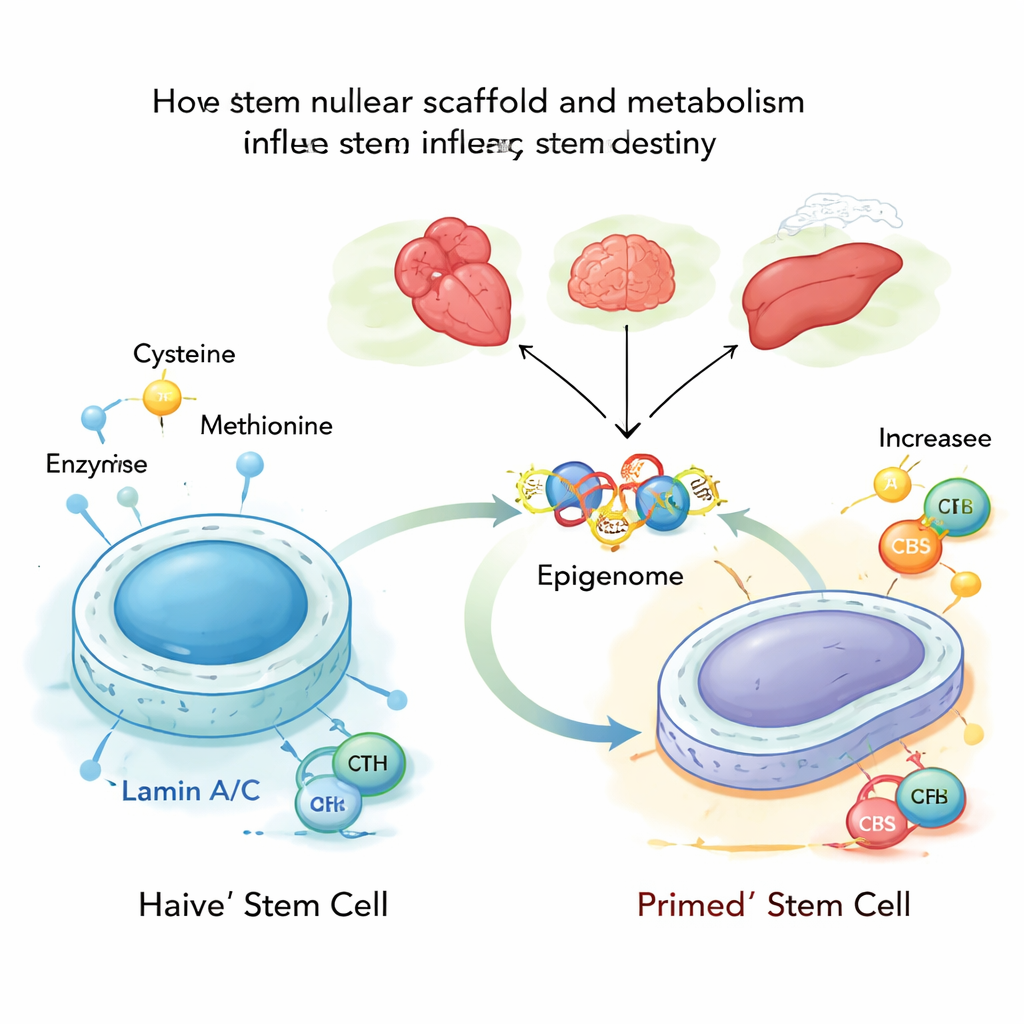
当结构失效,代谢加速
接着,研究者删除了层粘蛋白A/C或引入一种模拟人类早衰疾病Hutchinson–Gilford早衰综合征的致病突变。在缺乏正常层粘蛋白A/C的情况下,CBS和CTH基因变得更易接近并被转录因子SP1更强烈结合,从而被激活。该改变促使更多半胱氨酸流入一条以乙酰辅酶A(acetyl‑CoA)为终产物的代谢途径,乙酰‑CoA携带的乙酰基可用于松开DNA的包装。当越来越多的半胱氨酸被引入乙酰‑CoA路径时,乙酰基优先添加到组蛋白特定位点——尤其是组蛋白H3的K9和K27这两个位置——使邻近基因更易被激活。
从化学修饰到细胞命运抉择
这些组蛋白“标记”的变化就像对细胞控制面板的整体重新调谐。在朴素干细胞中,提高CBS和CTH的活性,或仅仅补给更多半胱氨酸,会推动细胞向更成熟的“准备态(primed)”转变,接近形成真实组织的状态。参与心脏发育和其他谱系的基因变得更活跃,DNA的三维折叠也发生改变以偏向这些程序。相反,下调CBS和CTH或限制半胱氨酸供应,即便在核层受损时也有助于恢复更朴素、更年轻的身份。在胚胎模型中,这种代谢误连线导致三胚层(器官早期构建模块)形成偏倚——除非重新平衡CBS和CTH,否则会异常偏向心肌细胞。 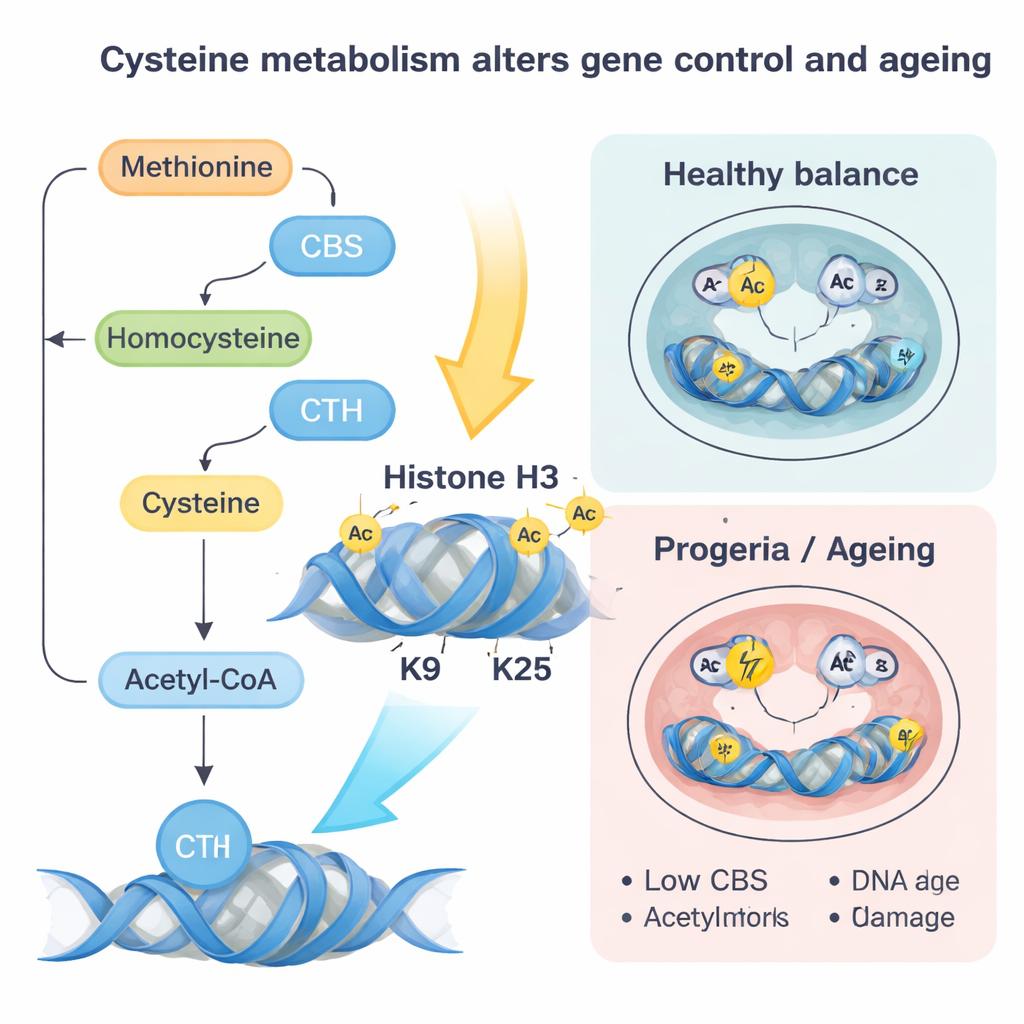
代谢、DNA修饰与早衰
类似早衰的层粘蛋白突变讲述了互补的故事。在这种情况下,CBS和CTH水平下降,来自该路径的半胱氨酸通量和乙酰‑CoA减少。与此同时,半胱氨酸的前体同型半胱氨酸被重新导入甲硫氨酸循环,导致SAM(一种通用的甲基供体)水平上升。这会促成额外的甲基标记,尤其是由酶SUV39H1置加的H3K9me3标记,它会致密染色质并与受损的DNA修复相关。作者展示了温和恢复CBS或限制甲硫氨酸可降低SAM,减少这些抑制性甲基标记,改善DNA修复,降低氧化应激和衰老标志,并部分拯救心肌细胞分化。在正常衰老的小鼠心脏以及来自年长人群和早衰患者的人类成纤维细胞中,也观察到类似的CBS下降和抑制性修饰上升,提示该回路在自然衰老中亦在起作用。
对健康与衰老的意义
对非专业读者而言,结论是:细胞的结构框架与其代谢密切相连——当由层粘蛋白A/C构成的核壳被扰动时,半胱氨酸的利用方式发生变化,进而改写包裹DNA的蛋白上的化学标记。这些标记决定了干细胞在构建机体时哪些基因被开启,并影响细胞在一生中修复损伤的能力。通过精细调节如CBS和CTH之类的酶,或调整甲硫氨酸与半胱氨酸等营养物的供应,可能有望纠正一些层粘蛋白相关疾病中错误的修饰书写,并或许缓解部分早衰或正常衰老的表现。
引用: Wang, Y., Shi, H., Wittig, J. et al. Lamin A/C-regulated cysteine catabolic flux modulates stem cell fate through epigenome reprogramming. Nat Metab 8, 431–453 (2026). https://doi.org/10.1038/s42255-025-01443-2
关键词: 干细胞, 核膜, 半胱氨酸代谢, 表观遗传学, 衰老