Clear Sky Science · zh
结合位点深度调节光可逆配体在5-HT2A受体上的效力
为可切换的脑内药物照亮方向
想象一种可以用一束光开关的药物,精确操控大脑受体并减少副作用。本研究正是探索这样一个针对关键血清素受体(与情绪、知觉及迷幻药相关)的想法。研究者调查了为什么两种几乎相同的光敏分子表现截然不同——一种近乎理想的开/关开关,另一种却顽固地无法完全关闭。他们的答案归结为一个出人意料的简单因素:分子在受体内所处的深度。
脑内的光驱动药物
光激活药物,也称为光药理学工具,设计为光束能够使分子的部分在两种形态之间转换,例如弯曲与伸直两种构象。这些构象会改变药物与靶点的结合强度。本研究的靶点是人类5-HT2A受体,一种位于脑细胞膜上的蛋白,响应血清素并且在抗精神病与迷幻效应中起核心作用。研究的分子是N,N-二甲基色胺(DMT)的衍生物,接入了一个光敏的偶氮苯单元。两种版本仅在环上一个微小的甲氧基基团位置不同——分别位于“对位(para)”或“间位(meta)”——但在光照下的生物学行为却截然不同。
两种几乎相同的分子,截然不同的开关行为
在细胞实验中,对位版本(称为化合物1)行为近似数字开关。在黑暗中,它的“反式(trans)”构象几乎不激活受体,甚至略微阻断受体,表现出弱拮抗特性。当光将其翻转为“顺式(cis)”构象时,同一分子变为中等强度的激活剂,使受体部分开启。间位版本(化合物2)则不肯配合:不论光照与否,其两种构象都使受体保持相当活跃,始终无法提供真正的“关”状态。本文的核心谜题是,为什么如此微小的化学改动——仅仅把一个小基团在芳环上移动一个位置——会强烈改变受体的响应。
以原子级电影窥视内部
为了解答这一点,团队使用了大量全原子分子动力学模拟,实际上制作了受体、周围膜、溶剂和每个配体中每个原子的详细电影,总时长约80微秒。他们模拟了两种分子在其受光控制的两种构象下,并在5-HT2A受体的静止与活化两种构象中进行模拟。通过追踪蛋白内部已知的结构“微开关”——例如会翻转的关键色氨酸、会断裂的盐桥,以及位于核心深处的钠离子和水的运动——他们能够判定受体是在倾向于关还是开状态。他们还将新分子的结合姿态与研究充分的部分激动剂LSD的结合位做对比,利用芳环重叠程度作为参考。
深度比形状更重要
核心观点是:分子的效力主要由其插入受体结合口袋的深度决定。在静止受体中,对位化合物的反式构象形成了一组特殊的氢键,将其异常地拉入更深处,低于典型激活接触发生的区域。这种“过度插入”阻止了它触及那些帮助开启受体的关键极性残基,从而稳定了关状态。间位化合物的反式构象无法形成相同的锚定接触,而是停留在更高处,呈现出更类似LSD的姿态,符合激活所需,解释了其残余活性。当光将两种分子转为顺式时,它们通常会移向更浅、更像激动剂的位置。然而即便如此,几何差异仍然重要:在活化受体中,顺式化合物2能够滑入两条螺旋之间的疏水通道并形成持久的氢键,强化其强效激动剂行为,而顺式化合物1由于空间阻碍无法做到这一点。
精细控制内部水和离子
模拟还显示,结合深度能微妙调节一个已知影响受体激活的内部钠位点和水通道。对位化合物在其反式构象中的深而刚性的结合使一个钠离子被紧密束缚且周围区域相对干燥,这些特征与关状态相关。相比之下,间位化合物或顺式构象的结合更具可动性,允许更多水分侵入并松动钠离子的环境,为受体激活做好准备。一个关键的芳香“开关”残基在配体灵活且未被过度锚定时更容易翻转取向,进一步推动受体向开样状态移动,尤其是在顺式化合物2的存在下。
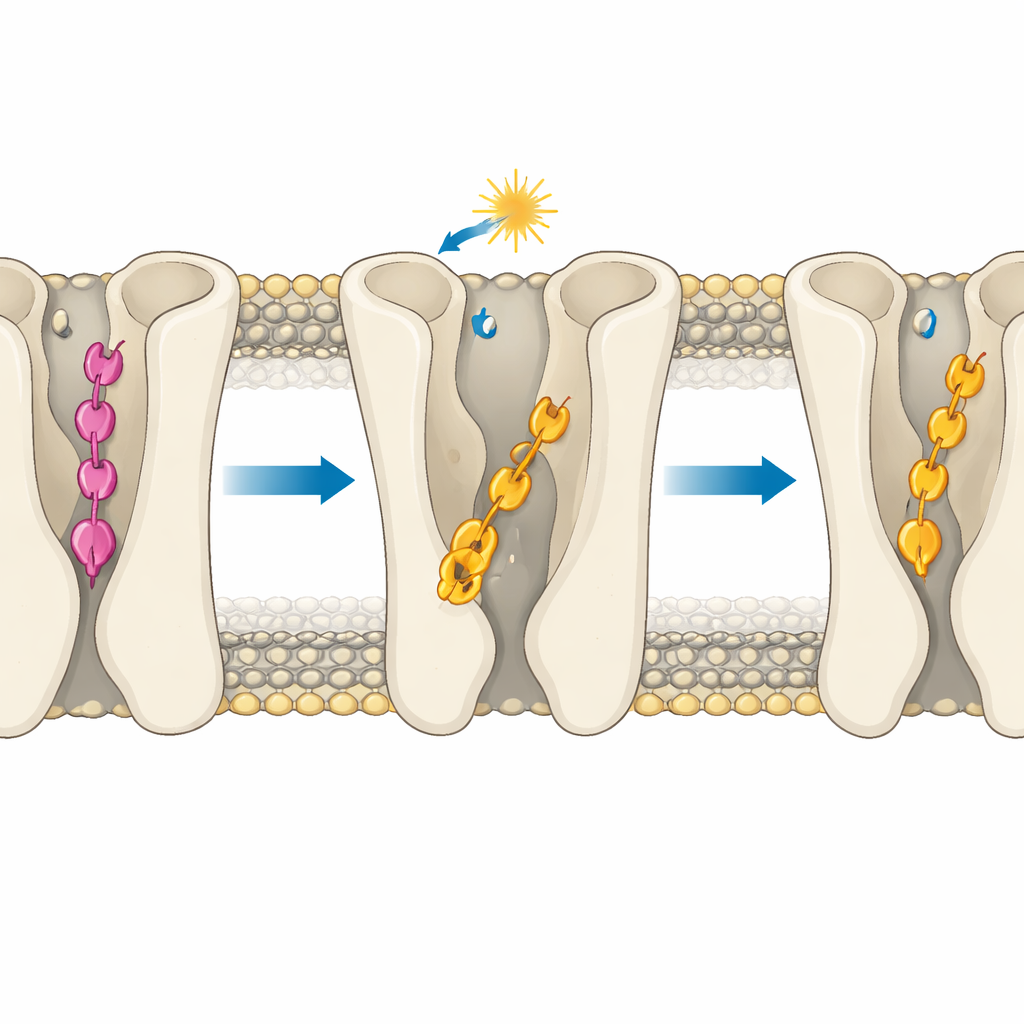
未来光控药物的设计法则
对于非专业读者来说,结论是:药物在受体口袋中所处的确切深度,可能决定关、部分开与强烈开启之间的差别——即便在化学图上改动看起来极小。通过展示一种光可逆配体如何过度插入并锁定受体关闭,而密切相关的另一种则停留在利于激活的深度,这项研究提出了一个明确的设计原则:在控制光致构象变化的同时,也要像控制构象一样精确地控制插入深度。这些洞见可指导新一代光敏化合物的开发,以前所未有的精度治疗脑部疾病,在可控、可逆的方式下调节信号通路并将副作用降到最低。
引用: Weber, V., Salvadori, G., Natale, F. et al. Binding pose depth modulates photoswitchable ligands’ efficacy at the 5-HT2A receptor. Commun Chem 9, 121 (2026). https://doi.org/10.1038/s42004-026-01936-5
关键词: 光药理学, 5-HT2A 血清素受体, 光可逆配体, GPCR 激活, 分子动力学模拟