Clear Sky Science · zh
通过研究tau/TDP-43液滴揭示的多组分蛋白凝聚体中支架-客户行为与结构组织
像微小油滴一样行为的蛋白质
在细胞内部,许多蛋白质并不会在水样细胞质中均匀分布。相反,它们聚集成微小的液滴,有点像油在水中的表现。本研究考察了两种此类蛋白——与阿尔茨海默病及其他痴呆密切相关的tau和TDP-43——如何共同聚成液滴。通过揭示这些液滴如何形成、混合与组织,这项工作为解释衰老大脑中有害蛋白聚集体为何出现以及未来如何可能加以控制提供了线索。
这两种脑蛋白为何重要
tau和TDP-43都已知在神经退行性疾病中形成有毒聚集体。传统上,科学家多单独研究它们,但人类脑部尸检越来越多地显示两者可在相同的受损区域共存。这提出了一个关键问题:当tau和TDP-43在细胞中同时存在时,它们在液滴内部如何分配空间,这种共存环境是否会促成与疾病相关的聚集?作者选择了一个简化但现实的模型:tau与TDP-43的低复杂性尾段(LCD),后者是最负责液滴形成与最终固化的部分。
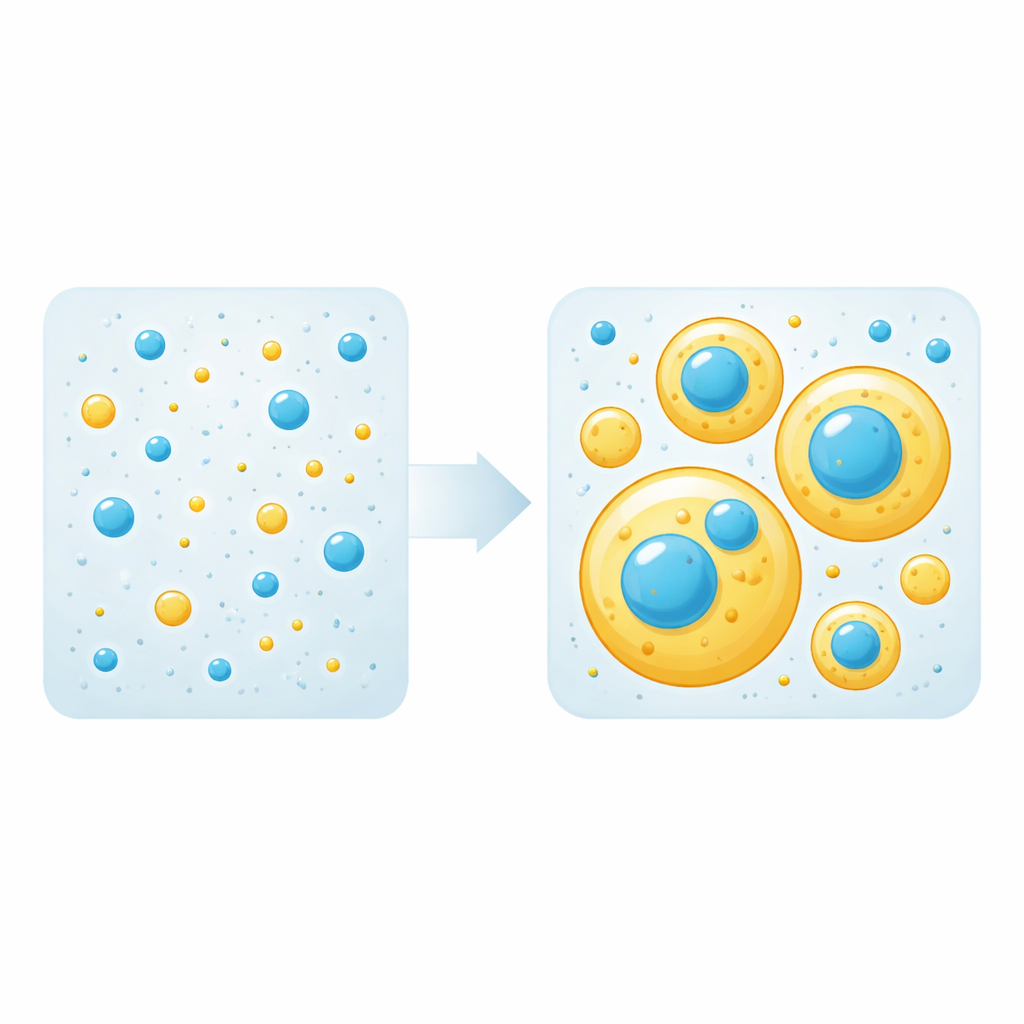
液滴、“支架”与“客户”
当蛋白–蛋白吸引力超过蛋白–水的亲和力时,这类液滴便会形成,导致溶液分裂为高密度相(液滴)和稀释相。在混合体系中,只有部分蛋白构建液滴;这些被称为“支架”。其他蛋白则作为“客户”被动带入液滴。研究团队首先测定了每种蛋白单独开始形成液滴的浓度阈值。随后他们混合不同比例的tau与TDP-43 LCD,并用荧光显微镜观察是否出现液滴以及蛋白如何分布。引人注意的是,他们发现任一蛋白是支架还是客户完全取决于其自身的浓度:当其高于自身阈值时它构建液滴,低于阈值时则被另一种蛋白形成的液滴被动招募。
分层液滴与神秘的晕环
当两种蛋白都足以单独形成液滴时,它们并未混合成单一均匀液滴。相反,较大的富含tau的液滴包裹着较小的富含TDP-43的液滴,形成分层的多相结构。对液滴在玻璃表面铺展行为的测量显示,TDP-43液滴具有更高的表面张力,因此将其置于更润湿(更易铺展)的tau液滴内部在能量上更有利。界面处出现了一个醒目的特征:tau在TDP-43液滴表面以特别高的浓度沉积,形成明亮的“晕环”,即便此时tau自身的液滴形成浓度尚未达到。随着时间推移,富含TDP-43的区域趋向于变得更为僵硬、类似固体,而富含tau的区域则保持液态,提示两者在转变为长寿命聚集体上的倾向不同。
调节相互作用并探查微观机制
作者接着测试了哪些分子力决定了哪种蛋白充当支架或客户。他们用1,6-己二醇选择性削弱驱动TDP-43 LCD凝结的疏水(排水)相互作用;并通过增加盐浓度分别削弱驱动tau凝结的静电(基于电荷)相互作用。在每种情况下,破坏一种蛋白的关键相互作用都会阻止其形成液滴,并使其成为另一种蛋白液滴中的客户,模拟了降低其浓度时的情形。为更深入理解晕环,他们改变盐浓度以观察tau进入TDP-43液滴的程度,并使用将每个氨基酸简化为一个珠子的计算机模拟。这些模拟重现了晕环,并显示tau带负电的N端区域的前约40个氨基酸在液滴表面锚定,而分子的其余部分则向外延伸到周围液体中,形成一种“两亲性”(部分亲凝聚相、部分亲水)的包覆层。用缺失该N端片段的缩短tau碎片进行的实验证实:没有这段序列,晕环就会消失。

对脑疾病的意义
总体而言,这些结果揭示了多组分蛋白液滴组装与组织的一组通用规则。在这个模拟病态神经元情形的tau/TDP-43体系中,浓度与相互作用强度共同决定哪些蛋白构建液滴、哪些仅占据其中。表面张力与两亲性排列进而塑造出分层液滴和晕环,使多种与疾病相关的蛋白在同一受限空间中被浓缩,可能促使它们硬化成聚集体。对非专业读者来说,关键的信息是:tau和TDP-43并非随机团聚;它们自组织成由简单物理原理支配的有结构液滴。理解并最终操控这些原理,可能为减缓或预防神经退行性疾病中有害蛋白堆积开辟新路径。
引用: Monnaka, V.U., Shipley, B., Boyko, S. et al. Scaffold-client behavior and structural organization in multicomponent protein condensates as revealed by studying tau/TDP-43 droplets. Commun Chem 9, 126 (2026). https://doi.org/10.1038/s42004-026-01933-8
关键词: 蛋白质凝聚体, 液-液相分离, tau蛋白, TDP-43, 神经退行性疾病