Clear Sky Science · zh
人类 RegⅢα 纤维形成的结构基础
我们的肠道如何对抗病菌
我们的肠道不断暴露于数十亿细菌,其中许多无害甚至有益。但当危险的微生物出现时,机体需要快速且精确的方式去攻击它们,同时不损伤自身组织。本研究仔细考察了一种天然防御蛋白 RegIIIα,揭示了它如何改变构象以杀死细菌,随后又转变为更安全、毒性较低的形式。理解这种构象转换有助于科学家更好地把握肠道微生物的平衡维持机制以及疾病时发生的紊乱。
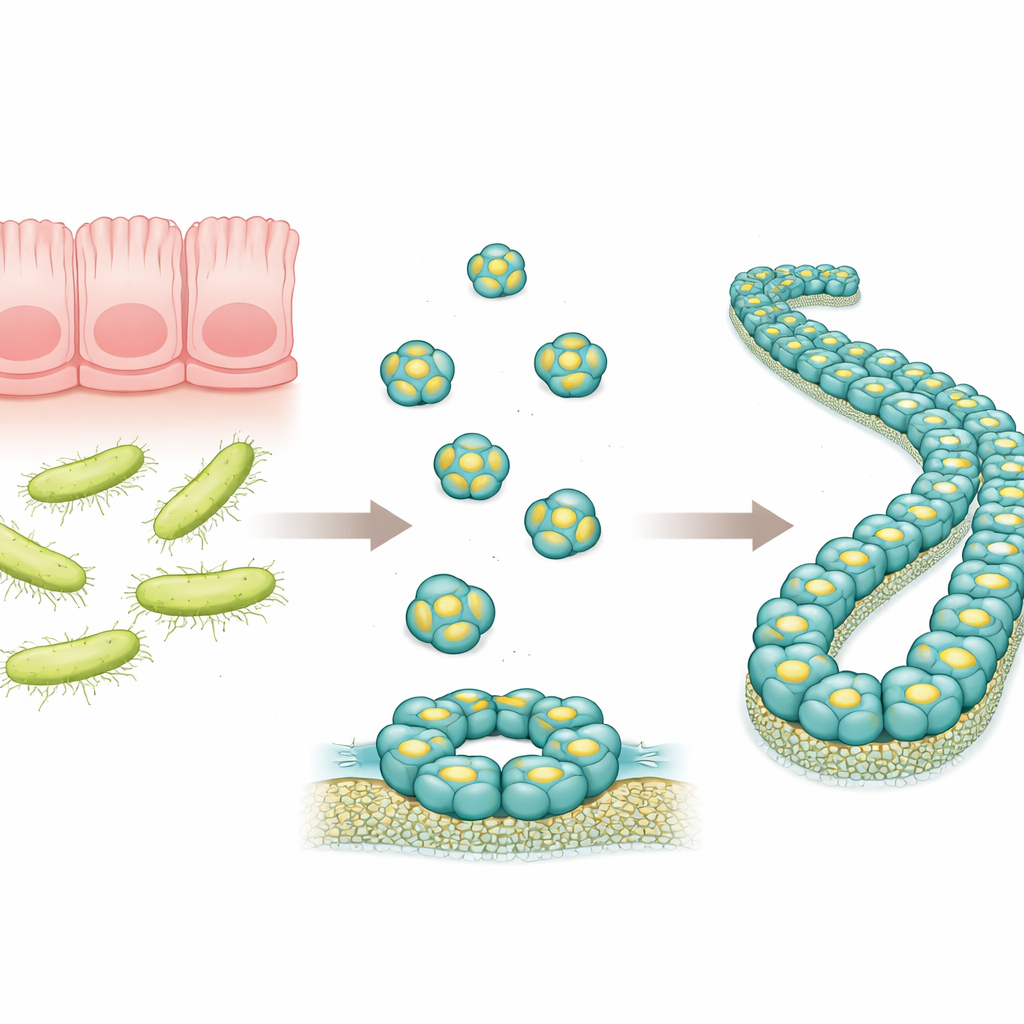
肠道中的微小护卫
RegIIIα 是肠道产生的一种蛋白,靶向特定细菌,尤其是具有厚外壁的革兰氏阳性细菌。早期工作表明,RegIIIα 能通过形成环状结构在细菌膜上打孔,使微生物内容物泄漏从而导致其死亡。研究者还观察到,这些环结构随着时间可以堆叠成长纤维,似乎会降低蛋白的杀菌活性。然而,这些大组装体中 RegIIIα 分子的确切排列细节尚不清楚,因而难以理解蛋白的工作方式及其活性如何被调控。
以近原子分辨率观察纤维
在本研究中,作者在细菌中表达人源 RegIIIα,并在受控条件下诱导其组装成纤维。他们使用一种强大的成像方法——低温电子显微镜(cryo-EM),该方法可以在近原子分辨率下可视化被冰冻在薄层冰中的生物分子。他们发现,纤维由重复的三聚体单元构成,这些三聚体以规则的螺旋方式堆叠。每个单独的 RegIIIα 分子与先前晶体结构中所见十分相似,但在纤维中的取向不同于早期较低分辨率模型。这个修正后的取向改变了科学家对该蛋白与细菌膜及其自身调控段相互作用的理解。
蛋白如何连接以及脂质为何重要
通过仔细检查结构,研究者鉴别出两个主要接触区或界面,邻近的 RegIIIα 分子在这些区域接触并将纤维维系在一起。随后他们对这些界面上的特定氨基酸进行了替换,结果显示这些改变阻止了纤维的形成,证实这些接触位点对组装至关重要。有趣的是,在两个界面中,cryo-EM 图谱都显示出额外的模糊区域,可能代表嵌在蛋白表面之间的小而细长的分子。它们的形状和化学环境暗示这些可能是脂质——与构成细胞膜的油性分子相同的种类。这支持了早先脂质促进 RegIIIα 组装的线索,可能是通过像分子胶一样稳定亚基间的连接来实现。
开–关开关:pH 与隐藏的片段
研究团队还调查了什么因素控制 RegIIIα 的组装。在其变得活性之前,蛋白携带一段短的“前体片段”(pro-segment),该片段必须被消化酶切除。他们的高分辨率纤维结构显示,在组装中心没有空间容纳这段额外片段,这意味着前体片段阻碍了 RegIIIα 形成穿孔环和纤维的能力。研究还发现,纤维形成的倾向依赖于酸碱度:在类似小肠的 pH 下纤维易于形成,而在更酸性的 pH 下则形成较差。单个氨基酸——组氨酸50(His50)——似乎充当 pH 敏感的开关;当其被替换为其他残基时,纤维形成对 pH 的敏感性显著下降。酶切、脂质结合与 pH 这几重机制共同构成了一套分层的控制系统,调节 RegIIIα 在何时何地发挥活性。
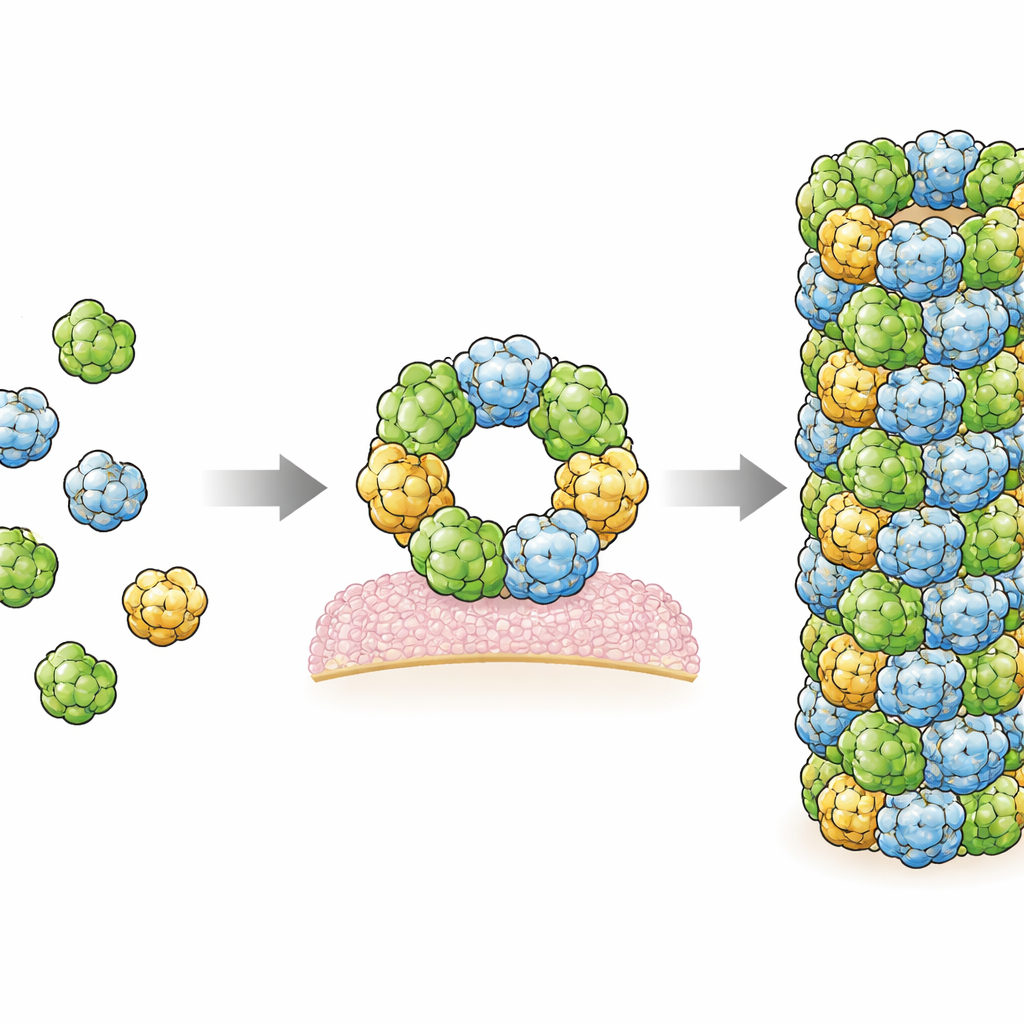
对肠道健康的意义
总体而言,这项工作提供了迄今最详细的图景,说明 RegIIIα 分子如何组装成与其抗菌作用及自限行为相关的更大结构。构建纤维的相同界面也参与构建被认为在细菌膜上形成孔道的六聚体环,这暗示了强效杀伤形式与更安全的受抑制状态之间的微妙平衡。将疾病相关突变映射到该结构上显示,许多突变位于关键接触点,提示组装紊乱可能是某些肠道或胰腺疾病的病理基础。通过阐明这种天然抗生素如何被激活、如何受脂质引导以及如何受局部 pH 影响,该研究为未来调节先天防御的尝试奠定了基础——无论是增强对感染的防御,还是在防御失调时使其平息。
引用: Han, J., Cao, Q. Structural basis for human RegⅢα filament formation. Commun Chem 9, 117 (2026). https://doi.org/10.1038/s42004-026-01921-y
关键词: RegIIIα, 肠道免疫, 低温电子显微镜, 蛋白质纤维, 抗菌肽