Clear Sky Science · zh
偶氮苯连接的可电离两亲性两面糖苷,实现光控、单组分及器官可调的质粒DNA递送
用光照亮更智能的基因递送
基因疗法有望通过将遗传信息直接输送到细胞来根治疾病。但将这类脆弱货物在血液中安全引导、到达正确的器官并进入目标细胞仍是主要障碍。本研究引入了一类新的微小糖基颗粒,其行为可以在进入体内之前通过光被切换,使研究者能够重定向治疗性基因的去向及其表达强度,同时对细胞的伤害很小。 
对精确基因载体的需求
目前最成功的基因递送载体是脂质纳米颗粒,它们促成了mRNA新冠疫苗的实现。这些多组分液滴包裹并保护核酸,但它们倾向于主要在肝脏累积,并且只有一小部分货物在细胞内被释放。改变其组成可以调整偏向的器官,但这些混合物复杂且难以精确控制。研究团队旨在设计单一、定义明确的分子,这些分子能自组装成具有可预测形状和行为的纳米颗粒——并能通过简单的光触发从外部主动调控。
由光控制的分子跷跷板
新系统的核心是成对的“两面”(Janus)糖苷:由两个葡萄糖单元构成的分子,带有亲水的带电头部和亲脂的尾部,并通过中心的偶氮苯“铰链”连接。偶氮苯在不同颜色光照下可以在两种镜像形态(称为E和Z)之间翻转。在含有DNA的水溶液中,许多此类分子会自发聚集成软性的层状颗粒,包裹质粒DNA链。研究者制备了两种版本——一种为糖与铰链之间通过氧桥连接,另一种为硫桥连接——以微调稳定性和生物学行为。通过预先照射溶液,他们可以富集E或Z构型,并研究每种状态如何影响所形成的基因递送颗粒。
变形颗粒的行为
对颗粒尺寸、表面电荷和内部结构的测量表明,由光诱导的E/Z构型切换带来明显的物理差异。总体上,Z构型产生的纳米颗粒更小、形状更均一,且内部呈现比E构型更有序的层状结构。显微观察显示这些内部结构类似交替的类脂片层与DNA层。重要的是,两种构型都能保护DNA免受酶解。在肾脏、肝脏和免疫组织来源的细胞培养中,不同异构体状态导致了截然不同的基因表达水平,尽管所用DNA相同。对进入细胞后的颗粒施以反复光脉冲能将基因表达提高数倍,这表明构型切换带来的机械刺激有助于颗粒松动并释放其货物,也可能帮助颗粒逃逸细胞内隔室。 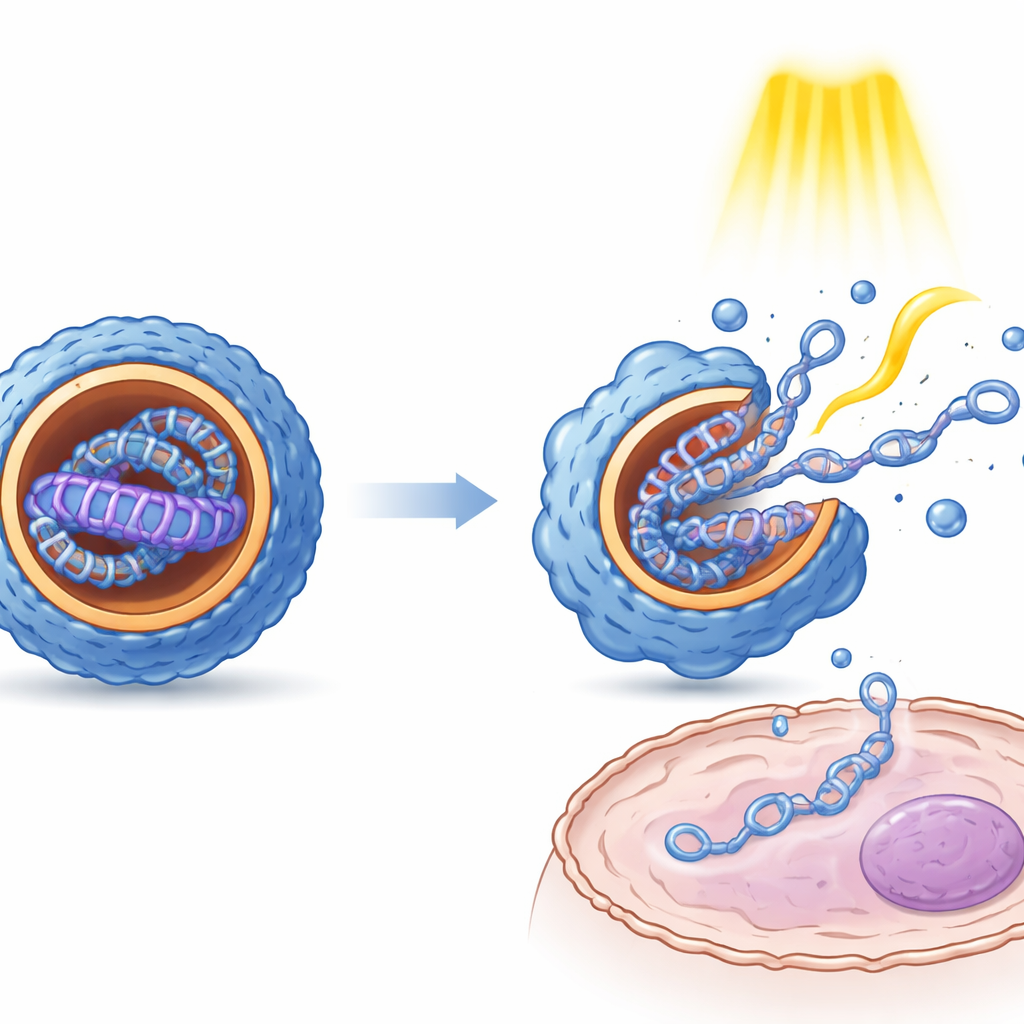
将基因引导到特定器官
在小鼠体内观察到的行为最为令人惊讶。当氧桥连接的颗粒以富含E构型给药时,标记基因的表达主要出现在肝脏,并伴有少量肺部表达。将其在注射前预先切换为Z构型不仅提高了总体表达水平,还将分布偏向肺部。硫桥连接的颗粒则呈现不同模式:其Z构型更偏向脾脏这一关键免疫器官。因此,利用相同的基本分子骨架——且无需改变DNA货物——研究者只需选择连接键(氧或硫)和载体的光激活形态(E或Z),就能将基因活性主要定向到肝、肺或脾。在这些测试中,细胞存活率保持较高,表明该系统相对温和。
一种可用光调节的未来基因药物路线
通俗地说,团队构建了一个微小且可光切换的DNA运输载体。注射前,短暂的光处理“编程”这些载体为两种形态之一。每种形态组装出具有特征尺寸和表面特性的纳米颗粒,这反过来决定了它们与不同细胞类型的亲和力以及在体内的分布。由于相同的化学骨架可以通过许多小改动来调整,且构型切换是可逆的且不改变DNA本身,该平台提供了一种灵活的方法来精细控制基因疗法的作用部位和方式。尽管在临床应用之前仍需大量工作,这项研究表明经过精心设计的、由单一分子构成且受光控制的载体有望成为更安全、更精准基因药物的有力工具。
引用: Wang, Z., Rivero-Barbarroja, G., Benito, J.M. et al. Azobenzene-bridged ionizable amphiphilic Janus glycosides for light-controlled, single-component and organ-modulable pDNA delivery. Commun Chem 9, 118 (2026). https://doi.org/10.1038/s42004-026-01920-z
关键词: 基因递送, 光响应纳米颗粒, 偶氮苯开关, 靶向DNA疗法, 纳米医学