Clear Sky Science · zh
S9 蛋白酶 WprP2 在 RiPP 生物合成中对前体肽进行均一切割
细胞内这些微小切割工具为何重要
在细菌体内,专门的分子剪刀将长的氨基酸链切割成更短、更具活性的片段,这些片段常成为抗生素或其他有用的天然产物。该研究揭示了一种此前未知的切割工具——名为 WprP2 的蛋白酶,它以不寻常的精确度修剪其靶肽。理解该酶的工作机制可帮助科学家设计新的生物活性肽和下一代抗生素。
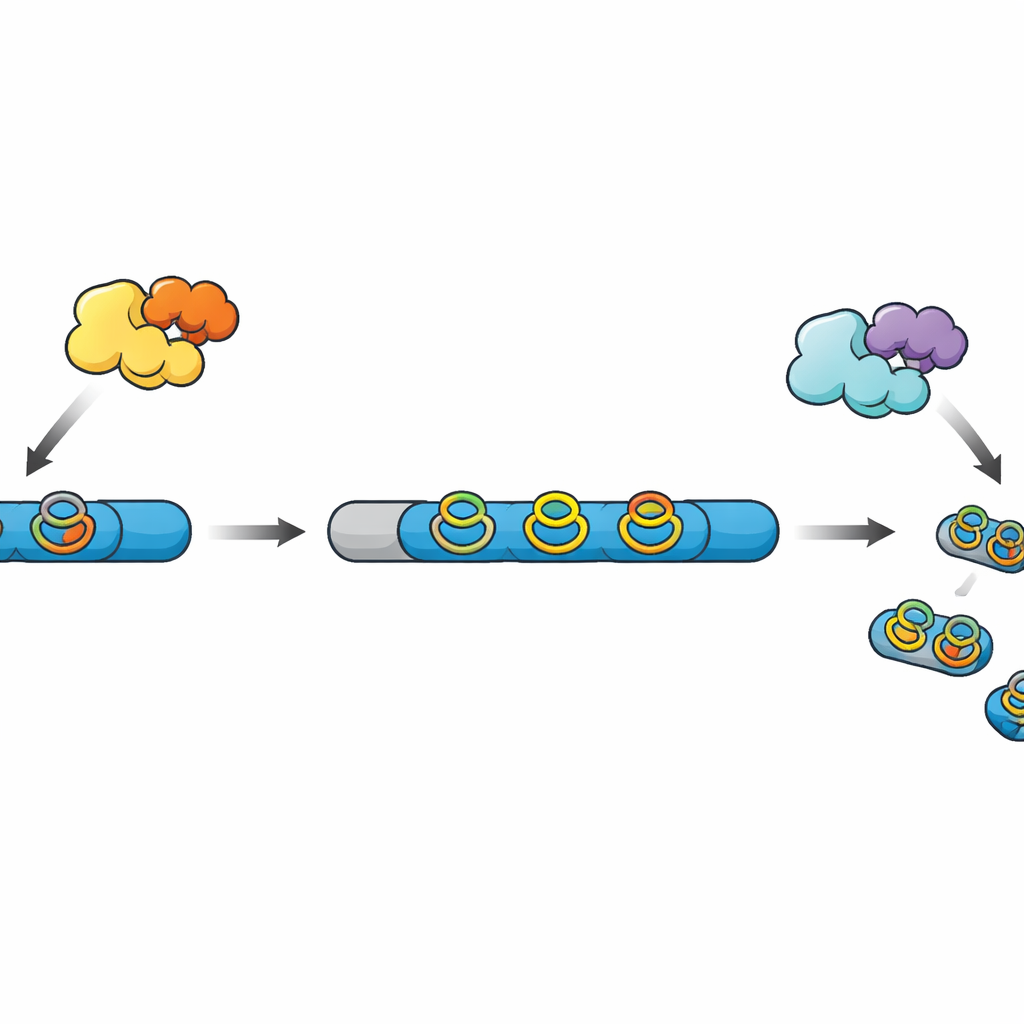
从原始链到成品小型药物
许多现代的肽类天然产物,统称为 RiPPs,起始于核糖体合成的简单肽链。这些肽链包含一个作为抓手的前导区和将通过一系列化学修饰成为最终产物的核心区。其他酶会添加交联和环结构,使肽更稳定、活性更高,最终由蛋白酶切除前导肽并释放成熟分子。在最近发现的一类 RiPP 中,radical SAM 酶构建涉及芳香族氨基酸的紧凑“环芳烃”环,但在大多数已知的基因簇中,匹配的蛋白酶缺失,使得最终加工步骤成谜。
追踪缺失的伙伴酶
作者此前研究过一种名为 WprB1 的 radical SAM 酶,该酶在前体肽的三个重复 WPR 片段上安装相同的交联。在新工作中,他们在细菌基因组中搜索该酶的亲缘蛋白,并在邻近区域寻找可能编码蛋白酶的基因。在斯氏链霉菌(Streptomyces venezuelae)中,他们发现了一个有希望的基因簇,包含类似的交联酶、其辅助蛋白、含有三个 WPR 重复的匹配前体肽以及一个候选的 S9 家族丝氨酸蛋白酶,他们将其命名为 WprP2。这使该系统成为揭示肽最终如何被切割以释放活性片段的理想实验模型。
观察肽被切割的过程
为研究 WprP2,团队在细菌中生产了前体肽(有无交联酶两种情况),将其纯化后在受控的体外反应中与该蛋白酶混合。质谱分析表明,WprP2 首先在每个 WPR 片段之后立即切断链,然后在序列中较远处的特定位点——一个脯氨酸残基之前的固定距离处再进行第二次切割。这两步形成了一系列较小且均一的片段。值得注意的是,无论交联酶是否已安装环芳烃环,WprP2 都执行这一切割模式,表明环结构并非识别所必需。与商业胰蛋白酶(trypsin)相比,后者在某些交联位点无法切割,而 WprP2 仍能发挥作用,强调了其不寻常的耐受性。
解码酶识别的要点
研究人员接着探究 WprP2 实际识别肽的哪些特征。通过系统性地改变切割位点附近的单个氨基酸,他们发现改变许多邻近残基影响不大,但改变 WPR 片段中的关键精氨酸或第二次切割位点的谷氨酰胺或脯氨酸则可阻断相应步骤。对带有不同侧翼残基的相关前体肽的实验显示,蛋白酶仍会在 WPR 重复之后切割,但仅在存在谷氨酰胺‑脯氨酸对时才执行第二次切割。使用 AlphaFold3 生成的计算结构模型支持了这一图景:在预测的复合体中,基于 WPR 的位点和谷氨酰胺‑脯氨酸位点依次与酶的催化中心排列一致,符合一个顺序的两步机制。
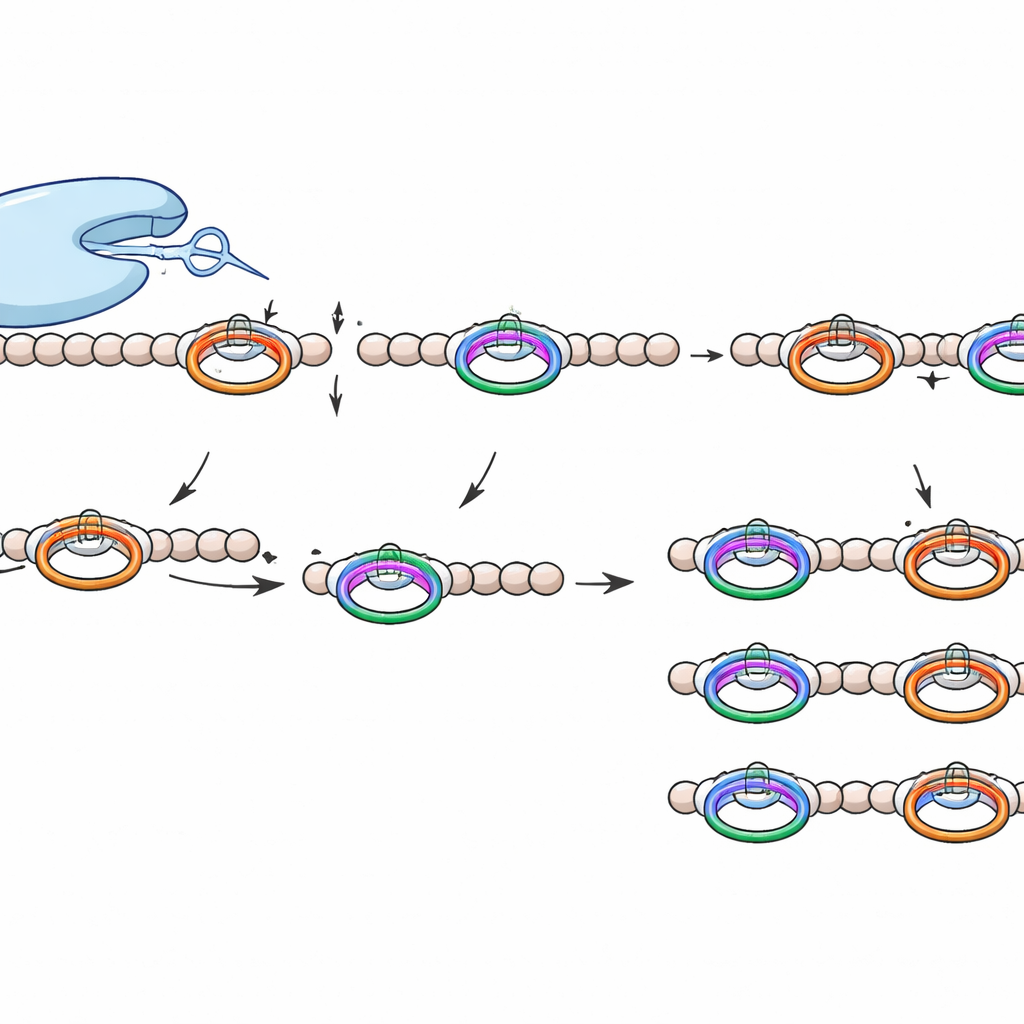
使该切割工具与众不同的地方
WprP2 属于更广泛的 S9 蛋白酶家族,该家族已包含若干与医学相关的酶,但 WprP2 在若干方面独树一帜。它在脯氨酸残基的 N 端侧进行切割(而不是在其之后),它作用于重复基序以在整个前体链上产生均匀尺寸的片段,并且对位于两个识别位点之间的氨基酸显示出较大的容忍性。这种精确性与灵活性的组合在已知的 RiPP 相关蛋白酶中尚属首次。
这一发现的潜在应用
通过揭示一种识别简单序列线索并进行均匀、重复切割的蛋白酶,这项工作为不断扩展的肽工程工具箱增添了一个强大的新工具。就实际应用而言,WprP2 可被利用来释放或重塑设计肽,包括那些含有复杂交联、对常规酶(如胰蛋白酶)具有抗性的肽。对非专业读者而言,核心结论是科学家发现了一种新型分子剪刀,它能将长肽链切割成精确、均一的片段,从而为更可控地生产潜在抗生素和其他生物活性分子打开了大门。
引用: Haedar, J.R., Khan, A.H., Ma, S. et al. S9 protease WprP2 catalyzes uniform cleavage on the precursor peptide in RiPP biosynthesis. Commun Chem 9, 108 (2026). https://doi.org/10.1038/s42004-026-01915-w
关键词: RiPP 肽, 丝氨酸蛋白酶, WprP2, 环芳烃类天然产物, 肽工程