Clear Sky Science · zh
离子液体包覆金核高分子纳米颗粒用于选择性中性粒细胞搭载以治疗子宫内膜异位症
重新思考一种常见却隐蔽疾病的缓解方式
子宫内膜异位症是一种疼痛性疾病,子宫内膜样组织在不该出现的部位生长,常导致剧烈痉挛、慢性疼痛和生育问题。现有治疗多依赖激素或手术,常伴随副作用、反复治疗且不能保证长期缓解。本研究探讨了一种截然不同的想法:利用微小的光激活颗粒搭乘自身免疫细胞前往病灶,温和摧毁病变组织,这有望成为一种非手术方案,保护生育功能并减少副作用。
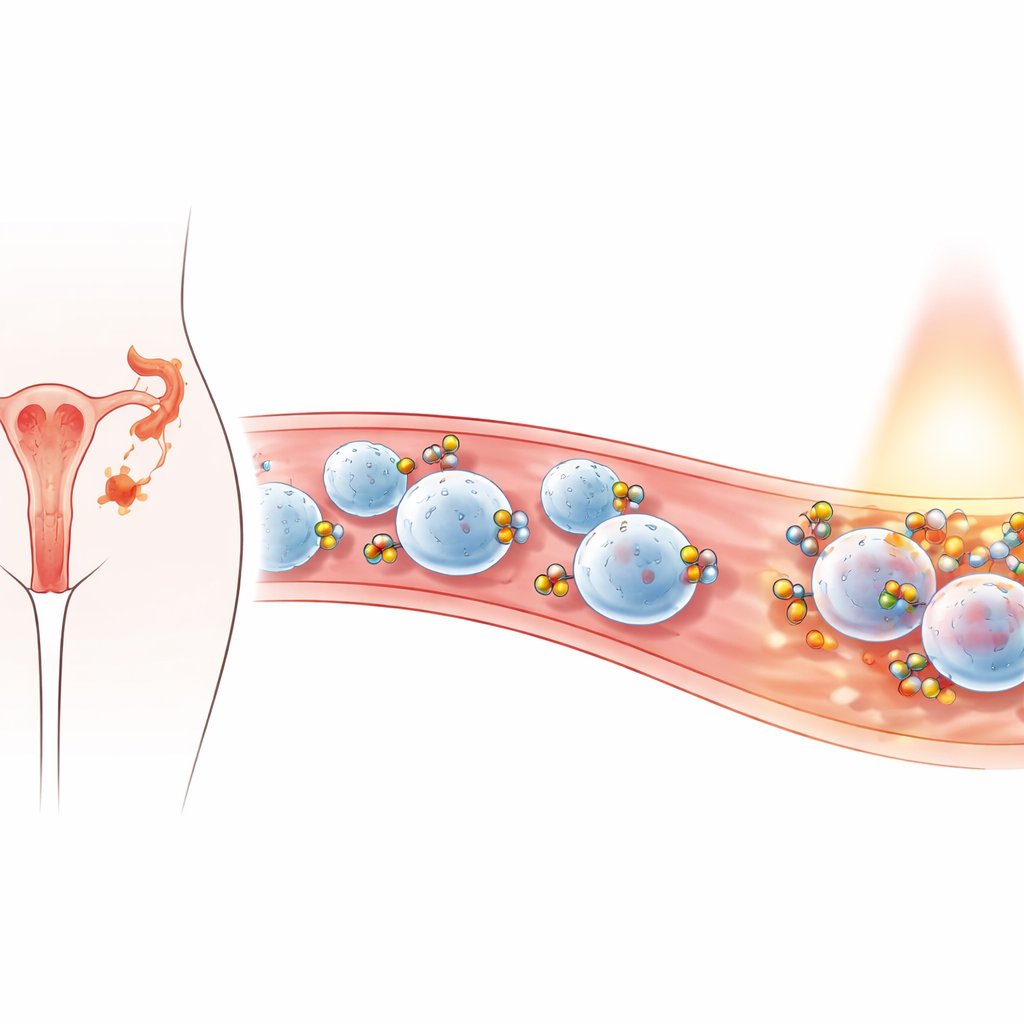
搭乘机体首发应答者的小帮手
研究人员聚焦于中性粒细胞,这类白细胞会迅速赶赴炎症部位,包括子宫内膜异位病灶。他们的策略是通过包覆纳米颗粒使其被中性粒细胞自然摄取或携带在细胞表面,从而“搭便车”。当中性粒细胞迁移到受炎症影响的子宫内膜组织时,会把纳米颗粒一并带到那里,在病灶处集中治疗而尽量保护健康区域。关键在于,健康盆腔组织在大部分月经周期内中性粒细胞的活跃度通常较低,这有助于把治疗聚焦在病变部位而非正常组织。
构建智能、对光响应的纳米颗粒
为使该系统发挥作用,团队构建了具有三重关键成分的颗粒。核心为金属金,因其能吸收近红外光并可受控地将光能转化为热能。金核外包覆一层可生物降解的高分子壳层PLGA,这种材料在医疗植入物和药物递送中被广泛使用。最后,他们用特殊的“离子液体”——在相对较低温度下保持液态的带盐性油状分子——对壳层进行包覆。通过精心选择离子液体,他们能够调节颗粒与血细胞(尤其是中性粒细胞)之间的相互作用。显微镜和粒径测量证实颗粒形成了整齐的核壳结构,光学测试显示包覆层改变了颗粒的光吸收特性,从而提升了其加热性能。
在不使用强烈药物的情况下加热病变细胞
在获得稳定的颗粒设计后,研究人员在体外用人类子宫内膜细胞测试了这些纳米级加热器的效果。当含颗粒的溶液用近红外光照射——类似可由医疗激光提供的光源——总体温度仅上升数摄氏度,但这足以损伤周围细胞。重要的是,无光照时这些颗粒基本无害:暴露于颗粒的子宫内膜细胞在广泛剂量范围内仍保持超过80%的活力。然而在光照下,细胞主要经历的是凋亡,这是一种有序的程序性细胞死亡,而非可引发炎症的坏死。额外检测显示几乎无DNA损伤迹象,也未检测到被处理细胞释放促炎信号分子。
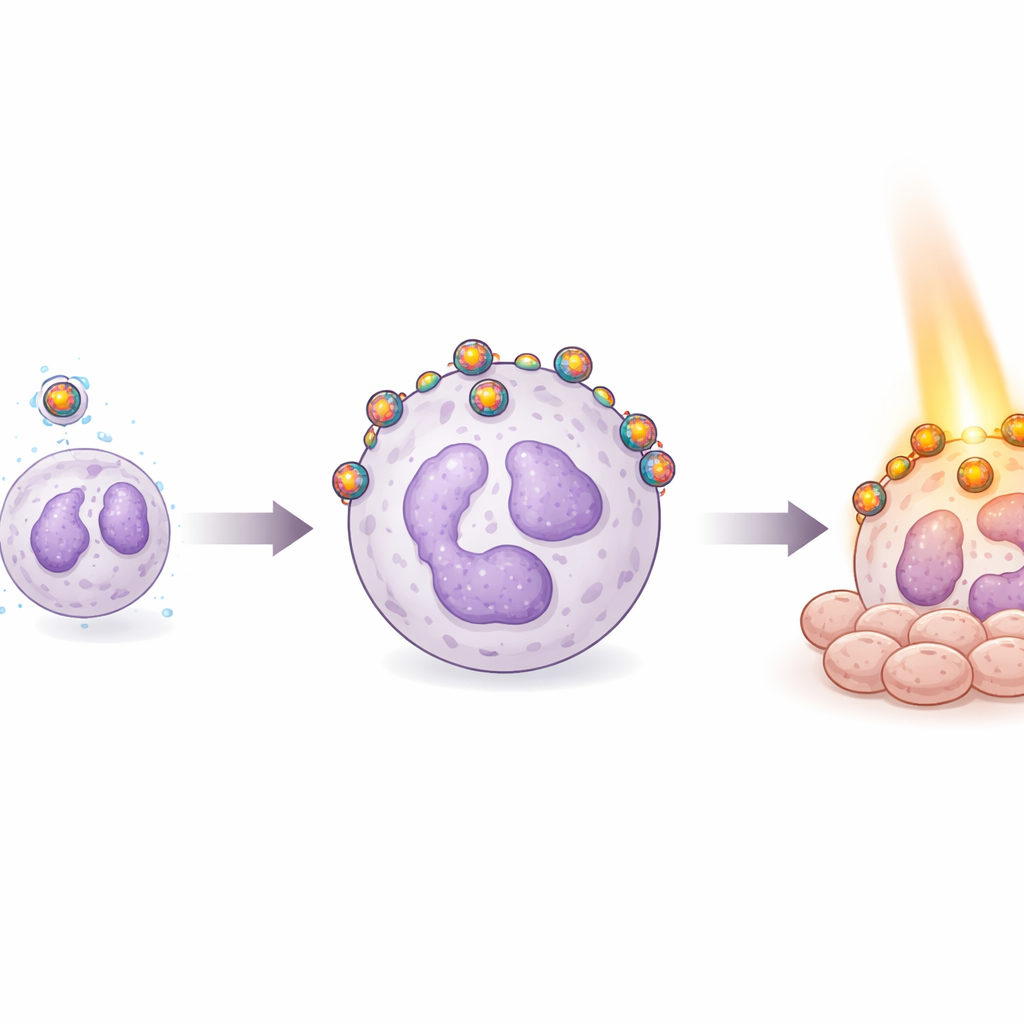
验证血液安全性并追踪“搭车”过程
对任何静脉注射治疗而言,血液内的安全性至关重要。团队将这些纳米颗粒与人红细胞接触,结果显示基本无溶血——红细胞破裂会引发严重并发症——表明颗粒对血液温和。他们随后给颗粒加入荧光染料并与人血样混合,以追踪颗粒偏好结合的细胞。与未包覆颗粒相比,离子液体包覆的颗粒与中性粒细胞的关联明显更强。有些包覆促使中性粒细胞吞噬颗粒,而另一些则使颗粒像小珠子一样粘附在细胞表面。两种结合方式都增加了中性粒细胞中检测到的金含量,证实这些包覆成功引导纳米颗粒搭载于机体天然的炎症运输细胞上。
对未来治疗的潜在意义
总体而言,该研究提出了一种新型“智能”纳米颗粒,设计用于随中性粒细胞搭载、在血液中安全循环,并在温和激光触发时通过可控的加热主要诱导细胞通过程序性自毁路径死亡,从而杀灭子宫内膜细胞。尽管这些实验是在细胞和血样中完成,尚未在活体患者中验证,但结果表明未来有可能无需大手术或大量激素即可体内治疗子宫内膜异位病灶。通过将靶向递送与可精确控制的光热加热相结合,这一方法有望在未来提供更持久的缓解、更少的副作用以及更好的生育保护,造福患有子宫内膜异位症的人群。
引用: Vashisth, P., Clerc, L.T.D., Hu, D. et al. Ionic liquid-coated gold core polymeric nanoparticles for selective neutrophil hitchhiking towards endometriosis treatment. Commun Chem 9, 119 (2026). https://doi.org/10.1038/s42004-026-01909-8
关键词: 子宫内膜异位症, 纳米颗粒, 光热治疗, 中性粒细胞, 靶向药物递送