Clear Sky Science · zh
用于人类NQO1氧化还原循环的时间分辨串行晶体学的最小化样品消耗
用更少的珍贵样品观察酶的工作
现代生物学常借助强大的X射线激光来观察生命分子的运动与构象变化,但这些实验通常消耗大量精心制备的蛋白质。本研究引入了一种更高效地将微小蛋白晶体“送入”X射线自由电子激光的新方法,可将所需材料减少多达97%。研究还表明,这种节省样品的方法仍可捕捉到与医学相关的人体酶活性早期步骤,为更常规地拍摄蛋白工作时的“电影”打开了大门。 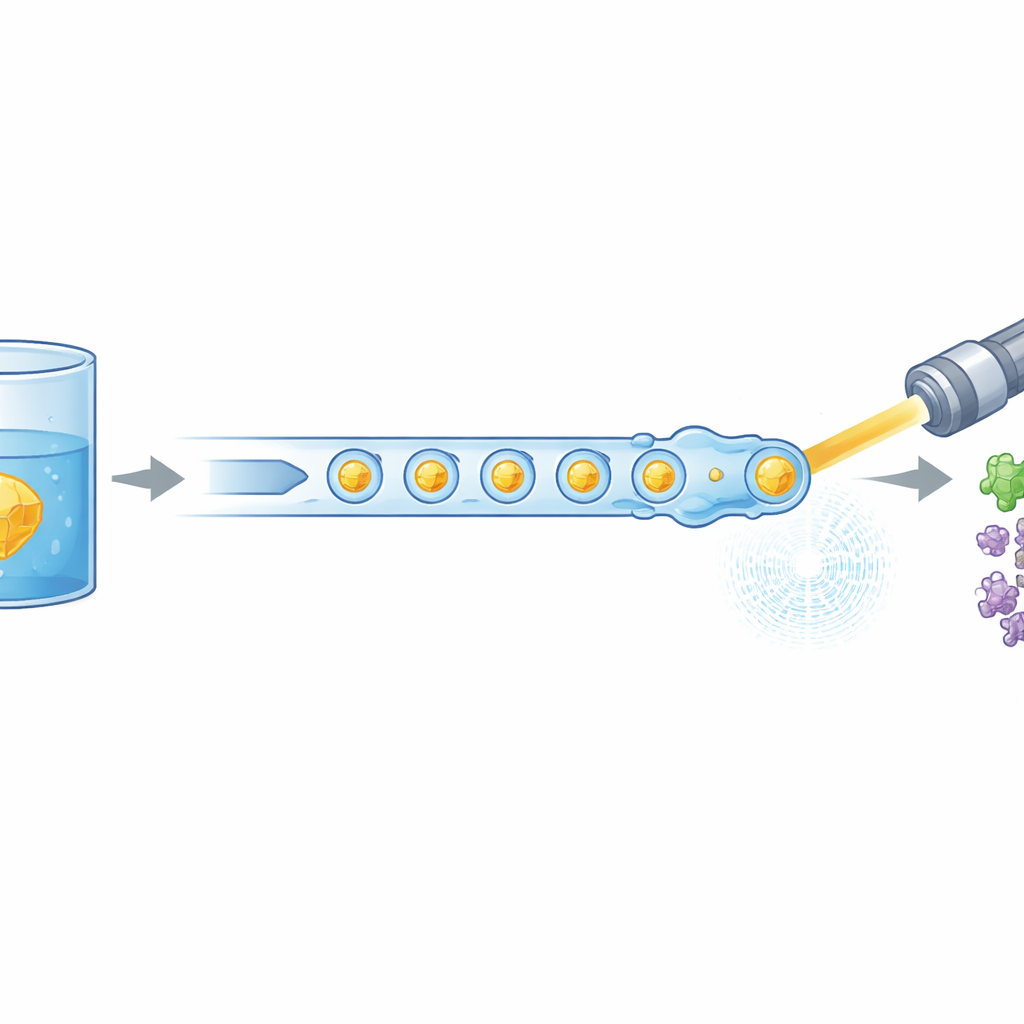
为什么拍分子电影代价高昂
为了理解蛋白质如何真正发挥功能,科学家越来越多地从静态快照转向跟踪反应实时变化的时间推移“电影”。一种领先方法是时间分辨串行晶体学,它将数百万个微小蛋白晶体喷洒过超亮的X射线束。每个晶体仅被击中一次,从而获得无损伤的结构信息,成千上万张这样的图像合成完整画面。问题在于,反应沿途的每个时间点——十分之一秒、整秒等——都需要一批新的晶体。由于蛋白制备往往耗时且昂贵,样品消耗已成为一个主要瓶颈,尤其是在像欧洲XFEL这样脉冲以兆赫率成列到达的尖端设施。
按需输送微小液滴的新方法
研究人员通过重新设计晶体输送方式来解决这一问题。他们不是使用连续流液,而是产生精确间隔的微小液滴列,每个液滴内包含蛋白晶体,并由油相隔开。一个微型3D打印装置将两股流——蛋白晶体和溶解的反应物——合并成微小混合体,随后被切分成液滴。这些液滴被引导通过一个气体聚焦喷嘴,形成一个与真空环境和XFEL速度相兼容的窄喷流。关键在于,液滴生成与X射线脉冲列在电气上同步,使几乎所有有用的脉冲都击中液滴而非空白液体。 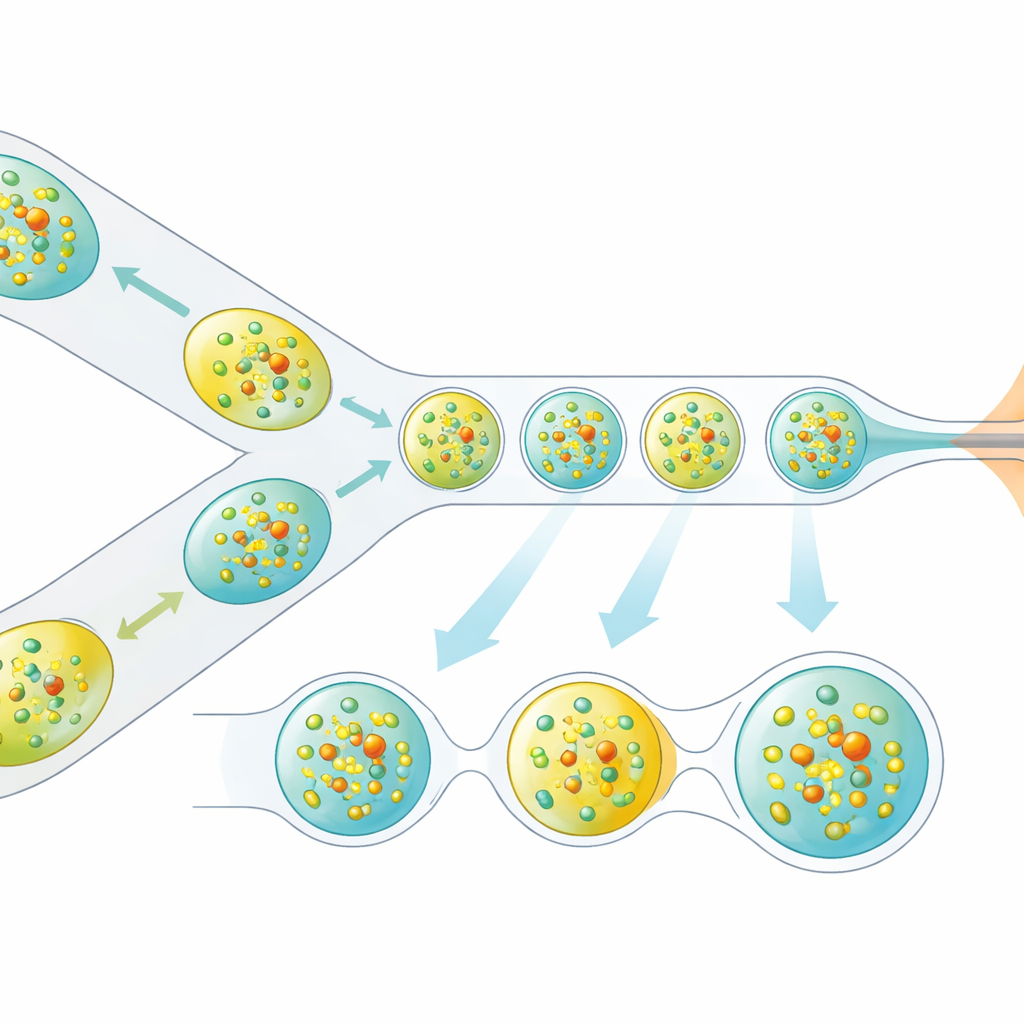
用一种人类酶检验该方法
为证明基于液滴的方法能应对真实的生物学问题,团队研究了NAD(P)H:醌氧化还原酶1(NQO1),这是一种参与细胞氧化还原平衡并与疾病相关的人类酶。他们将NQO1的微晶与其天然辅因子NADH混合,并在混合后两个早期时间点——0.3秒和1.2秒——对体系进行探测。通过分析所得的X射线衍射图样,他们为每个延迟时间重建出了该酶的三维结构。尽管使用的蛋白量远低于传统的连续流实验,数据质量仍足以在酶的活性位点揭示细微的电子密度特征,这与NADH分子以低占有率开始结合的情形一致。
早期结构快照揭示了什么
这些结构显示,混合后不久,晶体中的各活性位点并不完全一致地表现。在0.3秒时,晶胞中四个位点中的三个清楚地出现了NADH的迹象,且常以不止一种构象出现,表明辅因子在最终定位前会探索多种位置。到1.2秒,一些这些特征变得更清晰,呈现出占主导的结合模式,但总体图景仍是灵活且仅部分占有的相互作用。这种不均匀、不断变化的行为与早期生化证据一致:NQO1二聚体中的两个亚单位并非完全同步,而是表现出“半位点”活性——一侧先参与,另一侧随后跟进。时间分辨数据因此提供了这种不对称性在真实空间中如何展开的早期结构见解。
在保持科学性的同时节省样品
从实际角度看,与在相似条件下的传统连续喷流相比,分段液滴方法在0.3秒测量中将蛋白使用量约减少了六倍,在1.2秒实验中最多减少了97%。同时,它仍在室温下提供可靠的结构信息,并与欧洲XFEL严格的脉冲结构兼容。对非专业读者而言,结论是研究人员现在可以用每个时间点仅毫克级的珍贵样品近实时观察像NQO1这样的酶如何开始其工作。这使得在更多反应时间点和多种蛋白上开展调查变得更加现实,最终有助于揭示医学重要酶在执行生命化学反应时如何移动、弯曲并协同工作。
引用: Doppler, D., Grieco, A., Koh, D. et al. Minimized sample consumption for time-resolved serial crystallography applied to the redox cycle of human NQO1. Commun Chem 9, 107 (2026). https://doi.org/10.1038/s42004-026-01908-9
关键词: 串行晶体学, X射线自由电子激光, 液滴微流控, 酶动力学, NQO1