Clear Sky Science · zh
致癌性 PI3Kα 变体揭示具有突变特异性隐匿口袋的分级构象谱
当单一 DNA 变化不足以说明问题时
癌症常被描述为一种突变性疾病,但这项研究表明并非所有突变都是单独发挥作用。研究人员研究了一个关键的生长调控酶 PI3Kα,发现当两个特定的 DNA 变化同时出现在同一基因拷贝中时,它们可以将该蛋白推向比任一单独变化更具活性的构象。这很重要,因为过度活化的 PI3Kα 不仅推动癌症发展,还参与良性增生综合征和脑发育疾病——也有助于解释为何一些肿瘤对现有药物反应不佳。
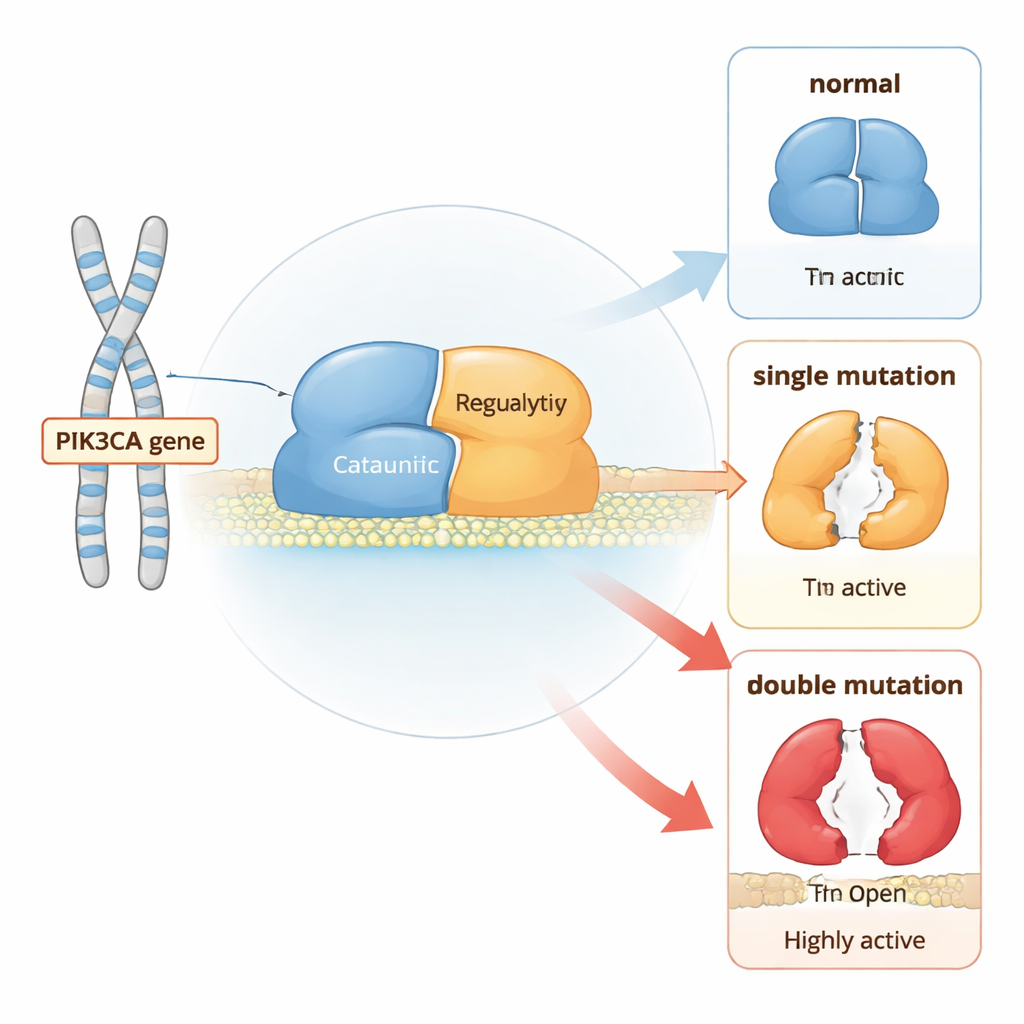
细胞生长的分子开关
PI3Kα 是一个位于细胞膜附近、负责传递生长信号的双组分蛋白。在正常情况下,它大多处于“关闭”状态,直到细胞表面的受体受到刺激。随后,PI3Kα 移动到膜上,将一种称为 PIP2 的脂质转化为 PIP3,后者指示细胞生长和分裂。为防止失控生长,蛋白的若干部分充当内置制动器:一段结构夹住催化核心,另一段将一条柔性激活环保持靠近,且一个伴侣亚基有助于抑制整个复合体的活性。
单突变与双突变如何倾斜平衡
作者利用长期的原子级计算模拟,将正常的 PI3Kα 与携带单个“热点”癌变突变或在同一分子中携带热点与更弱突变组合的变体进行了比较。他们发现每种突变都会改变蛋白访问更开放、活性构象的频率,但双突变比单突变把这种平衡推得更远。尤其是,某些突变对能协同松动将一个调控片段(称为 nSH2)固定在原位的接触,并使另一个片段(iSH2)远离其对接位点。这种协调的运动解开了催化核心,使蛋白更容易移向膜并开始信号传递。
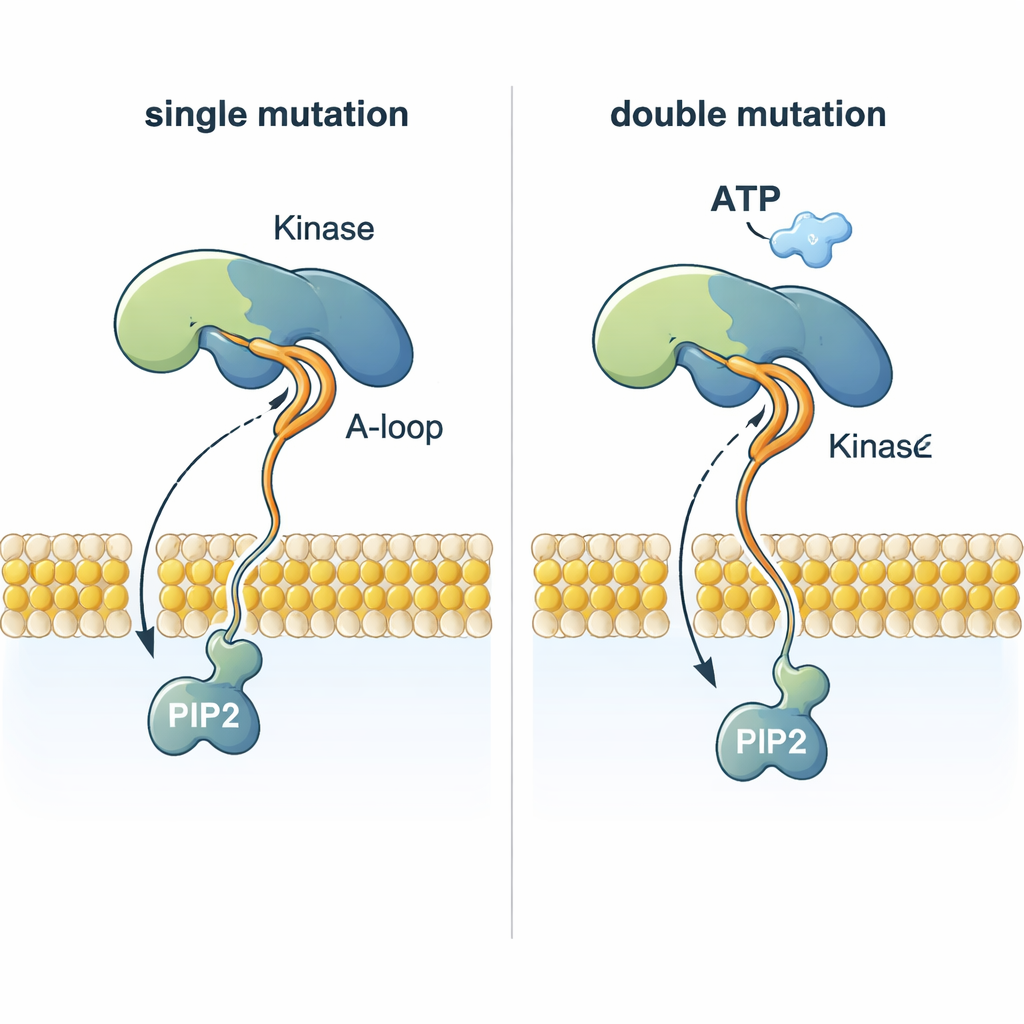
帮助底物到达反应位点
一个引人注目的难题是 PI3Kα 如何将来自 ATP 的磷酸基(ATP 位于距膜近 2 纳米处)加到嵌入膜中的 PIP2 上。模拟显示,某些突变重塑了柔性激活环,使一段高度带正电的序列向膜突出。该环可以抓住带负电的 PIP2 头基,将其从脂质层中拉出,并引导其向 ATP 移动。将锚定膜的突变与改变该环的突变结合的双突变,比正常 PI3Kα 或单突变体更高效地协调 PIP2,这为为何携带两处 PI3Kα 突变的肿瘤可能尤其具有侵袭性提供了结构学解释。
由运动揭示的隐匿药物位点
由于 PI3Kα 体积大且柔性强,单一针对其活性位点的药物常常难以在所有突变形式中发挥作用,并可能引起如严重血糖变化等副作用。通过追踪蛋白随时间的呼吸和弯曲,研究人员发现了“隐匿”口袋——仅在某些突变构象下短暂打开、在静态晶体结构中看不到的沟槽。这些口袋出现在突变特异性的位置,例如靠近在特定双突变中运动最强的区域。这表明经过精心设计的变构药物——结合在活性位点之外——可以被定制用来将个别突变体锁定回更安全、活性较低的构象。
迈向更聪明的组合治疗
总体而言,这项工作支持一种“二击”式的癌症遗传学观点:一个强效的热点突变加上同一 PI3Kα 分子中的一个较弱伙伴,可以产生一个更活跃构象的分级谱,这常与更严重的临床结局相关。对于治疗,作者认为,与其依赖单一抑制剂,不如将靶向不同口袋的药物组合起来——一个针对活性位点,另一个或多个针对仅在特定突变体中存在的变构位点。这样的药物组合原则上可以更精确地降低 PI3Kα 活性,减少毒性副作用,并更好地将治疗匹配到患者肿瘤中的确切突变模式。
引用: Jang, H., Yavuz, B.R., Zhang, M. et al. Oncogenic PI3Kα variants reveal graded conformational spectrum with mutation-specific cryptic pockets. Commun Chem 9, 100 (2026). https://doi.org/10.1038/s42004-026-01906-x
关键词: PI3K alpha, 致癌突变, 变构抑制剂, 分子动力学, 信号转导