Clear Sky Science · zh
用于靶向胶质瘤治疗的四重共轭碳点纳米模型的开发
顽固性脑肿瘤的新希望
像胶质母细胞瘤这样的高等级脑肿瘤是最难治疗的癌症之一。许多在体内其他部位有效的药物要么无法穿过大脑的保护性血脑屏障,要么在过程中损伤健康组织。本研究描述了一种在实验室构建的“智能”纳米颗粒,旨在更精确地进入脑肿瘤,携带强效药物组合,并在肿瘤细胞核内直接释放,从而在尽量保护正常细胞的同时,对癌细胞造成最大破坏。
由碳构成的微小运输车
这一新方法的核心是碳点——纳米尺度的碳颗粒,生产成本低、易于水相分散,并在特定光照下会发光。由于其表面含有丰富的化学“挂钩”,可以同时修饰多种生物成分。在这项工作中,研究者设计了一种“四重共轭”纳米模型:每个碳点在一次单锅反应中化学连接了两种不同的靶向肽和两种抗癌负载物。这种模块化设计使每个碳点成为一个微小的运输车,能够识别肿瘤细胞、穿越细胞屏障并将药物运送到正确的细胞内位置。
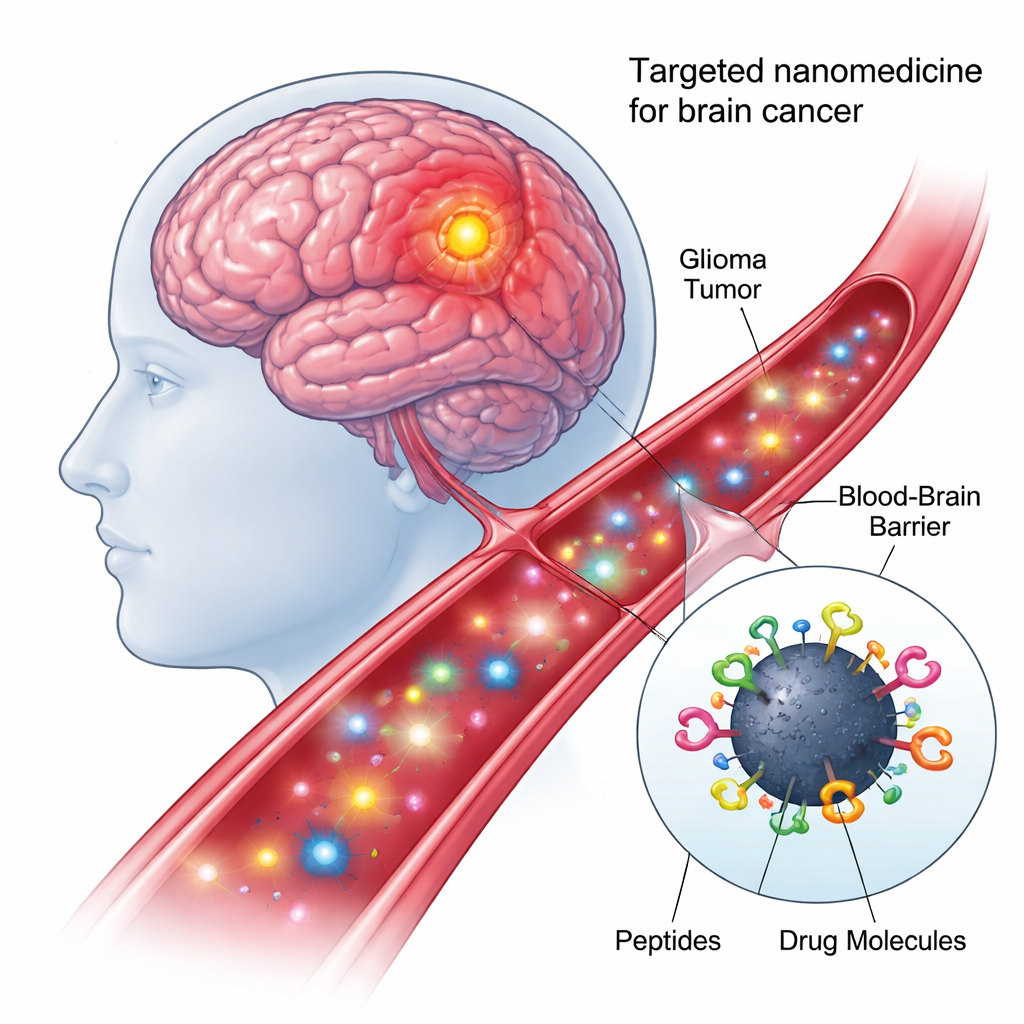
寻找并进入正确的脑细胞
纳米颗粒上的第一个肽称为 shPep-1,旨在识别名为 IL13Rα2 的受体。该受体在许多侵袭性脑肿瘤(包括成人与儿童胶质母细胞瘤以及弥漫性内桥脑肿瘤)上高表达,而在正常脑细胞上表达较弱。通过结合 IL13Rα2,shPep-1 帮助碳点定位并通过受体介导摄取进入肿瘤细胞。第二个较长的肽 lnPep-1 含有核定位信号:一段短序列,帮助货物穿过核膜到达存放 DNA 的细胞控制中心。两种肽结合在一起,使纳米颗粒既具有肿瘤选择性,又能在进入细胞后抵达细胞核。
递送协同药物攻击
治疗负载由两种小分子组成。第一种是表阿霉素(epirubicin),这是一种已知的化疗药,通过插入 DNA 并阻断修复双链断裂所需的酶来杀伤癌细胞。第二种是代谢物 5-氨基咪唑-4-羧酰胺(AIC),在生理 pH 下由脑肿瘤药物替莫唑胺产生。在早期工作中,同一团队已显示将表阿霉素和 AIC 组合在碳点上相比单一药物能够增强对癌细胞的杀伤效果。在新的设计中,两者都在双肽纳米颗粒上共同递送,旨在肿瘤细胞核内实现协同效应。
对肿瘤细胞强效、对正常细胞更温和
为了测试该纳米模型的效能,团队将多种高等级胶质瘤细胞系——成人胶质母细胞瘤、儿童胶质母细胞瘤以及弥漫性内桥脑肿瘤模型——暴露于四重共轭的碳点中。即使在非常低的浓度(低至 50 纳摩尔)下,肿瘤细胞活力也降至未处理对照的大约一半;在更高剂量时,所有测试的共轭物几乎杀死了大多数肿瘤细胞。值得注意的是,四重纳米模型的表现优于更简单的“单肽”版本,即便其总体携带的表阿霉素更少。在对非癌性血管平滑肌细胞的测试中,其毒性显著降低:这些细胞需要约 25–40 倍更多的纳米颗粒才出现类似的活力丧失,提示通过肿瘤靶向而非简单增剂量,存在一个有用的安全窗。
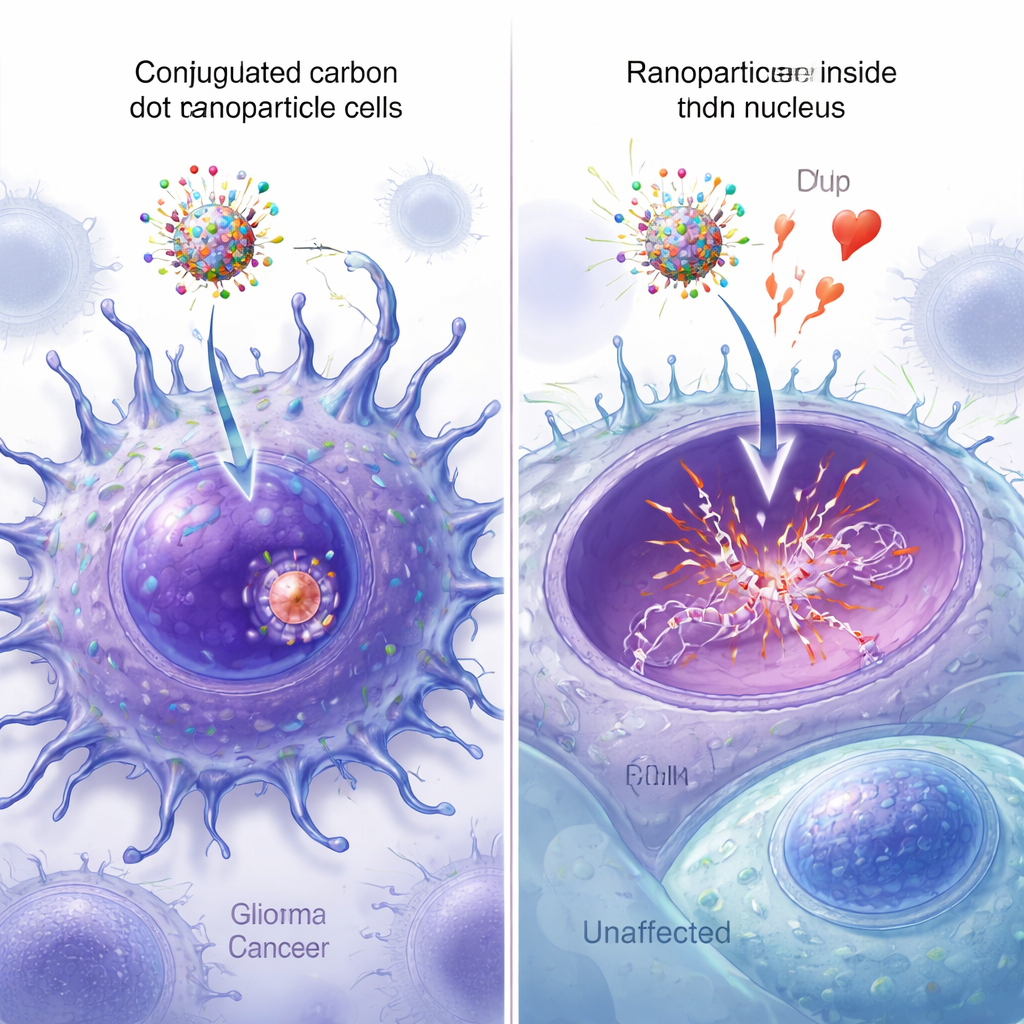
观察纳米颗粒到达细胞核
荧光标记的纳米颗粒使研究者能够观察每种设计进入细胞并到达细胞核的情况。在显微镜下,同时携带两种肽的碳点在癌细胞内显示出最强的信号,绿色纳米颗粒荧光与蓝色核染色有明显重叠。定量图像分析证实,双肽颗粒具有最高的核共定位度,显著高于仅携带一种肽或不携带肽的颗粒。额外的光谱学、质谱和原子力显微镜测量验证了所有四种成分已成功连接到碳点上,并适度增大了其尺寸,同时未破坏表阿霉素的关键 DNA 结合功能。
这对未来脑癌治疗意味着什么
对患者而言,这些发现仍属于早期的细胞水平证据,而非可立即使用的疗法。但它们展示了一个有前景的概念:一种小巧、稳定且相对易于制备的碳基纳米颗粒,可快速用靶向肽和药物组合进行定制。通过将药物专门引导至过度表达 IL13Rα2 的肿瘤细胞并在细胞核内浓缩,此类纳米药物未来或可实现更低剂量、更少副作用以及针对高度致命性脑肿瘤(如胶质母细胞瘤和弥漫性内桥脑肿瘤)的更个性化治疗策略。
引用: Cilingir, E.K., Hettiarachchi, S.D., Rathee, P. et al. Development of a quadruple-conjugated carbon dot nanomodel for targeted glioma therapy. Commun Chem 9, 96 (2026). https://doi.org/10.1038/s42004-026-01900-3
关键词: 胶质母细胞瘤, 纳米医学, 碳点, 靶向药物递送, 脑肿瘤