Clear Sky Science · zh
钒化合物与人血清运铁蛋白反应后形成加合物的首个晶体结构
为什么血液蛋白和金属药物很重要
许多实验性药物包含可用于治疗从糖尿病到癌症等疾病的金属原子。但这些基于金属的药物一旦进入血液,就必须依赖体内的天然运输蛋白进行转运。本研究考察了其中一种蛋白——人血清运铁蛋白(我们血液中运输铁的主要载体)——与一种有前景的钒化合物的相互作用,揭示了金属药物如何在体内被携带,以及如何通过这些机制对药物进行更安全、更有效的优化。
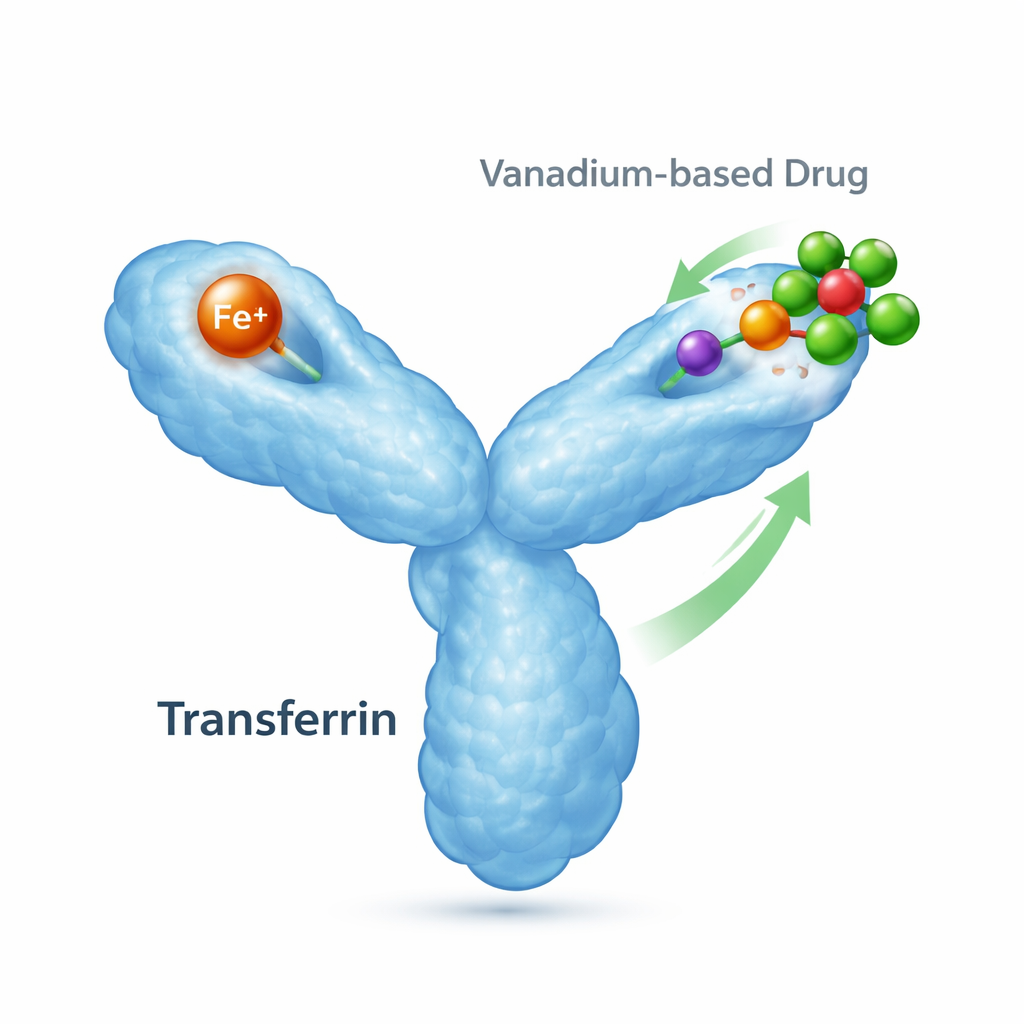
体内的铁运输者及其额外“兼职”
运铁蛋白是一种约80千道尔顿的蛋白,其主要功能是结合铁并将其输送到需要的细胞。它具有两个“叶”,每个叶可结合一个铁离子,并会根据是否结合铁而改变构象。结合铁时,叶片闭合;没有铁时则保持打开。细胞表面的专门受体能识别这些载铁形式并内化它们,使运铁蛋白在铁稳态和细胞健康中至关重要。然而,运铁蛋白也能结合其他金属,包括来自药物治疗的金属,这意味着它可能影响基于金属的药物的分布和作用方式。
钒在运铁蛋白上的形态快照
研究人员聚焦于一种研究较多的钒候选药物:双(乙酰丙酮)氧代钒(IV),常写作 [VIVO(acac)₂]。早期工作表明该化合物或其在水中衍生的物种可以附着于运铁蛋白,但没人确切看到其结合方式。利用X射线晶体学,团队获得了高分辨率的运铁蛋白结构,样品仅在C端叶片携带铁(“FeC”形式),并在暴露于钒药物前后进行了比较。在经钒处理的晶体中,他们观察到的不是原始药物分子,而是一个转化后的钒-氧簇,结合在不含铁的N端叶片上。这为钒片段附着于人运铁蛋白提供了首个直接的结构影像。
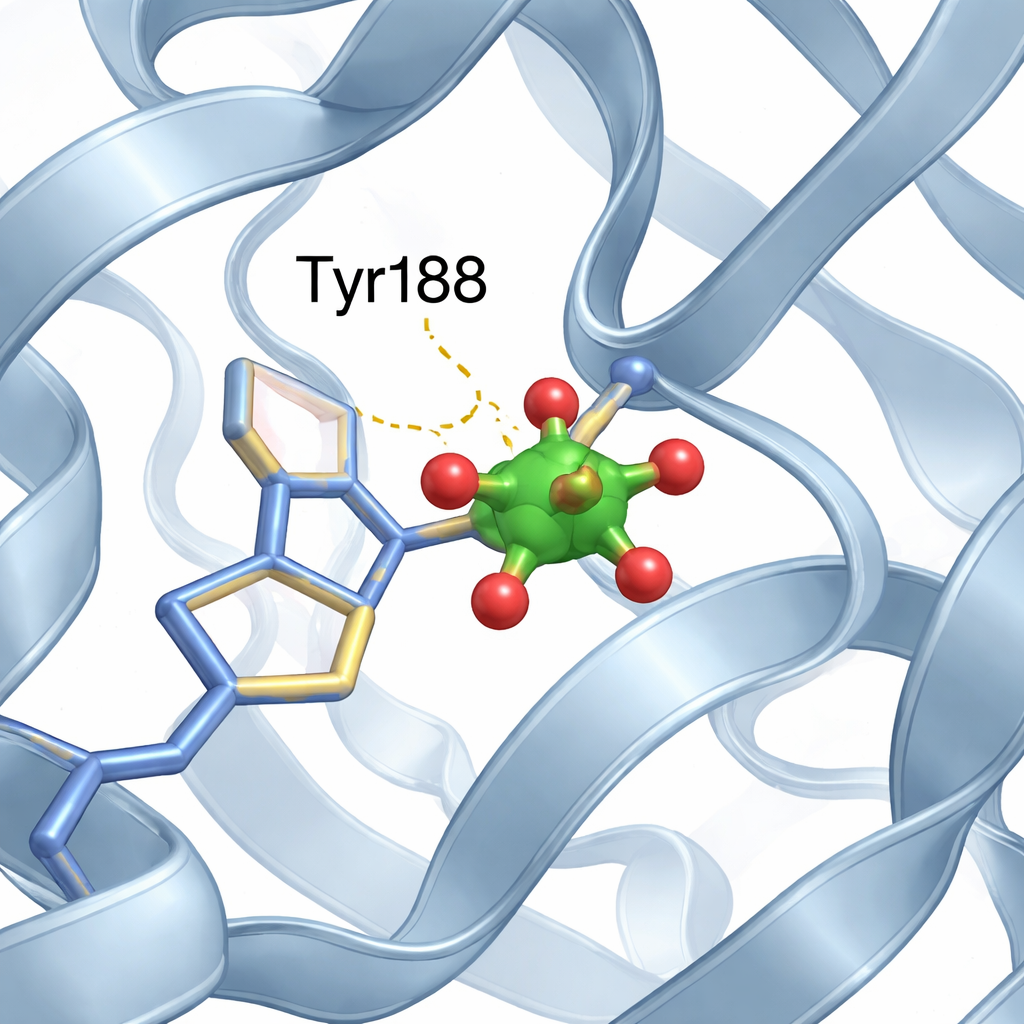
一个微小的钒簇找到归宿
在N端叶片的铁结合位点内,研究组鉴定出一个由两个钒原子和氧原子组成的小簇,最佳描述为修饰过的“二钒酸盐”单元。该簇的一个氧位置被来自特定氨基酸——酪氨酸188(Tyr188)的氧占据,形成了蛋白与金属簇之间的直接键。附近蛋白片段提供的氢键等温和相互作用进一步稳定了该簇。重要的是,尽管这个新的金属客体占据了铁结合口袋,整个蛋白仍保持其常见的开放N端叶片和闭合C端叶片构象,与无钒的结构几乎相同。
运铁蛋白如何重塑钒的化学形态
在用于晶体化的pH和浓度下,晶体中观察到的这种双钒物种在溶液中通常只是次要组分;更大的钒-氧簇往往占优势。光谱测量和理论配分计算表明,原始钒药物在水中会缓慢被氧化并分解,产生简单的钒酸根离子,这些离子随后组装成多种簇。晶体结构表明,运铁蛋白选择性地稳定了这种小型的类二钒酸盐片段而非更大的簇,实质上通过在Tyr188处提供一个贴合的结合位点和支持性的氢键网络,从混杂的溶液物种中“挑选”出一种化学形态。
保持与细胞受体的“握手”
由于运铁蛋白必须与细胞表面的受体结合以输送铁,研究人员探究将该钒簇附着是否会破坏这一关键的互作。通过非变性凝胶电泳和一种称为生物层干涉的灵敏技术,他们测量了经钒处理的运铁蛋白与运铁蛋白受体的结合能力,并与未处理仅含铁的形式比较。两者的表现几乎相同,均在低纳摩尔范围内表现出很强的结合力。这确认了尽管钒簇嵌入N端叶片,但并未显著改变运铁蛋白与受体相互作用处的构象,因此不应妨碍细胞识别该蛋白。
这对基于金属的药物意味着什么
对非专业读者而言,结论是:本研究提供了一个分子层面的快照,显示了钒药物衍生物如何附着在体内主要的铁运输蛋白上,而不破坏其正常功能。运铁蛋白能在铁位点捕获特定的小型钒-氧簇,但蛋白的整体形状及其与受体结合的能力基本保持不变。这有助于解释钒类药物可能如何以与运铁蛋白结合的形式循环,并强调不同蛋白可能偏好不同尺寸的钒簇。此类见解对于设计能够预测并控制其在血流中行为——形成何种物种、去向与稳定性——的更智能的基于金属的疗法至关重要。
引用: Banneville, AS., Lucignano, R., Paolillo, M. et al. First crystal structure of an adduct formed upon reaction of a vanadium compound with human serum transferrin. Commun Chem 9, 89 (2026). https://doi.org/10.1038/s42004-026-01891-1
关键词: 钒类药物, 人血清运铁蛋白, 基于金属的治疗剂, 蛋白-金属结合, 结构生物学