Clear Sky Science · zh
内酰胺促使硼酸酯远程重排生成C═N键
构建类药分子的全新捷径
化学家不断寻求更快、更清洁的方法来合成药物和高性能材料中的复杂分子。该研究提出了一种巧妙的捷径:一种常见的环状结构——内酰胺——可暂时引导反应然后悄然退出,使得利用简单、易得的原料在不借助昂贵金属或复杂预处理的情况下,直接生成对制药有价值的构建块成为可能。
将“沉默的帮手”变成短时引导者
许多现代药物和功能性材料依赖硼酸的反应,这类含硼化合物因可靠且反应温和而备受青睐。传统上,要促使硼酸与碳–氮双键(C=N)形成新键,化学家通常需要在起始物上预先安装特殊的“定向基”。这些基团像把手一样引导反应,但增加了时间、成本和步骤,并且常常只在高度活泼的底物上有效。作者意识到,内酰胺——与蛋白质中常见的酰胺相近的环状结构——可以作为内建的、短暂的引导基。通过与硼原子配位,内酰胺中的氧有助于形成高度有序的四配位硼中心,使得连接在硼上的片段能够沿分子远程重排,建立新的碳–氮键而无需任何永久性的定向基。
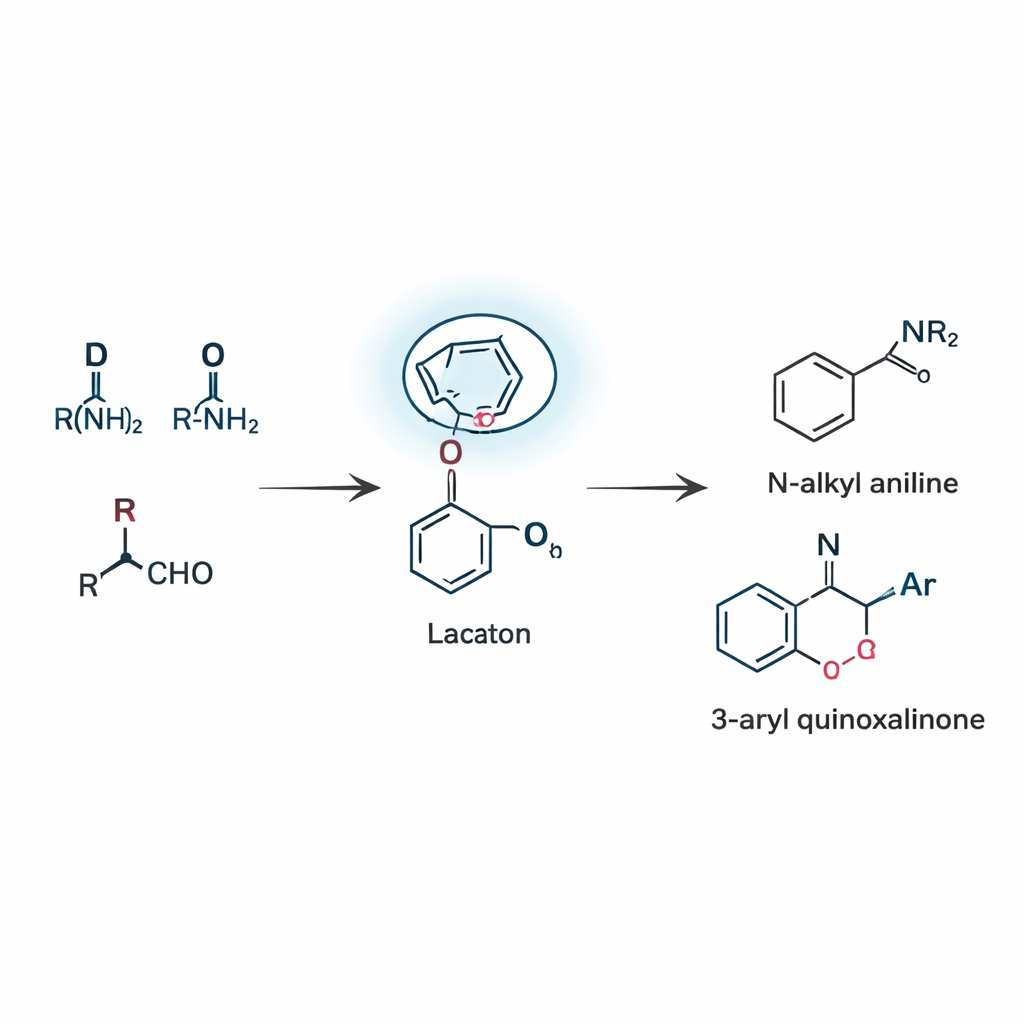
一套策略构建两类有用产物
基于这一概念,团队开发了两种相关反应,都依赖这种内酰胺引导的重排——即远程硼酸酯重排。在第一类反应中,三种简单组分——醛、胺和硼酸——组合形成N-烷基苯胺,这是一种在无数候选药物和染料中出现的核心结构。该反应通过一种罕见的1,5位迁移实现,其中硼上的芳基跨越五个原子到达C=N键位。通过精细调节催化剂、溶剂和温度,研究者获得了可观的产率,并展示了多种取代基(包括卤素、烷基和杂环)均具有良好耐受性。在第二种反应模式中,相同的引导思路应用于喹喔喃酮——一类富含氮的环系,常见于药物化学。这一体系完全不需要外加金属催化剂,仍能高效产生3-芳基喹喔喃酮,得益于内酰胺与硼的相互作用以及对关键中间体的稳定作用。
绿色条件与药物的晚期修饰
除了展示广泛的适用性外,作者还证明该策略对实际分子具有可行性。因为在喹喔喃酮上的1,4-重排在金属自由的条件下于特定醇类溶剂中进行,它避免了使用昂贵或有毒的过渡金属。团队将该方法应用于来源于已上市药物(如布洛芬)及其它含喹喔喃酮骨架的复杂片段。在每一例中,反应都能在特定位置引入新的芳基而不破坏其它敏感官能团。这类“晚期功能化”让化学家能够快速地在现有药物核心上引入新的侧链,加快寻找更高效、更安全或物性更佳的候选分子的过程。
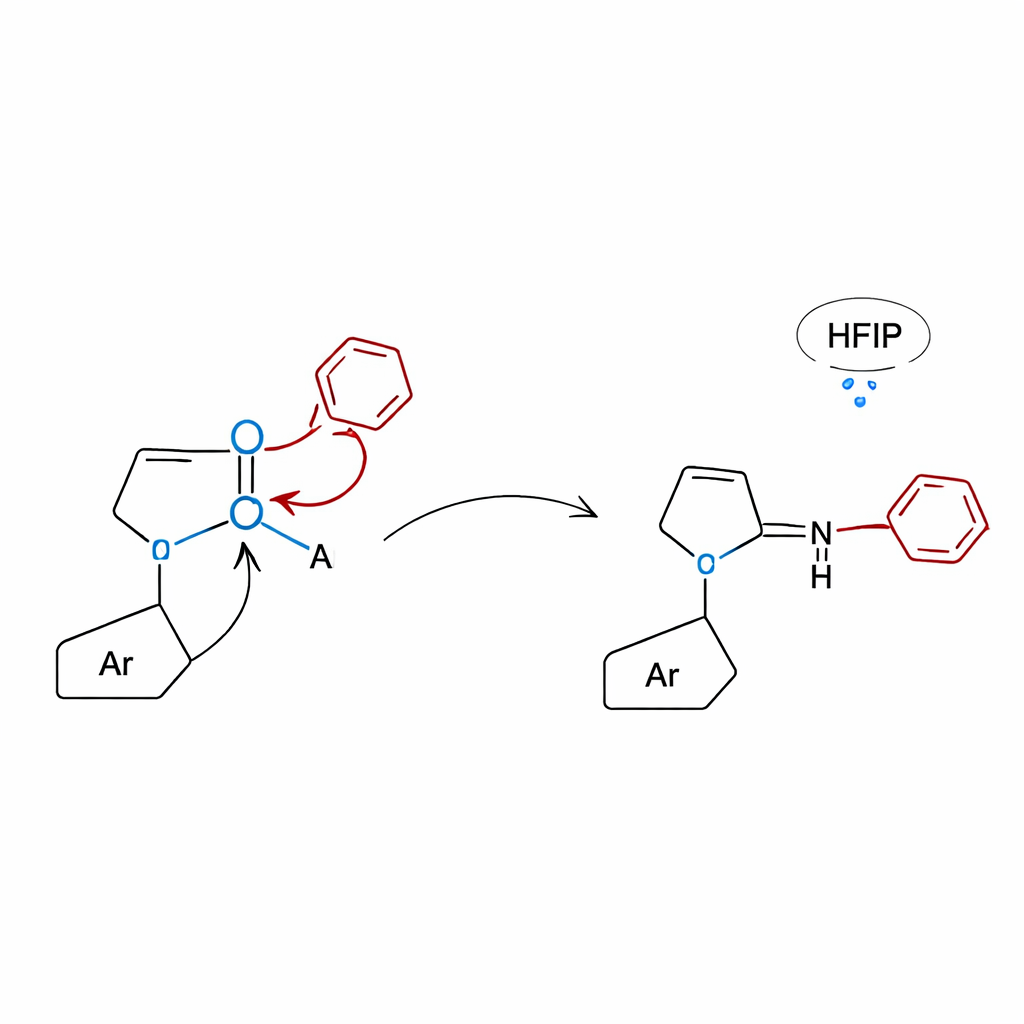
用理论与对照实验揭示机理
为了弄清内酰胺策略为何如此有效,研究者将精心设计的对照实验与计算机模拟相结合。当测试不含内酰胺基团的分子时,反应基本失活,证实内酰胺环对于活化硼酸并引导重排是必不可少的。量子化学计算显示,内酰胺的氧与硼结合形成紧凑的四配位结构,从该结构中芳基可以发生跨五个原子的迁移(1,5-迁移)生成N-烷基苯胺,或跨四个原子的迁移(1,4-迁移)生成3-芳基喹喔喃酮。在喹喔喃酮的案例中,HFIP(六氟异丙醇)溶剂所提供的氢键网络进一步降低了能垒,帮助反应在相对温和的热条件下无需任何外加催化剂即可进行。
对未来药物研究的意义
总体而言,这项工作表明,一个简单的内酰胺环可以作为一种动态且可回收的引导基,开启硼酸化学中此前难以实现的键形成模式。对非专业读者而言,关键信息是:化学家现在拥有一种更直接、高效的方法,将基础构建块转化为两类重要的含氮分子,这些分子是许多药物的基础。由于该方法避免了贵金属、耐受多种官能团并可用于复杂类药结构,它有望简化未来药物乃至潜在新型农用化学品的设计与优化流程。
引用: Lei, J., Xu, J., Li, X. et al. Lactam enables remote boronate rearrangements to C═N bonds. Commun Chem 9, 88 (2026). https://doi.org/10.1038/s42004-026-01890-2
关键词: 硼酸, 内酰胺化学, C–N键形成, 喹喔喃酮, 药物化学