Clear Sky Science · zh
基于同源推断的酶挖掘以多样化抗癌伊沃地啶骨架
把植物化学物质变成更好的药物
今天许多药物起源于植物的防御化学物质。这些天然分子常对癌症、感染或疼痛表现出强效,但它们很少是“完美”的药物。化学家希望精确调整这些分子的结构以提高安全性和疗效,然而这些分子通常极为复杂,即便是微小改动也很困难。本研究展示了科学家如何借助植物酶作为微小的分子工具,对一种名为伊沃地啶的抗癌化合物进行定点改造,从而可能开辟通向改良疗法的新途径。
为何这种植物分子重要
伊沃地啶是存在于一种用于传统中医的树果实中的天然化合物。它属于一类环状分子,这类骨架已构成某些用于癌症、高血压和感染的关键药物。伊沃地啶本身展现出抗癌、抗炎、镇痛和抗微生物活性,而其一些改造衍生物在作为多靶点抗癌先导化合物方面尤其有前景。挑战在于如何在这一拥挤的骨架上,于极其特定的位置引入新的化学“把手”(例如含氧基团),而不依赖苛刻试剂或多步合成工序。
让酶完成难做的化学反应
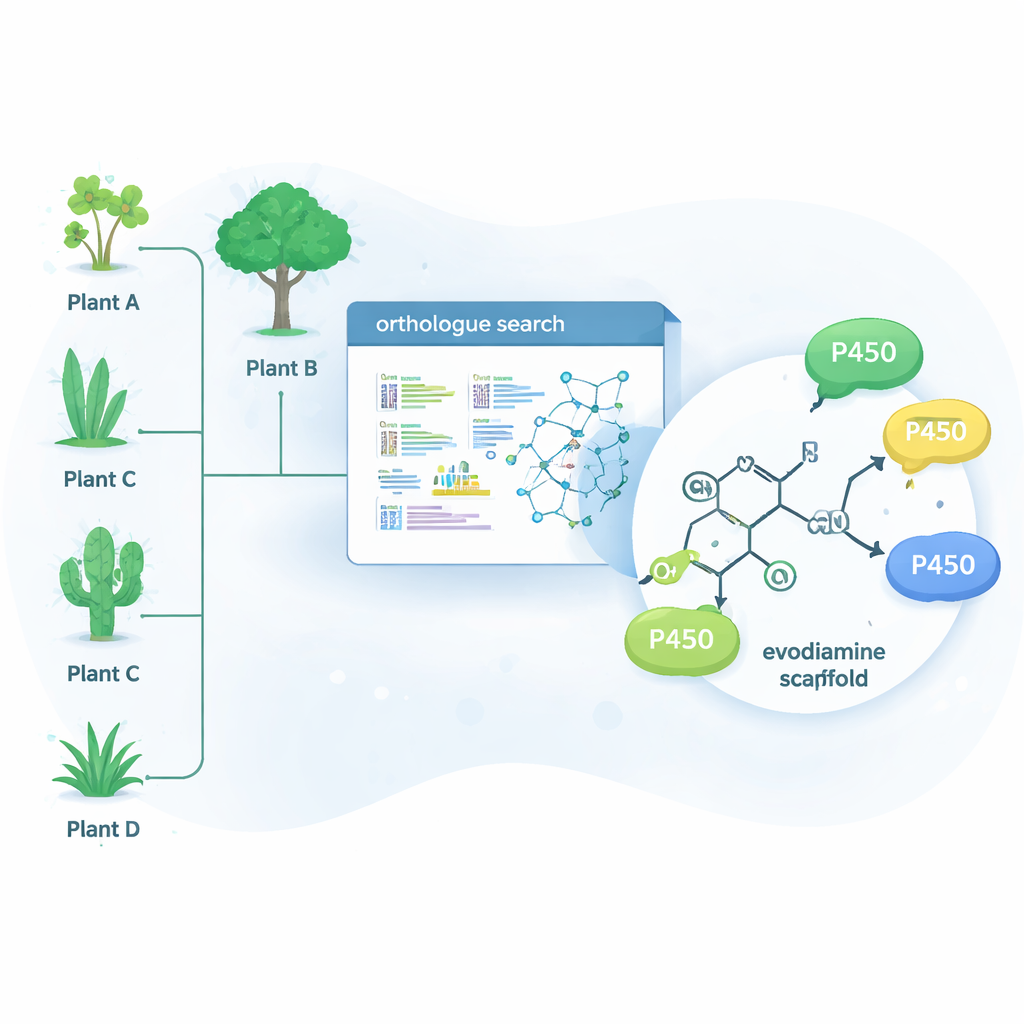
自然已经用酶——催化特定反应的蛋白质——解决了许多这类难题。其中一个大型酶家族,称为细胞色素P450,擅长在原本不活泼的碳—氢键上引入氧。仅一步氧化就能显著改变分子在体内的行为,也能为后续化学改造提供起点。研究者并未仅在天然产生伊沃地啶的植物中寻找,而是使用名为OrthoFinder的生物信息学工具,扫描15种生物碱产生植物的基因数据,寻找与已知生物碱改造酶密切相关的P450“直系同源物”。他们的推理是:这些酶的近亲可能同样能够微调相关的类药物分子。
在意想不到的植物中发现新酶
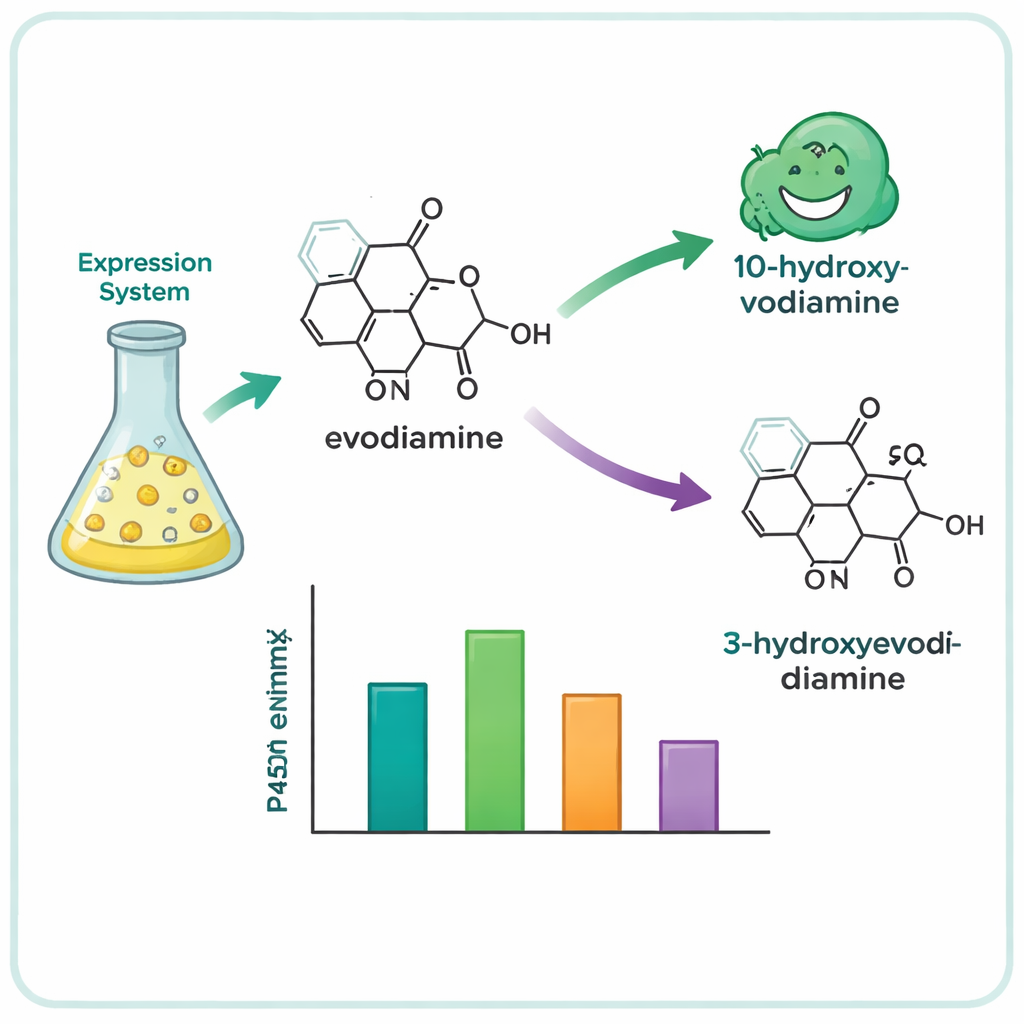
从数百个候选基因中,团队将名单缩减到15个有前景的P450,并在酵母细胞中表达这些酶,酵母作为微型酶工厂。接着他们向这些酵母提供一组复杂植物分子,分析哪些分子被化学改造。结果发现四种酶——三种来自喜树(Camptotheca acuminata),一种来自瑟伯纳莫塔那(Tabernaemontana elegans)灌木——能作用于伊沃地啶,尽管这两种植物并不以产生该化合物闻名。这些酶选择性地在伊沃地啶环系的两个位置之一插入一个氧原子,生成两种主要产物:10‑羟基伊沃地啶和3‑羟基伊沃地啶。这样的含氧衍生物比传统合成路线更易用温和化学方法进一步转化为水溶性或更高效的药物候选物。
窥探分子工具箱内部
为了解释这些密切相关的酶为何表现不同,研究者利用现代蛋白结构预测工具构建了最活跃酶及其近亲的三维模型。随后他们使用计算对接观察伊沃地啶如何位于酶的活性口袋中,靠近P450含铁中心的反应位点。模型突出了若干体积较大且疏水的氨基酸——尤其是苯丙氨酸残基——位于伊沃地啶芳香环附近。通过精细地突变这些位点,团队证明改变该口袋的尺寸和形状会削弱活性、改变底物的适配性,甚至将优先生氧化位点从分子的一个环切换到另一个环。在一例中,单一突变就使酶的产物偏好从10‑羟基产物翻转为3‑羟基产物。
这对未来药物意味着什么
对非专业读者而言,关键结论是作者展示了一条实用路线:发现并调谐能够对复杂类药分子执行精确“外科式”修饰的植物酶。通过结合大规模基因挖掘、酶学测试和结构建模,他们发现了一组生物催化剂,能够在传统化学难以触及的位置选择性地重塑伊沃地啶骨架。这不仅提供了一种更清洁、更可持续的方式来制造伊沃地啶的高级衍生物(例如水溶性抗癌先导),还表明有用的酶可以在并不生成目标化合物的植物中被发现。同样的策略现在可应用于许多其他天然产物,加速下一代植物来源药物的设计。
引用: Kwan, B.D., Kim, T., Nguyen, H.H. et al. Orthologue inference-based enzyme mining for diversification of the anti-cancer evodiamine scaffold. Commun Chem 9, 73 (2026). https://doi.org/10.1038/s42004-025-01876-6
关键词: 伊沃地啶, 植物酶, 细胞色素P450, 生物催化, 药物发现