Clear Sky Science · zh
ETV7通过CXCL1诱导的NETs形成促进结直肠癌对5‑FU的耐药性与恶性进展
这项研究为何重要
许多结直肠癌患者接受长期使用的化疗药物5‑氟尿嘧啶(5‑FU)治疗。对部分患者而言,该药起初有效,但随时间肿瘤寻得反击之策而失去疗效。本研究揭示了癌细胞与机体免疫细胞之间的一种隐秘“合作”,这种合作帮助肿瘤抵抗5‑FU,并指出了可能打破这一同盟、恢复药物效力的新途径。
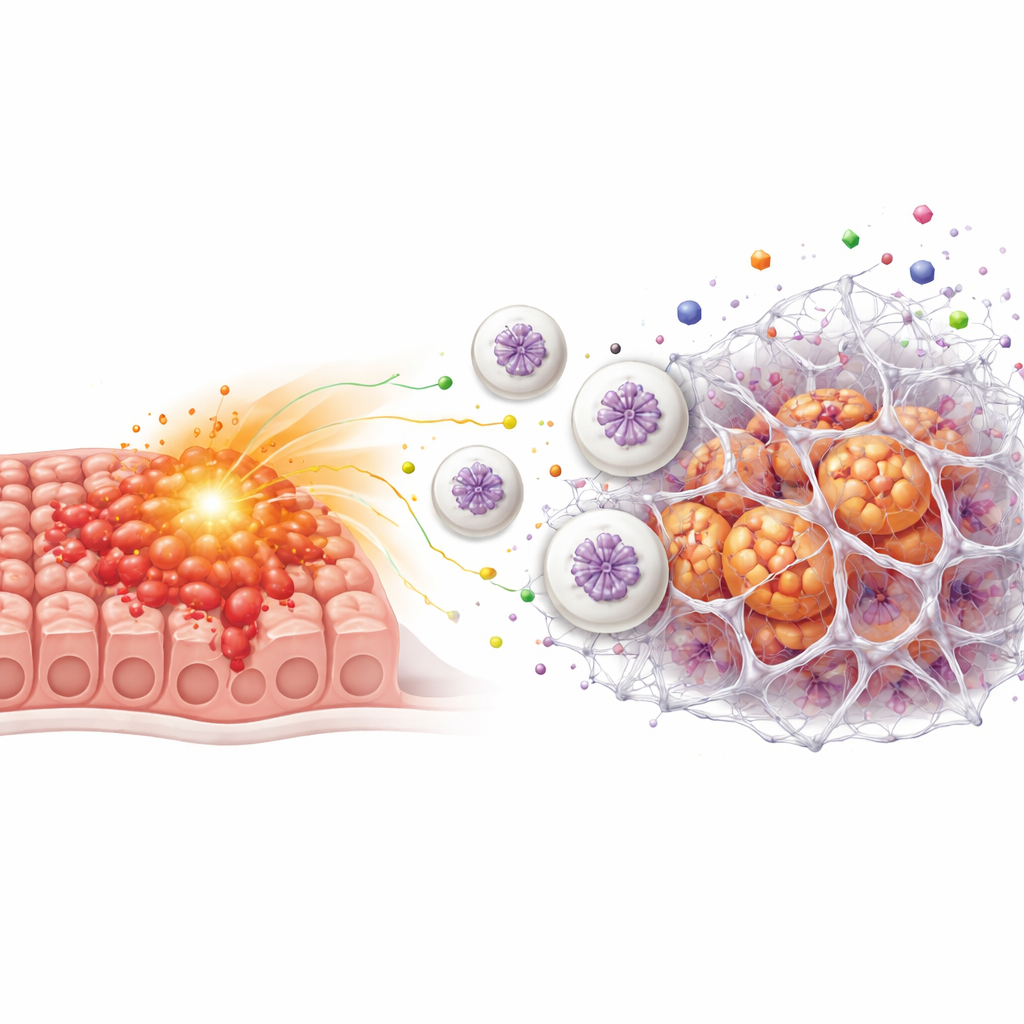
被过度开启的癌症“开关”
研究者聚焦于一种名为ETV7的蛋白,它是许多细胞类型中的基因调控开关。通过分析公共癌症数据库和患者组织样本,他们发现结直肠肿瘤中的ETV7水平远高于邻近健康组织。肿瘤中ETV7表达较高的患者总体生存期和无疾病生存期倾向较差,提示该蛋白与更具侵袭性的疾病相关。在体外培养的癌细胞中,提升ETV7使细胞更易分裂、迁移和侵袭;相反降低ETV7则抑制了这些恶性行为。
当培养皿误导结论时
令人好奇的是,当癌细胞单独在简单的塑料培养皿中生长时,改变ETV7水平并未明显改变它们对5‑FU的敏感性。然而在小鼠体内,经过基因改造过度表达ETV7的肿瘤在5‑FU治疗下仍持续生长。这一不一致提示,在体外培养皿中缺失但在生物体内存在的关键因素参与了这一过程:即血管、结缔组织和免疫细胞等组成的肿瘤微环境。
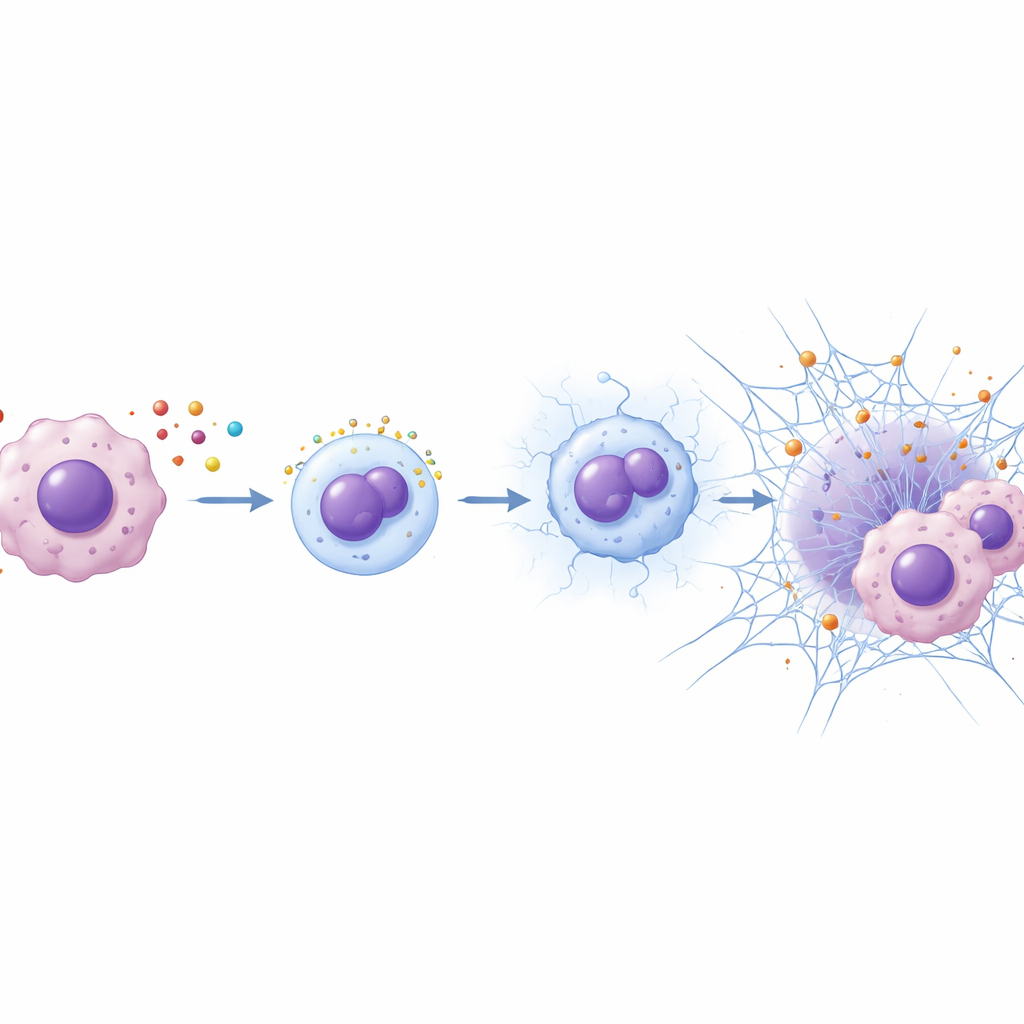
招募急先锋细胞构建粘性网状结构
团队接着探讨ETV7是否帮助肿瘤重塑其微环境。数据挖掘显示高ETV7与中性粒细胞浸润增多相关,中性粒细胞是一类以抵抗感染而著称的白细胞。在ETV7高表达的小鼠肿瘤中,更多中性粒细胞聚集在癌组织周围。将高ETV7的癌细胞与中性粒细胞共培养时,中性粒细胞显著促进了癌细胞的增殖、侵袭性及对5‑FU的耐受性。研究者将这一效应追溯到称为中性粒细胞胞外捕网(NETs)的网状结构——中性粒细胞通常抛出这些由DNA与蛋白构成的缠结以捕捉微生物。ETV7高表达的肿瘤中NETs更多,且来自ETV7高癌细胞的培养上清能在体外诱导中性粒细胞释放这些粘性网。
从肿瘤到中性粒细胞的信号链
ETV7如何说服中性粒细胞到来并织出这些捕网?基因分析指向CXCL1,一种小型可溶的信号分子,能作为吸引中性粒细胞的指引。本研究表明ETV7直接结合结直肠癌细胞中CXCL1基因的调控区并上调其表达。随着CXCL1水平升高,更多中性粒细胞被吸引到肿瘤并被激活。当阻断或降低CXCL1时,NETs形成减少,ETV7带来的肿瘤促进与药物耐受效应大多消失——尤其在中性粒细胞存在时。在接受5‑FU治疗的小鼠中,降低CXCL1、用抗体中和它或用酶分解NETs均能使ETV7驱动的肿瘤缩小,而联合阻断CXCL1与分解NETs的疗法效果最佳。
打破肿瘤的保护屏障
总体而言,这项工作揭示了结直肠癌中的ETV7–CXCL1–NETs轴:肿瘤细胞中的ETV7提升CXCL1,CXCL1招募并激活中性粒细胞,这些中性粒细胞释放NETs,形成一个围绕肿瘤的保护性促生长利基。该屏障帮助癌细胞在5‑FU治疗下生存与扩散。对患者而言,研究暗示检测ETV7或CXCL1可能有助于识别易产生耐药的肿瘤,并且旨在抑制CXCL1信号或NETs形成的药物可与标准化疗联合使用以提高疗效。
引用: Mo, S., Xia, P., Lv, Y. et al. ETV7 promotes 5-FU resistance and malignant progression through CXCL1-induced NETs formation in colorectal cancer. Commun Biol 9, 472 (2026). https://doi.org/10.1038/s42003-026-09976-2
关键词: 结直肠癌, 化疗耐药, 肿瘤微环境, 中性粒细胞胞外捕网, CXCL1信号