Clear Sky Science · zh
PACS1综合征突变通过HDAC6和BICD2破坏依赖动力蛋白的货物运输
这对大脑发育为何重要
PACS1综合征是一种罕见遗传病,会导致智力障碍、癫痫和明显的面部特征。家庭和临床医生熟悉这些症状,但直到最近,人们还不清楚患者细胞内部究竟发生了什么。该研究揭示了这一谜团,显示PACS1基因的单个字母变化如何扰乱细胞的内部运输系统,尤其是在神经元中,并说明这如何将PACS1综合征与更广泛的神经系统“交通”疾病家族联系起来。 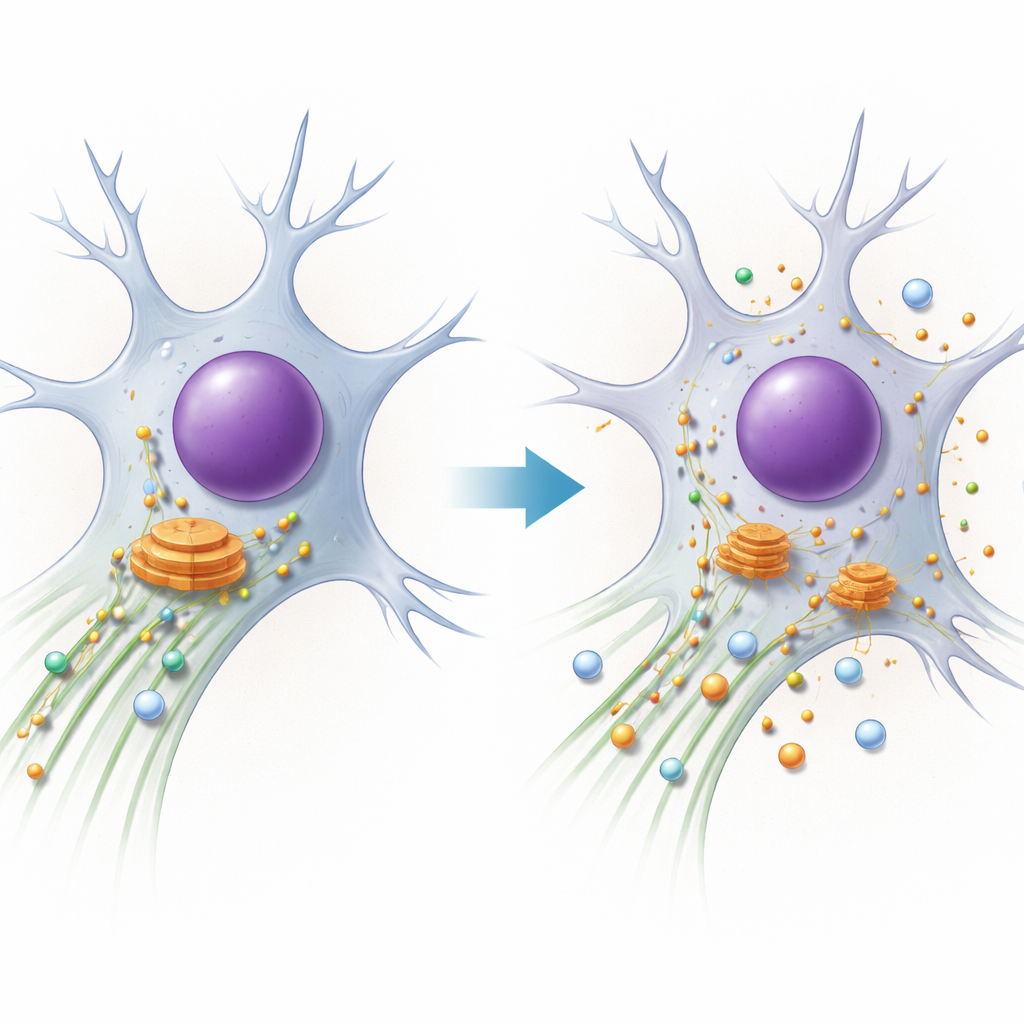
细胞的运输干道
每个细胞都依赖由蛋白质管状结构构成的微观“高速公路”,称为微管。分子马达沿着这些轨道行驶,运送酶和膜区室等货物到达所需位置。其中一种马达——动力蛋白(dynein)负责远距离的“回程”,将货物从细胞外围拉回到细胞中心的主要分拣站——高尔基体。作者将注意力集中在PACS1上,这是一种帮助选择哪些货物由动力蛋白运输的蛋白,并通过另一个蛋白HDAC6调节轨道状态,HDAC6控制微管上的一种化学标记(乙酰化)。神经元具有很长的突起,对这一系统的即便是微小故障也尤其敏感。
抓得太紧的突变协调子
PACS1综合征由PACS1基因中反复出现的R203W突变引起。研究团队发现,正常和突变的PACS1都能与动力蛋白的重链发生物理结合,但突变体结合得更紧。采用患者皮肤细胞和工程化细胞系,他们显示这种过度结合产生的后果类似于部分丧失动力蛋白功能:高尔基体解体为分散的小堆,高尔基体转侧通常定位的关键酶furin被错误地分流到其他区室。通过解析PACS1的结构,团队找到了一个短的β链“补丁”,该位点专门接触动力蛋白。当他们在不干扰PACS1其它功能的情况下改变这个补丁时,furin再次失去了正确位置,确认了动力蛋白–PACS1的握手对货物正确定位至关重要。 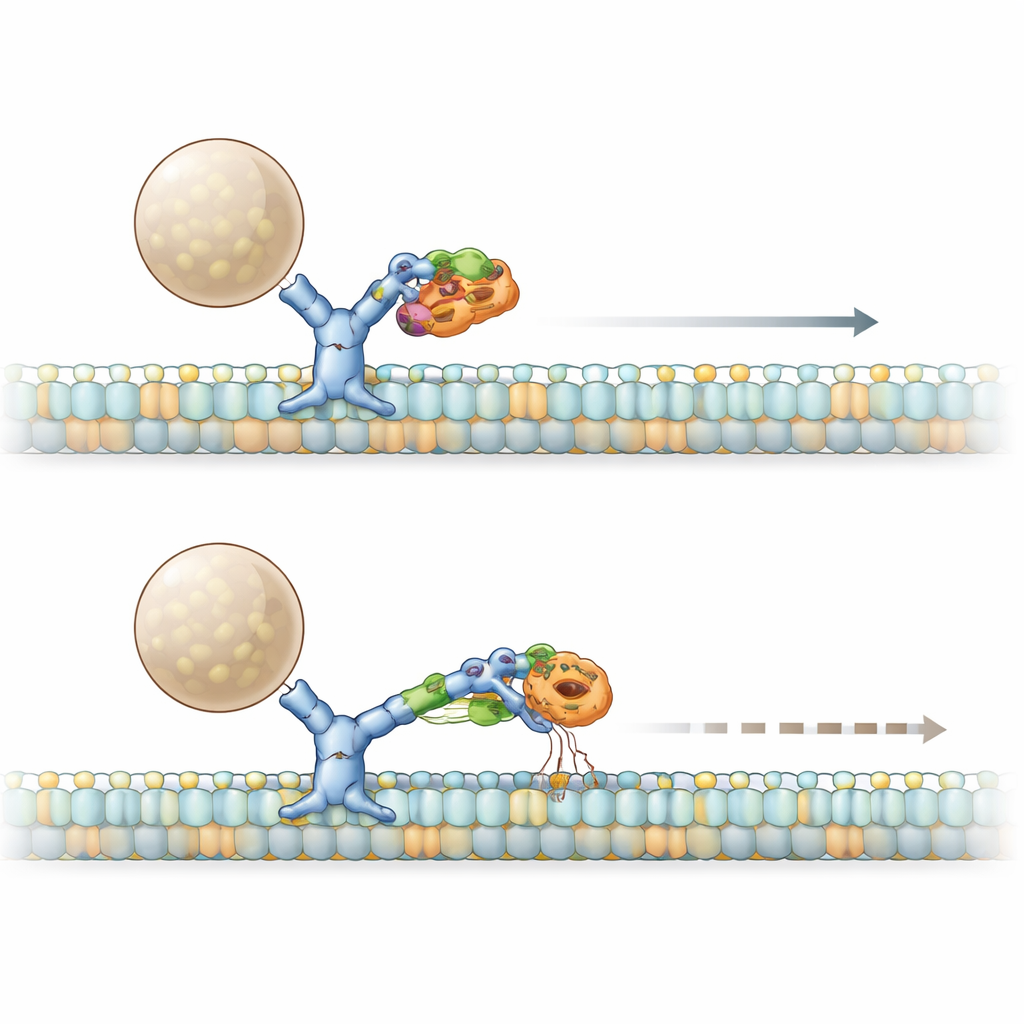
三蛋白联盟如何堵塞马达
故事更复杂地牵涉到另外两名玩家:HDAC6和一种名为BICD2的接头蛋白,后者有助于组装活性的动力蛋白复合体。突变的PACS1不仅增强了HDAC6的活性,降低了微管的乙酰化水平,还与HDAC6和BICD2形成了增大的复合体。生化检测显示,突变PACS1和HDAC6共同将BICD2从动力蛋白处撬开,同时保留了BICD2与向前行驶马达(驱动蛋白kinesin)的伙伴关系。在活细胞中,一个本应沿动力蛋白快速移动的人工货物在突变PACS1存在时减速,并且移动的货物数量减少。阻断HDAC6的活性能恢复速度和移动颗粒的数量,表明突变的PACS1–HDAC6–BICD2复合体像刹车一样抑制了动力蛋白启动和维持运输的能力。
用天然动力蛋白助手恢复运输
研究者接着测试是否能在突变复合体存在时“重新激活”动力蛋白。他们转向Lis1,这是一种已知的动力蛋白助手,可稳定活性马达装配。在患者细胞中,Lis1水平略有下降。当团队补充额外的Lis1时,有两方面得到了改善:高尔基体重新聚集到细胞中心附近,而先前外移的溶酶体等一类细胞器也恢复到位。在相同的运动测定中,Lis1在突变PACS1存在下提高了动力蛋白驱动货物移动的频率和速度。这些结果表明问题不是动力蛋白缺失,而是被困在一种低活性的状态——通过抑制HDAC6或加强动力蛋白激活,能部分纠正这种状态。
将一种罕见综合征与更广泛疾病相连
通过结构分析、细胞生物学和实时成像的结合,作者提出了一个清晰模型:PACS1通常将选定货物链接到动力蛋白,并通过HDAC6和微管乙酰化微调马达性能。R203W突变打开了PACS1的相互作用表面,过度招募HDAC6和BICD2形成一个削弱动力蛋白抓握微管并高效移动能力的复合体。其结果是在细胞内广泛错位高尔基体、溶酶体和其他货物,尤其是在长程运输至关重要的神经元中。这一机制有助于解释为何在小鼠模型中用反义寡核苷酸降低PACS1或HDAC6可以纠正大脑缺陷,并且这一策略现在正在患者中探索。更广泛地说,它将PACS1综合征置于日益增长的微管运输疾病谱系中,和由动力蛋白、BICD2及相关运输因子突变引起的病症并列。
引用: Yang, Y., Thomas, L., Chen, K. et al. PACS1 syndrome mutation disrupts dynein-mediated cargo transport via HDAC6 and BICD2. Commun Biol 9, 450 (2026). https://doi.org/10.1038/s42003-026-09924-0
关键词: PACS1综合征, 动力蛋白运输, 微管运输, 高尔基体组织, 神经元发育