Clear Sky Science · zh
脑膜炎奈瑟氏菌醌依赖型一氧化氮还原酶通过二聚化激活的结构基础
细菌如何智胜我们的免疫防线
当有害细菌入侵机体时,我们的免疫细胞会释放诸如一氧化氮等有毒分子以消灭它们。然而一些病原体已经进化出分子策略来中和这种攻击并存活下来。本研究以原子级细节揭示了一种关键细菌酶如何通过自我重构为二聚体,从而显著提升一氧化氮的解毒能力,并说明理解这种形变行为为何可能为抗生素设计开辟新途径。
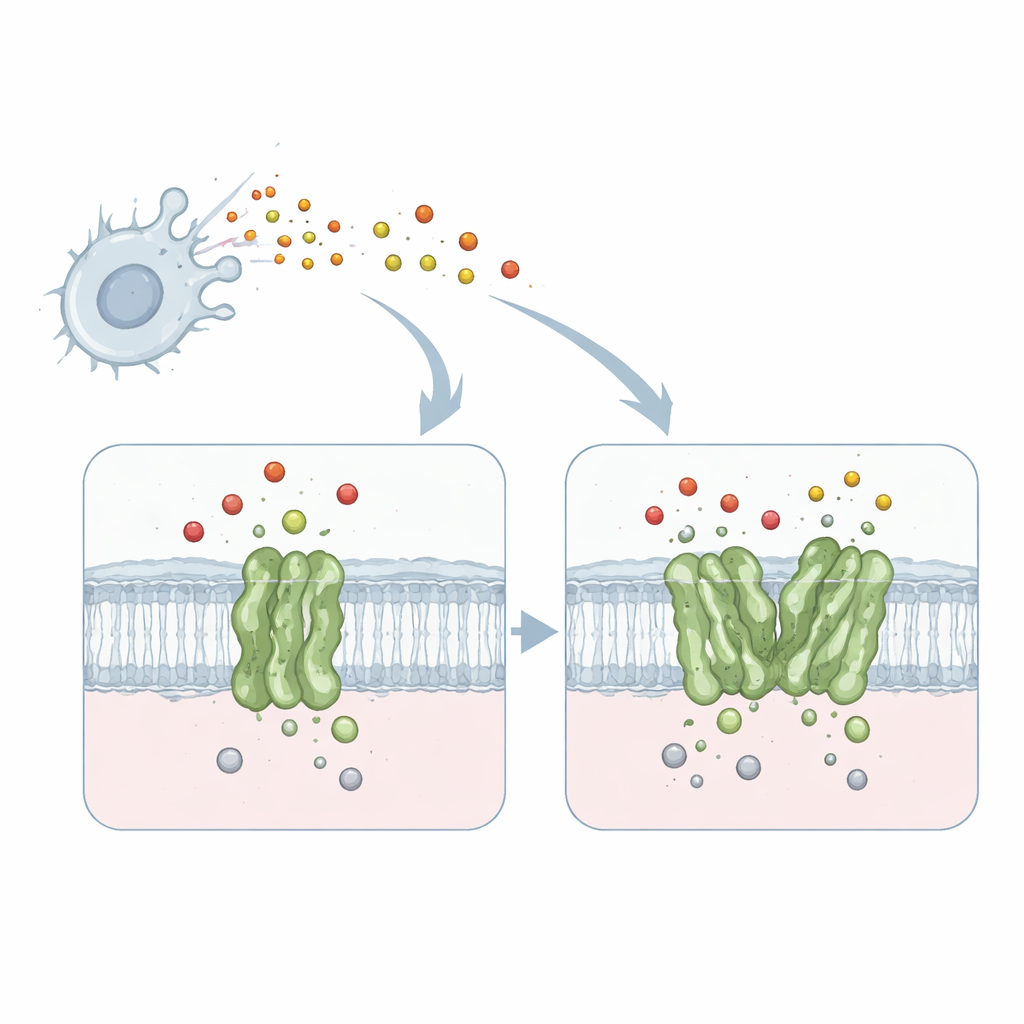
能够解除有毒气体的小型机器
该研究聚焦于一种位于膜上的蛋白——醌依赖型一氧化氮还原酶(quinol-dependent nitric oxide reductase,简称 qNOR),来自引发脑膜炎的细菌Neisseria meningitidis。qNOR 嵌入细菌细胞膜,将由我们免疫系统产生的一氧化氮这一有毒气体转化为危害较小的产物。这种解毒作用使微生物即便在像人类巨噬细胞等敌对环境中仍能维持呼吸和生长。由于呼吸和一氧化氮清除对病原体的存活至关重要,qNOR 因而成为有吸引力的新型抗菌药物靶点。
单体虽好,但二聚更优
先前的生化研究表明 qNOR 可存在为单个单元(单体)或成对存在(二聚体),且二聚体在中和一氧化氮方面的速率比单体高出两到四倍。此前尚不清楚为何仅仅将两个相同酶分子配对会对性能产生如此剧烈的影响。为了解答这一点,研究人员使用高分辨率单颗粒冷冻电子显微镜捕捉来自同一菌株的单体与二聚体 qNOR 的三维精细结构。他们获得了近原子分辨率的图像——二聚体为 1.89 埃,单体为 2.25 埃——清晰到可以定位到单个氨基酸侧链、金属离子以及大量水分子。
一段柔性螺旋变成稳定的支柱
出人意料的是,酶的催化核心——一氧化氮被转化的金属中心——在两种构象中几乎相同。关键差异出现在较远处,一段称为 TM10 的跨膜螺旋以及当两个 qNOR 分子配对时它如何与另一段螺旋(TM2)接触。在单体中,TM10 锚定较松,可大幅摆动和弯曲,这一点由对冷冻电镜数据的计算分析所揭示。在二聚体中,来自每个伙伴的 TM10 彼此抵靠形成四螺旋束,大大限制了其运动。这种稳定化细微地重新定位了一个关键氨基酸——名为 Glu563 的谷氨酸,使其靠近位于活性位点附近的另一谷氨酸(Glu494),从而塑造出更为集中且有利的质子引导通路。
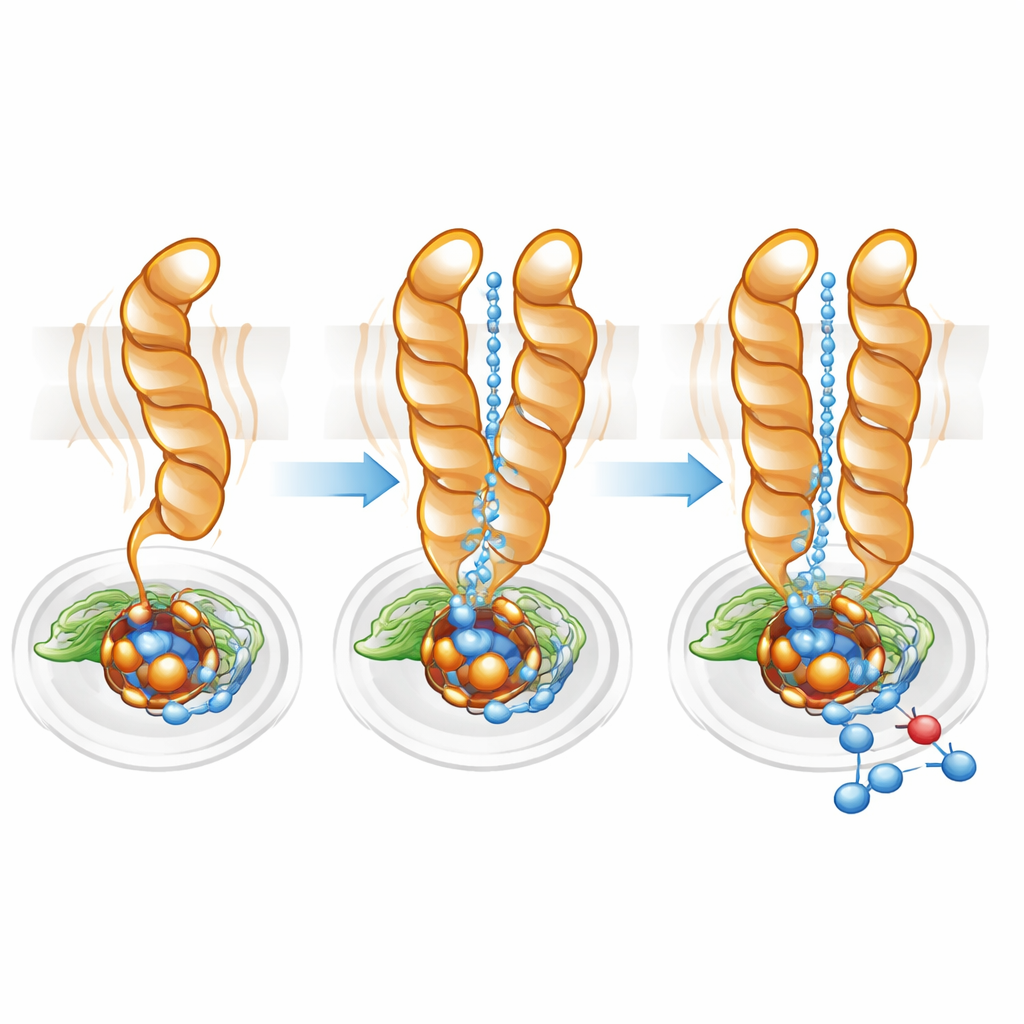
对质子通道的精细调控
质子——带正电的氢离子——必须有效地从细胞内部传送到埋藏的活性位点,才能使一氧化氮还原反应进行。利用通路映射软件,团队发现单体和二聚体中均存在一个将胞质与活性位点相连的亲水腔。然而在单体中该通道更宽、更分散,与 TM10 更大的可动性相一致。在二聚体中,TM10 的锁定位置和 Glu563 的有利取向有助于界定一条更直接、更有组织的通路。将 Glu563 突变为无法形成相同相互作用的氨基酸会使酶活性降至正常水平的 10% 以下,并且还会破坏二聚体的稳定性;而在相关位点的突变则减少了活性位点必需的非血红素铁含量。综合来看,这些结果表明二聚体形成以及 Glu563 与 Glu494 的精确定位与结构完整性和催化效率紧密相关。
将结构发现转化为新疗法
这些发现清晰地描绘出从膜表面蛋白配对到活性位点深处微调的全链路,这些调整共同控制 qNOR 清除一氧化氮的效率。简单来说,当两个酶分子结合时,它们拉直并加固了一段柔性片段,帮助引导质子进入反应中心,从而提升酶的产能。对药物开发而言,这提示了一种非常规策略:与其直接阻断活性位点,不如设计能够撬开二聚体或干扰 Glu563–Glu494 相互作用的分子,迫使酶回到迟缓的单体状态。鉴于 qNOR 及其相关酶对若干危险且耐药病原体的存活至关重要,这类基于结构的策略可能有助于下一代靶向抗微生物药物的研发。
引用: Gopalasingam, C.C., Egami, H., Shigematsu, H. et al. Structural basis of Neisseria meningitidis quinol dependent nitric oxide reductase activation by dimerization. Commun Biol 9, 433 (2026). https://doi.org/10.1038/s42003-026-09754-0
关键词: 一氧化氮解毒, 细菌呼吸, 膜蛋白酶, 冷冻电子显微镜, 抗菌药物靶点