Clear Sky Science · zh
空间多组学揭示不可逆电穿孔在肝癌炎性边缘诱导的免疫—代谢特征
为何需要更仔细地审视一种新的肝癌治疗方法
不可逆电穿孔(IRE)是一种较新的肝脏肿瘤破坏方式,使用短时高压电脉冲而非热能。由于它可以保护邻近的血管和胆道,特别适用于位置敏感的肿瘤。然而,多达三分之一的患者仍会在处理区域邻近处出现肿瘤复发。本研究探讨在IRE后那条狭窄的边界区域发生了什么——以及该处免疫细胞和细胞代谢的隐蔽变化是否可能悄然为肿瘤再生创造条件。
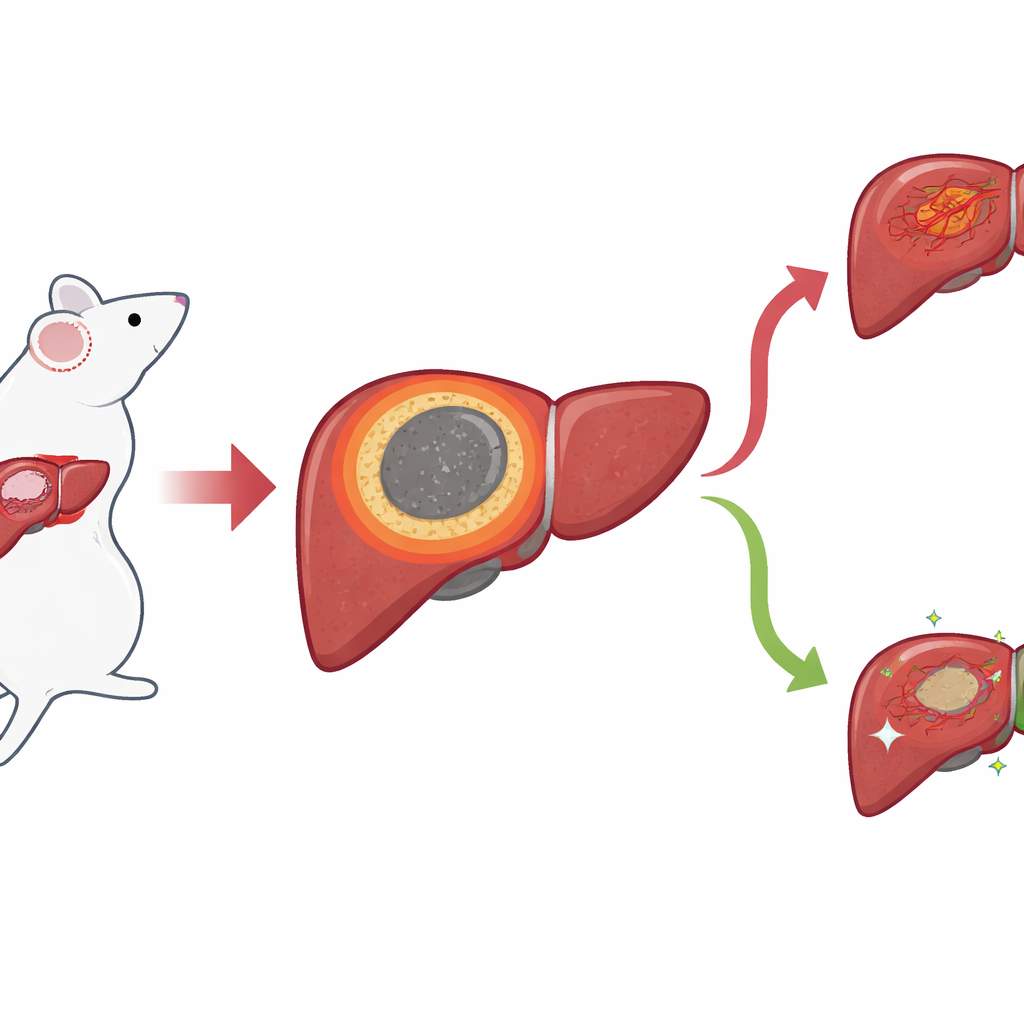
狭窄边界却后果重大
研究者在小鼠肝癌模型中聚焦于在IRE后死去的消融核心与周围健康肝组织之间形成的那一道薄薄组织环。他们称之为炎性边缘(inflammatory margin,IM)。常规显微镜图像显示该区域恰好位于局部复发常出现的位置,但用肉眼难以明确划定其边界。为获得更清晰的图景,团队采用了“空间”方法,在保留组织位置信息的同时读取基因和小分子的分布。通过空间转录组学,他们逐点绘制了基因活性,发现一簇独特的点位正好与IM重合,将坏死的中心与正常肝组织和肿瘤区分开来。
免疫细胞聚集——但多数抑制攻击
随后,科学家结合单细胞和单核RNA测序以及一种强大的细胞谱系分析方法CyTOF,对肝脏中的细胞类型进行了详细目录化。他们发现IM以一种称为巨噬细胞的免疫细胞为主。尤其是类似“脂质相关巨噬细胞”(LAMs)的一类亚群在IRE后数日内大量涌入IM。这些细胞带有与免疫抑制相关的表面标志和基因特征,包括高表达的PD‑L1,这是一种已知会抑制T细胞反应的分子。基因表达分析显示,这些巨噬细胞擅长吞噬物质、响应趋化因子并发出可抑制杀伤肿瘤所需T细胞的信号。成像证实,PD‑L1阳性的巨噬细胞在IM中的丰度远高于邻近正常组织。
脂质化学发生改变的热点
接着,团队将这一免疫格局与空间代谢组学叠加——这是一种通过质谱成像绘制数百种小分子分布的方法。他们显示IM具有不同于死核或周围肝脏的代谢指纹。在这条狭窄的带状区域中,多条脂质相关通路显著增强,包括不饱和脂肪酸、花生四烯酸衍生物和鞘脂类的合成。以花生四烯酸为源的关键信号性脂质,如前列腺素和白三烯,在IM中富集,而处理同一底物的其他酶促路径相对减弱。另一类脂质家族——鞘脂(包括鞘氨醇、鞘磷脂等)也出现累积,并伴随合成和重塑这些分子的酶表达增加。
从损伤到富含能量的生态位的逐步转变
通过将炎性边缘从坏死核心向外细分为三层薄带,研究者观察到化学特征的逐步变化。最靠近坏死区的区域复杂脂质和胆固醇相关分子含量最高,而向外则小分子能量相关代谢物(如葡萄糖和某些氨基酸)含量上升。这一模式表明,在短距离内组织从一个脂质负荷高且信号分子丰富的环境,过渡到一个更有利于细胞生存和生长获得能量的环境。作者提出,这种分步式的重编程有助于维持占主导的嗜脂、免疫抑制性巨噬细胞,并可能悄然为肿瘤细胞重新定植创造条件。
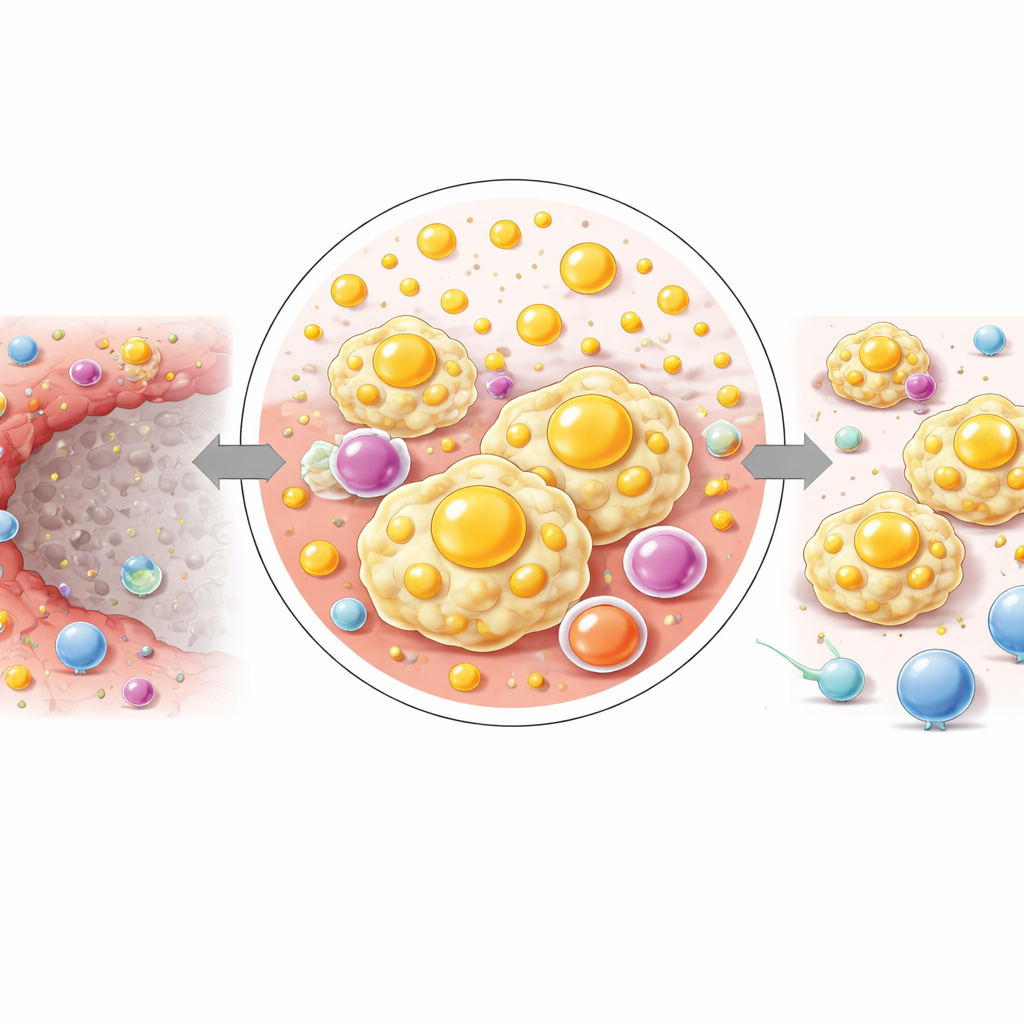
对未来肝癌治疗的意义
通俗地说,这项工作表明IRE不仅仅是杀死肿瘤细胞:它还在消融区周围形成一圈狭窄组织,在那里免疫细胞与脂质化学共同构建了一个受保护的、有利于肿瘤的微环境。该区域的巨噬细胞数量多、富含脂质,并倾向于关闭T细胞而非帮助其发挥作用。由于这些变化与特定代谢通路紧密相关,它们提示了新的治疗切入点。将IRE与针对脂质代谢的药物或阻断PD‑L1的疗法联合应用,理论上可能将这一容易复发的边界转变为真正完成抗肿瘤任务的区域。
引用: Liu, J., Guan, S., Sun, Z. et al. Spatial multiomics reveals irreversible electroporation-induced immuno-metabolic characteristics of the inflammatory margin in liver cancer. Commun Biol 9, 458 (2026). https://doi.org/10.1038/s42003-026-09742-4
关键词: 肝癌, 肿瘤消融, 免疫微环境, 巨噬细胞, 脂质代谢