Clear Sky Science · zh
通过表面修饰细菌产生稳健的活体治疗剂以改善溃疡性结肠炎治疗
把“友好细菌”变成微小保镖
溃疡性结肠炎是一种痛苦的肠道疾病,患者自身的肠道长期处于炎症状态,导致急迫性腹泻、出血和生活质量显著下降。医生和患者都对可能从体内抑制这种炎症的“益生菌”药丸抱有期望,但大多数这些微生物在穿过胃和小肠的严酷旅程中就已死亡,未能到达所需的结肠。该研究描述了一种将益生菌包裹在保护性装甲中的新方法,使其能够安全通过消化道、在结肠定植并帮助修复受损的肠道。
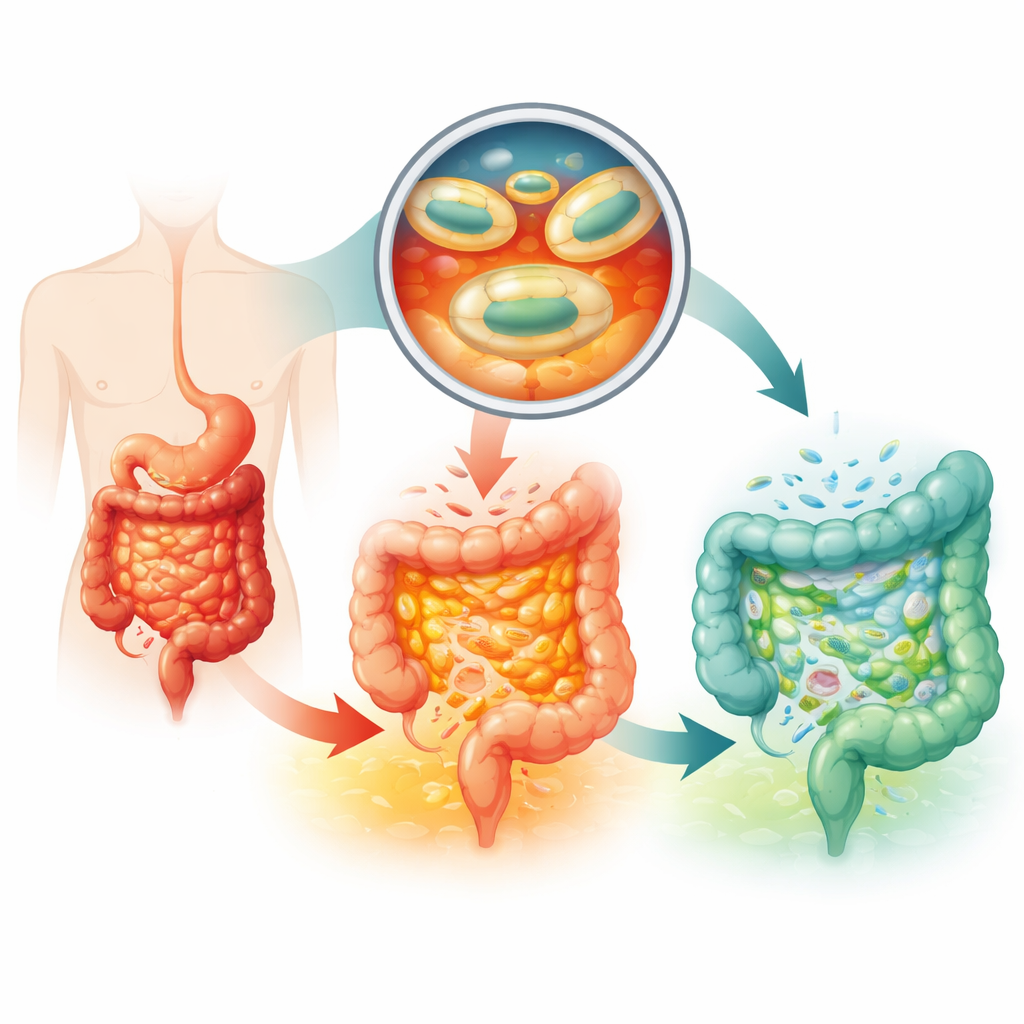
为什么现有益生菌药丸常常难以奏效
溃疡性结肠炎的标准治疗依赖抗炎和免疫抑制药物,这些药物可能有严重副作用且并非对所有人都有效。益生菌通过帮助重建肠道微生物群体提供了一种更温和的方法。一种名为Nissle 1917的大肠埃希氏菌菌株已被批准用于治疗该病,但患者必须每天服用极大量的菌株,即便如此疗效也有限。关键问题在于存活与递送:胃酸、消化酶以及上消化道的快速通过会在细菌附着并在结肠生长之前杀死或冲走大部分细菌,而正常情况下超过99%的肠道微生物位于结肠。
为有益细菌构建保护性外壳
为了解决这一问题,研究人员使用一种植物来源的材料——木质素,在每个益生菌细胞周围创建了一层薄而智能的涂层。他们通过化学改性使木质素更易溶且对酸度变化敏感,得到一种在强酸中保持稳定但在结肠较中性的环境中会分解的物质。采用温和的层层包覆工艺,研究者先在益生菌表面添加钙离子,然后用改性木质素包裹,形成约一万分之一毫米厚的光滑“盔甲”。显微镜观察和粒径测量表明,该防护层在不杀死细菌的情况下为其遮蔽,而且相同方法对几种非常不同的细菌物种均有效,表明这可能成为多种益生菌疗法的通用平台。
靶向结肠并促进其愈合
在模拟消化液中的测试显示,未受保护的细菌很快被胃酸消灭,而被包裹的细菌在数小时内保持存活,并且仅在结肠样的pH水平下有效释放其负载。在化学诱导的溃疡性结肠炎小鼠中,被包衣的细菌在结肠中强烈富集,而未包衣的细菌或与包衣材料的简单混合物大多未能如此。研究团队使用荧光成像、基因检测和数学建模表明,受保护的细菌不仅完整到达结肠,还在那里繁殖,达到了全部肠道微生物约千分之一的比例。接受治疗的小鼠体重下降较少、结肠保持更长,显微镜下肠道组织更健康,细胞连接更紧密,黏液层恢复,这些共同构成体内与肠道内容物之间的重要屏障。
平抑免疫反应并重塑微生物组
除了物理修复外,这些有盔甲的益生菌还重塑了患病肠道的免疫与微生物格局。在病鼠的血液和结肠中,炎性分子的水平偏高、关键的抗炎信号偏低;新疗法逆转了这些趋势,使免疫系统趋于更平静的状态。详细的细胞分析显示结肠和脾脏中的免疫细胞构成发生了变化。与此同时,对肠道微生物的DNA测序显示该疗法提高了整体微生物多样性并增加了若干与肠道健康相关的细菌群,如Akkermansia和Muribaculum。代谢物分析进一步显示与维生素、脂肪酸和氨基酸代谢相关的小分子发生了广泛变化,表明重建后的微生物组正在产生更有利于愈合的化学环境。
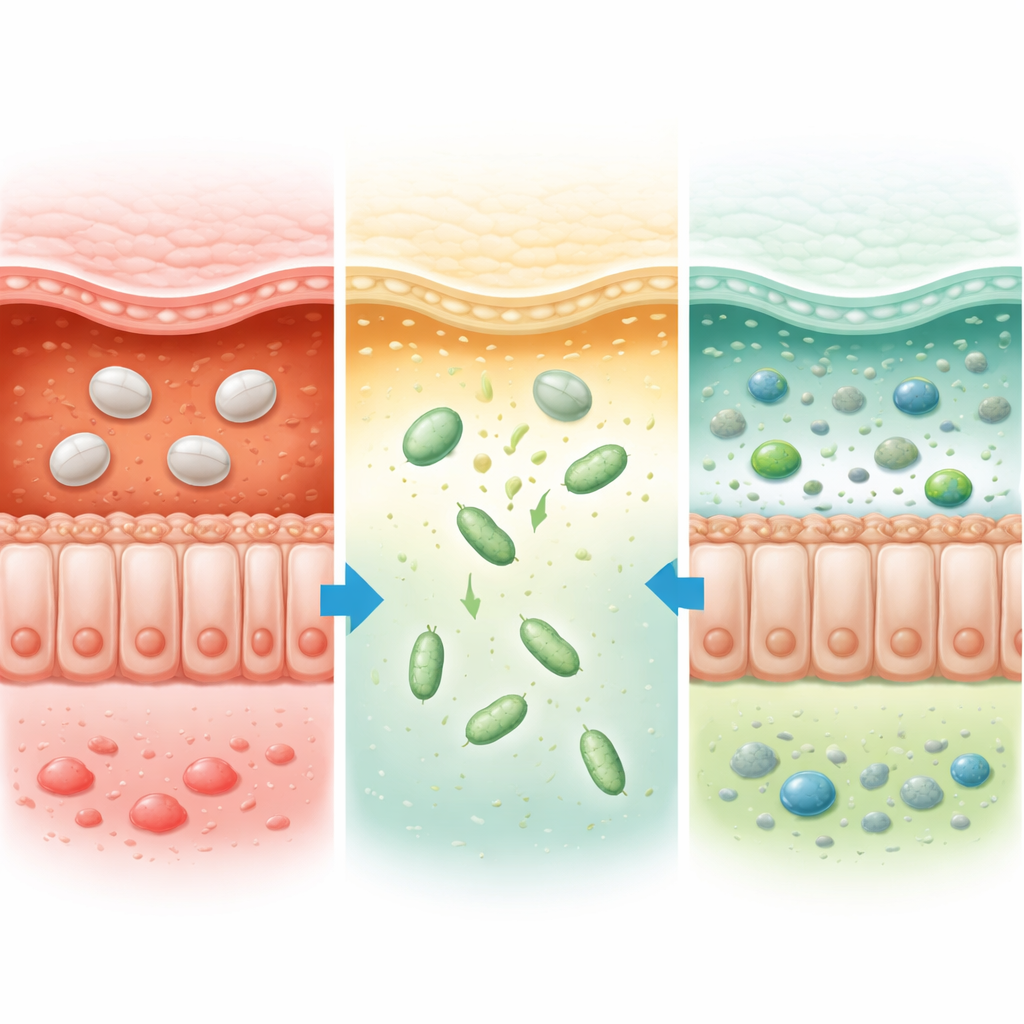
从小鼠研究到未来的活体药物
总体而言,该工作表明为益生菌提供一种pH敏感的装甲可以可靠地将它们护送通过消化道的考验,并将其释放到溃疡性结肠炎造成最大损伤的部位。在小鼠中,这一策略使得更低剂量的细菌就能定植结肠、修复肠道屏障、降低有害炎症并恢复更健康的微生物群落和代谢谱。由于该植物基包衣本身在很大程度上不经改变通过体内,且该方法可应用于多种细菌类型,作者认为他们的方法为设计下一代用于溃疡性结肠炎和其它结肠疾病的“活体”药物提供了一个广泛适用的蓝图。
引用: Liu, J., Fang, Z., Li, X. et al. Surface decoration of bacteria generates robust living therapeutics for improved ulcerative colitis therapy. Commun Biol 9, 428 (2026). https://doi.org/10.1038/s42003-026-09732-6
关键词: 溃疡性结肠炎, 益生菌, 肠道微生物组, 药物递送, 肠道屏障