Clear Sky Science · zh
单核RNA测序与急性甲基苯丙胺诱导认知损伤的功能研究
这对大脑健康为何重要
甲基苯丙胺常被描述为能“烧毁”大脑的毒品,但这种损伤在细胞内部到底是什么样子?本研究逐个细胞检查小鼠记忆中枢——海马体,探查短时大量使用甲基苯丙胺如何扰乱支持学习与记忆的细胞机制。通过前所未有的细致图谱,研究指出了新的生物薄弱环节,这些环节未来可能成为保护或恢复受药物影响人群大脑功能的靶点。
暴饮暴食剂量的甲基苯丙胺如何影响记忆
研究者首先问了一个简单的问题:短期强烈剂量的甲基苯丙胺会损害小鼠记忆吗?实验动物在一天内接受四次注射,模拟暴饮暴食模式。测试显示,这些小鼠在识别新物体方面出现困难,并且在水迷宫中找到隐藏平台的时间更长,这是学习与空间记忆受损的典型表现。即便平台被移除,它们也较少在正确位置搜索,表明海马体——大脑的导航与记忆枢纽——的某些功能已受到影响。
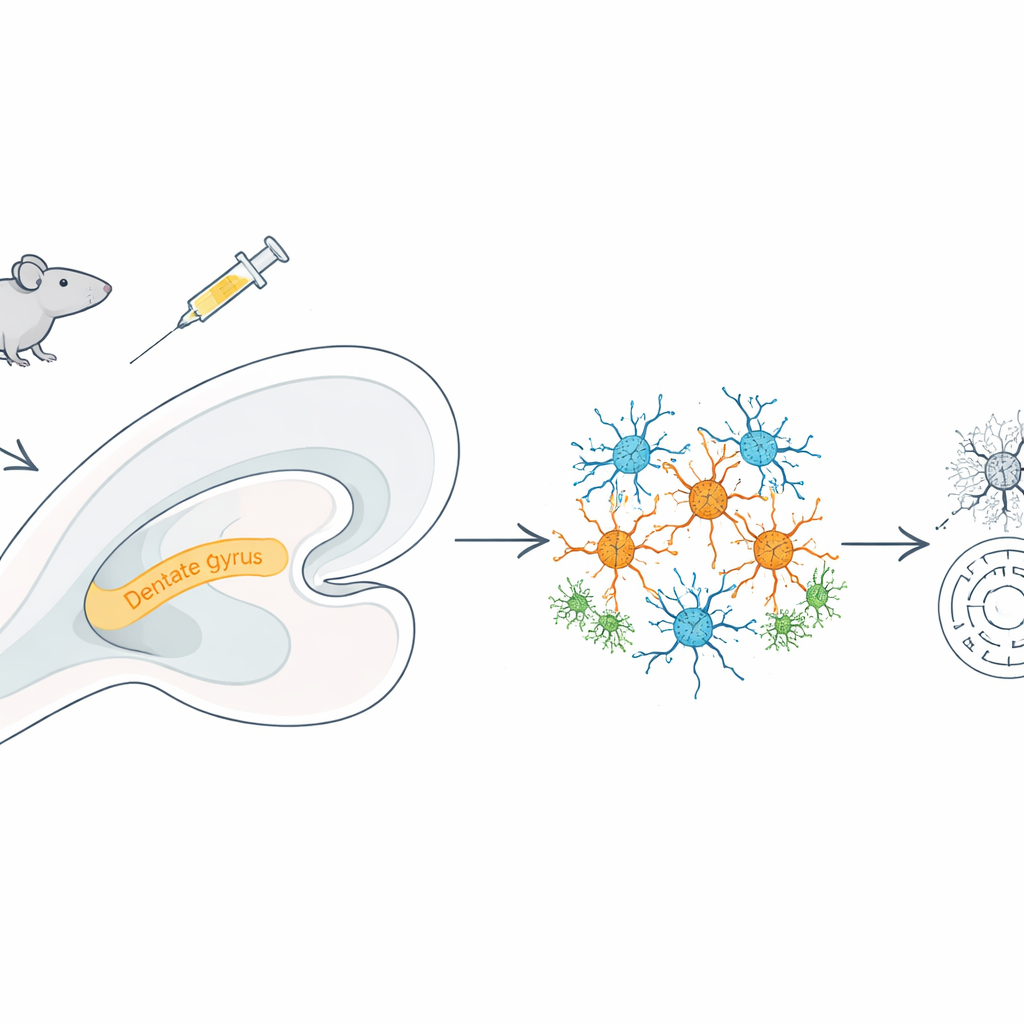
逐个细胞核观察
为了解具体出问题的环节,团队采用了单核RNA测序,这项技术可同时读取数千个独立细胞核中被激活的基因。从超过36,000个海马细胞核中,他们鉴定出十种主要细胞类型,包括兴奋性与抑制性神经元、星形胶质细胞、小胶质细胞、少突胶质细胞以及血管细胞。甲基苯丙胺暴露改变了这一细胞景观:兴奋性神经元、小胶质细胞、少突胶质细胞和内皮细胞数量增加,而抑制性神经元减少。这一倾向使兴奋性占优,可能令神经回路更容易受到应激与损伤。
能量工厂承压、防御体系衰弱
最显著的基因变化出现在兴奋性神经元,尤其是位于海马体的齿状回(dentate gyrus)区,该区对于形成独特记忆至关重要。在这里,与氧化磷酸化相关的基因——线粒体产生细胞能量的过程——发生了强烈改变,电子显微镜图像显示线粒体破碎、内结构受损。同时,与活性氧和炎性信号相关的通路被激活,一类称为过氧化物酶体的细胞器(负责控制代谢有害副产物)出现功能衰退的迹象。重要的过氧化物酶体相关基因,包括PEX5,活性下降,而驱动炎症与氧化应激的基因上调,表明甲基苯丙胺使神经元陷入能量危机,同时削弱其天然解毒系统。
脆弱的细胞群体与混乱的细胞间对话
进一步分析显示,兴奋性神经元可细分为五个区域亚型,齿状回细胞表现出最强烈的应激信号:炎症增强、氧化负担更重以及一种称为焦亡(pyroptosis)的炎性细胞死亡形式。在该区域内,研究者鉴定出一组在甲基苯丙胺处理动物中高度富集的兴奋性神经元亚群,携带最强的损伤标记,可能是暴露后的主要受害者。整个海马体中,兴奋性神经元与其他细胞类型之间的通信增强,而来自抑制性神经元的联系减弱。作为大脑免疫哨兵的小胶质细胞转向高度炎性状态。与此同时,研究团队追踪到多组与记忆表现密切相关的基因簇,强调了兴奋性神经元、抑制性神经元、星形胶质细胞和少突胶质细胞中可能加剧或缓冲认知下降的网络。
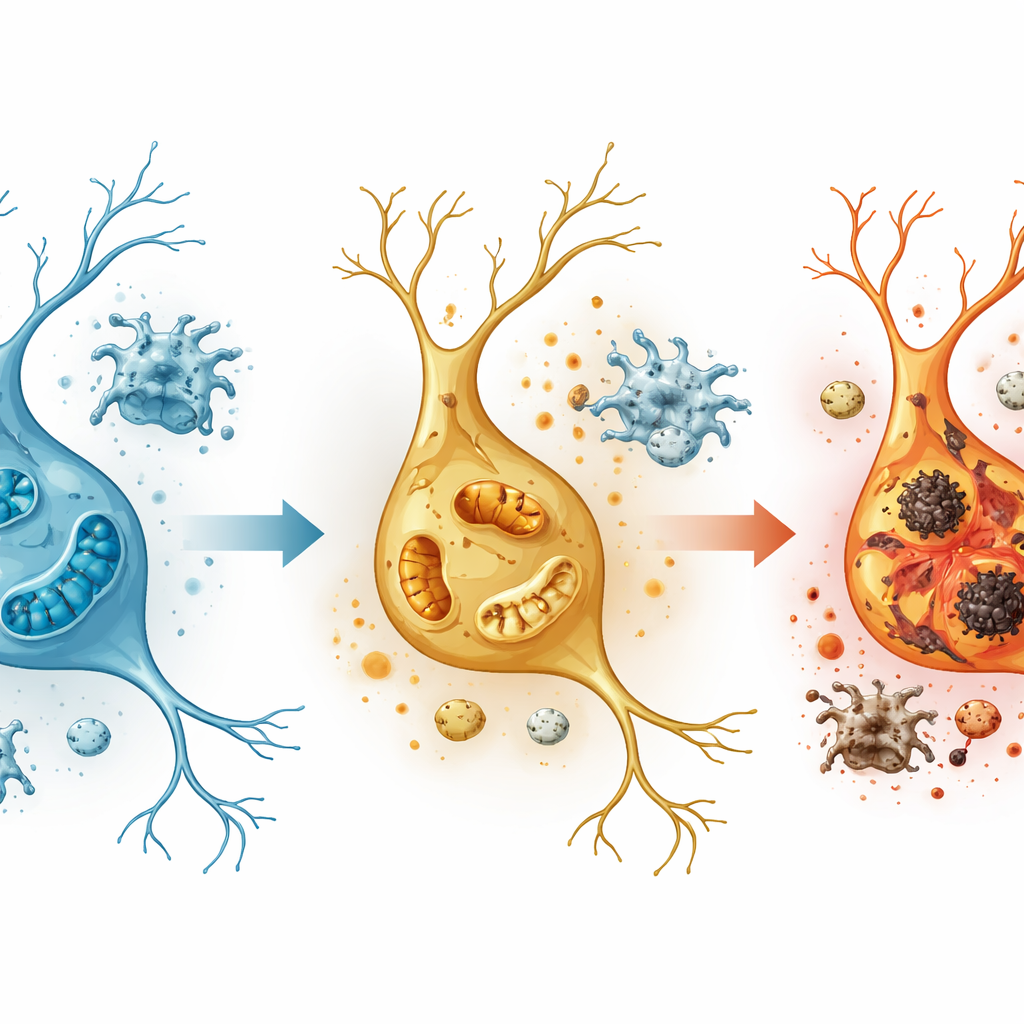
新的分子线索与可能的脑保护路径
研究还聚焦于可能在甲基苯丙胺损伤中处于核心位置的特定分子。其一是名为Ddx5的RNA加工蛋白,在多种细胞类型中显著上调,尤其在齿状回,暗示一种广泛的应激反应,其是保护性还是有害尚待澄清。相反,PEX5与调节脂质的开关PPARα这两者——对维持过氧化物酶体和线粒体平衡都很重要——在兴奋性神经元中被下调。综合来看,这些变化表明恢复能量代谢、巩固过氧化物酶体功能并抑制过度活跃的免疫反应,可能是限制急性甲基苯丙胺暴露后脑损伤的有前景策略。
用通俗的话说这意味着什么
通俗地说,这项工作显示即使一次短暂的甲基苯丙胺暴饮暴食也会在大脑的记忆中心留下深刻印记。它使齿状回的关键神经元陷入能量短缺,令它们积累有毒代谢产物,削弱清除系统,并激活邻近的免疫细胞,进一步加剧组织炎症。通过精确描绘哪些细胞类型、区域和基因网络受影响最深,研究超越了“脑损伤”这一模糊概念,识别出可具体干预的生物过程——如能量生成失常和解毒通路损坏——这为保护或修复受甲基苯丙胺伤害者的大脑提供了可行方向。
引用: An, D., Lu, F., Wang, Y. et al. Single-nucleus RNA sequencing and functional studies of acute methamphetamine-induced cognitive impairment. Commun Biol 9, 440 (2026). https://doi.org/10.1038/s42003-026-09728-2
关键词: 甲基苯丙胺, 海马体, 单核RNA测序, 线粒体功能障碍, 神经炎症