Clear Sky Science · zh
NRF2 激活剂与核输出抑制剂塞利奈克索通过一种独立于 NRF2 的机制,靶向涉及 ACE2、TMPRSS2 和 XPO1 的网络,从而限制冠状病毒
帮助细胞对冠状病毒说“不”的药物
目前大多数冠状病毒治疗策略直接针对病毒本身。但病毒善于变异,新变种很快就能削弱这些药物的效果。本研究探讨了另一种策略:让我们的细胞变得对严重的 SARS-CoV-2 及较温和的季节性毒株都不那么友好。通过调整细胞处理几个关键“门卫”蛋白的方式,研究者表明现有的小分子可以在体外模型中显著降低感染,而且它们的作用并不依赖于这些化合物最初出名的常见抗病毒通路。
对冠状病毒防御的新视角
团队集中研究了已知能激活由蛋白 NRF2 控制的细胞保护程序的化合物。这些化合物——4-辛基伊塔康酸酯(4OI)、巴多昔酮(BARD)和萝卜硫素(SFN)——与阻断一种称为 XPO1 的运输蛋白的药物塞利奈克索(SEL)一起进行了测试,XPO1 有助于将蛋白从细胞核运输出去。在肺和肾细胞模型中,这四种药物都能在不损害细胞的前提下降低 SARS-CoV-2 水平,并对若干关注变体有效。出人意料的是,当通过基因手段去除 NRF2 时,病毒复制反而增强,证明 NRF2 本身具有天然保护作用——但这些药物仍然有效,表明它们的抗病毒效力来自另一条途径。 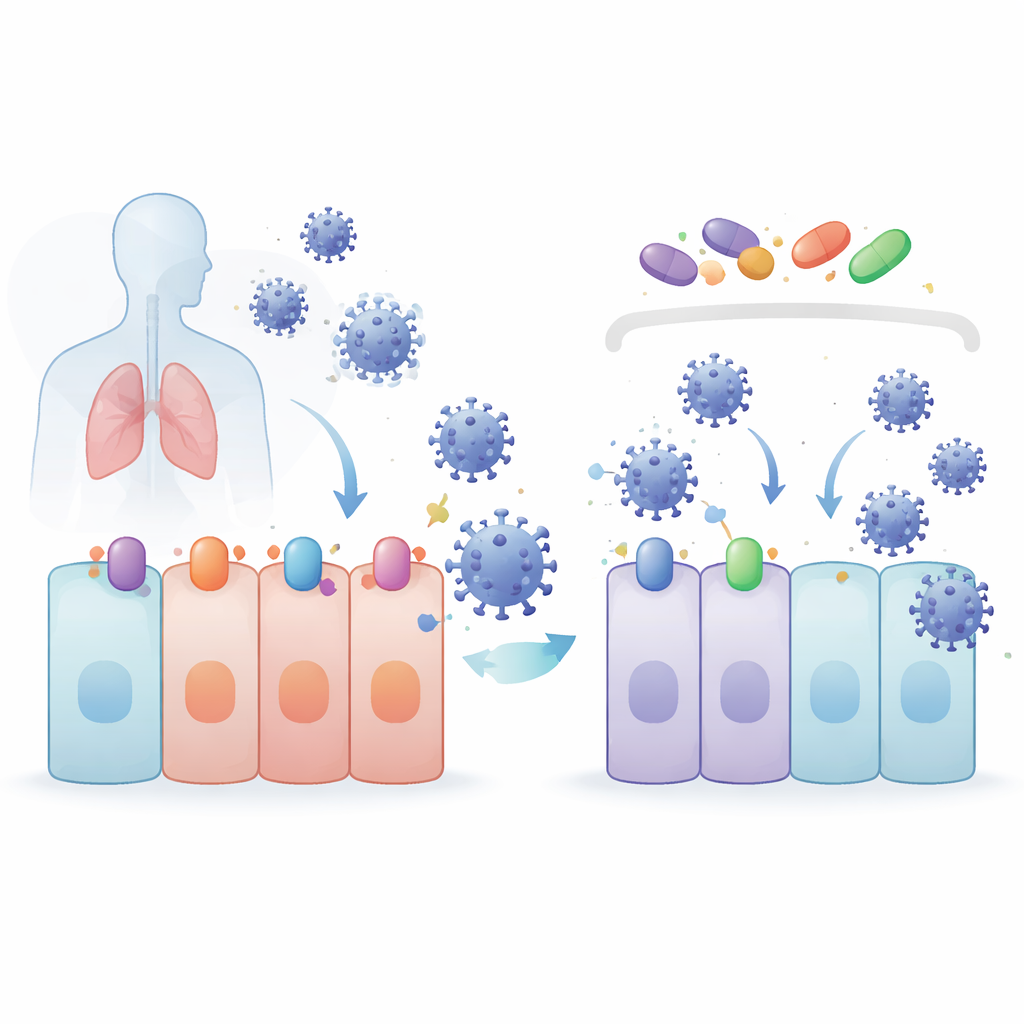
封锁病毒的前门
冠状病毒通过与细胞表面的受体蛋白结合来启动感染。对 SARS-CoV-2 及其近亲来说,主要“门”是 ACE2,并由一种称为 TMPRSS2 的切割酶辅助。出口蛋白 XPO1 似乎也有助于感染。研究人员发现,4OI、BARD、SFN 和 SEL 都能降低人肺细胞中 ACE2、TMPRSS2 和 XPO1 的含量。尤其是 4OI 和 SEL 在感染前存在时最为有效,它们阻止了包裹有冠状病毒刺突蛋白的类病毒颗粒进入。换句话说,这些药物不仅在病毒进入后减慢其速度——它们还帮助去除病毒打开“门”所需的锁和把手。
细胞如何拆除关键的病毒助推器
进一步研究显示,4OI 加速了 ACE2 蛋白的降解。在正常条件下,ACE2 可存在数小时;加入 4OI 后,它在远短于此的时间内从细胞表面消失。这种破坏需要两个细胞内的标记酶 NEDD4L 和 MDM2,它们向蛋白附加分子“处理掉我”的标签。阻断这些标记酶削弱了 4OI 清除 ACE2 的能力。令人惊讶的是,常见的蛋白碎解机器——蛋白酶体,并不是主要途径。ACE2 被引导进入细胞的回收与废物处理系统——溶酶体。研究还发现,这些药物降低了 ACE2 和 XPO1 的基因表达,部分原因是它们减少了通常促进 ACE2 基因转录的 STAT3 蛋白的活性。 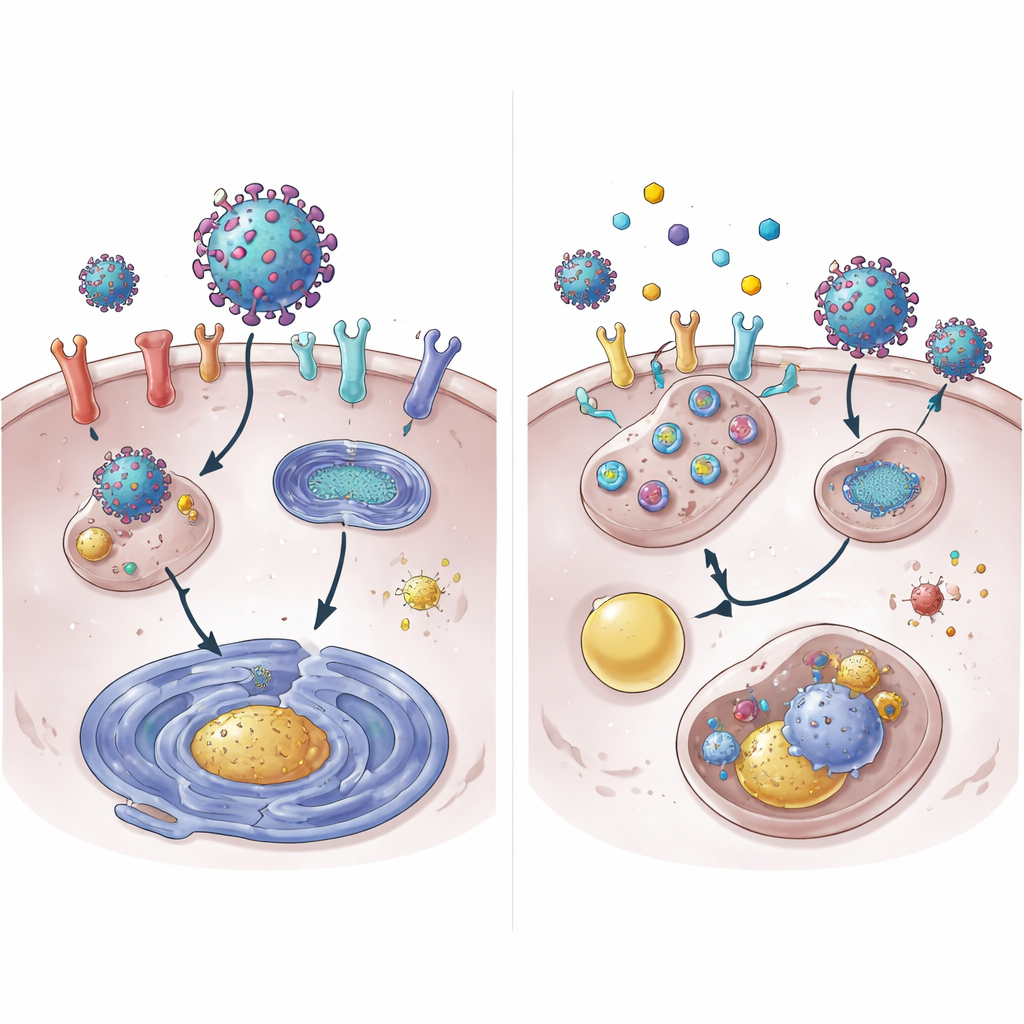
季节性冠状病毒与 XPO1 的关联
接着,科学家们转向了 hCoV-229E,这是一种通常引起轻微感冒但在免疫功能低下者中可能致命的季节性冠状病毒。使用工程化的能在复制时发光的病毒,他们表明四种化合物在肺细胞和血管细胞中都能强烈抑制 229E,即使在缺失 NRF2 的情况下亦然。与 SARS-CoV-2 不同,这种病毒使用另一种受体 ANPEP,而这些药物并未改变 ANPEP。相反,它们的影响与降低 XPO1 的能力密切相关。敲低 XPO1 本身就能显著降低 229E 的复制,而在这些 XPO1 含量低的细胞中,塞利奈克索的效果几乎消失。这个排序——SEL 最依赖 XPO1,BARD 最少依赖——表明每种化合物具有略微不同的靶点组合,而 XPO1 是它们许多抗病毒作用的中心枢纽。
这对未来治疗可能意味着什么
对非专业读者而言,关键结论是:我们不仅可以通过攻击病毒来对抗冠状病毒,还可以通过温和地重构自身细胞使其更难被感染来实现防御。在体外培养的人类细胞中,研究的化合物去除了 SARS-CoV-2 和一种普通感冒冠状病毒依赖的关键结合位点和辅助通路,而且它们在很大程度上并不依赖最初让它们受关注的 NRF2 通路。尽管这些发现仍处于临床前阶段,尚未直接转化为药物,但它们指向一条有前景的路径:通过靶向诸如 ACE2、TMPRSS2 和 XPO1 等共享宿主蛋白网络,同一类药物可以同时降低病毒入侵、抑制有害炎症并保护组织。
引用: Waqas, F.H., Silva da Costa, L., Zapatero-Belinchón, F.J. et al. NRF2 activators and the inhibitor of nuclear export, selinexor, restrict coronaviruses by targeting a network involving ACE2, TMPRSS2, and XPO1 through an NRF2-independent mechanism. Commun Biol 9, 384 (2026). https://doi.org/10.1038/s42003-026-09724-6
关键词: 宿主导向抗病毒药物, 冠状病毒入侵, ACE2 与 TMPRSS2, NRF2 激活剂, XPO1 抑制