Clear Sky Science · zh
一种由肌动蛋白介导的两步策略使空肠弯曲菌(Campylobacter jejuni)促使线粒体聚集并维持铁稳态,以利胞内存活和持久化
为什么细胞内这场微小战斗很重要
未充分煮熟的鸡肉导致的食物中毒常被归咎于一种名为Campylobacter jejuni的细菌。大多数人会康复,但这种微生物在多种环境中出乎意料地善于生存,这有助于它从农场传播到餐桌。本研究考察了该细菌藏匿于一种常见的淡水自由生活变形虫内时的表现,并揭示了一种围绕重塑细胞内部骨架、使能量“动力包”(线粒体)聚集以及调控铁和有害氧化化学反应的复杂生存策略。理解其生命周期中这一隐蔽阶段,或可指向在细菌到达人类之前遏制其污染的新方法。
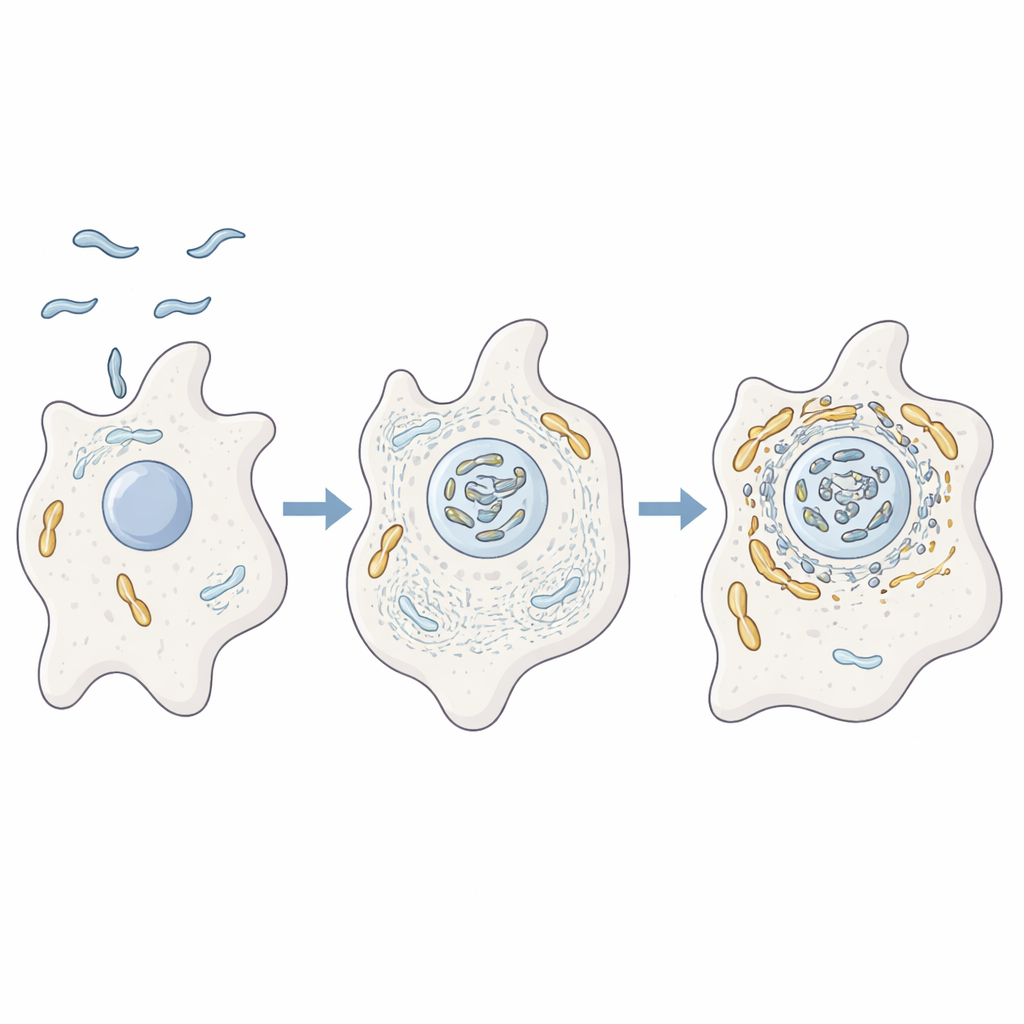
在变形虫中“训练”的微生物
作者研究了C. jejuni在变形虫Acanthamoeba castellanii内的行为,这是一种生活在土壤和水中的单细胞生物。这些变形虫为许多致病细菌提供了训练场,能保护细菌免受恶劣环境和消毒剂的伤害。通过先进的蛋白质分析、显微成像和基因突变体研究,研究人员显示当C. jejuni感染变形虫时,会与宿主的线粒体紧密相关联。与此同时,由肌动蛋白构成的细胞内部支架及调控其形状和运动的蛋白在这些线粒体附近明显富集,表明细菌在积极重排宿主细胞的内在结构。
弯曲细胞骨架以移动“动力包”
为检验肌动蛋白是否确实驱动这种相互作用,研究组阻断了肌动蛋白形成丝状结构或分支网络。在这些条件下,线粒体不再在细菌附近聚集,而是以零散点状分布,细菌的存活率下降。随后他们关注两种细菌辅助蛋白CiaD和CiaI,这些蛋白通过细菌的鞭毛(一种鞭状尾)注入宿主细胞。结果发现CiaD能促进肌动蛋白生长并在变形虫表面诱导尖刺状突起,帮助宿主细胞吞噬细菌。进入细胞后,线粒体以肌动蛋白依赖的方式在含菌区周围聚集,将细菌置于富含宿主能量机器的特权区域。
重塑线粒体的分子开关
虽然CiaD对进入至关重要,CiaI则控制后续过程。当研究人员删除CiaI基因时,C. jejuni不再诱导显著的线粒体聚集,且在变形虫内存活不佳。仅将纯化的CiaI附着在微小颗粒上(无需活细菌)就足以引起邻近线粒体融合和聚集,并局部去除肌动蛋白。生化测试表明CiaI以协同方式结合能量携带分子,表现得像一个分子开关,可能会根据宿主内的条件开启或关闭其活性。作者提出,在CiaD驱动的肌动蛋白生长将线粒体带近之后,CiaI促使局部肌动蛋白降解并将线粒体网络重塑为围绕含菌区的致密聚集体。
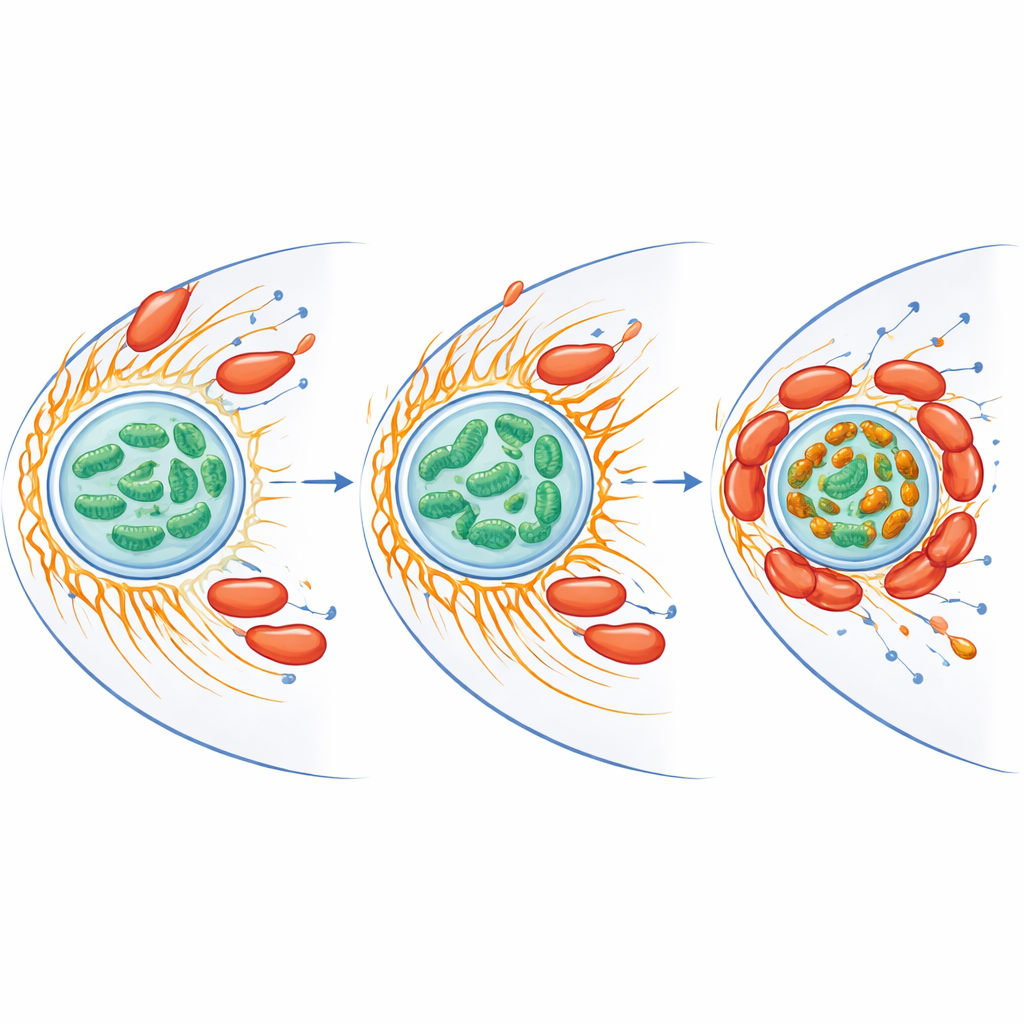
重接线宿主细胞内的铁与应激反应
线粒体的功能不仅是产生能量——它们也处理铁并产生反应性氧种(ROS),即可杀死微生物的化学活性氧。研究人员发现感染减少了线粒体内总体的游离铁,但同时在围绕细菌聚集的线粒体处产生了明亮的富铁簇。涉及铁处理和抗氧化应激的蛋白在宿主和细菌中均有所上调。当研究组用螯合化合物去除游离铁时,变形虫的ROS爆发下降,而C. jejuni的存活显著增加。被感染细胞中的线粒体还显示出更高的膜电位,表明活动性升高,这提示细菌促使宿主的“动力包”进入一种有利于其自身持续存在并抑制有害氧化反应的状态。
对食品安全与感染的意义
综合来看,结果支持一种两步策略:首先,CiaD刺激肌动蛋白生长,帮助细菌进入变形虫并将线粒体拉向入侵部位;其次,CiaI在局部拆解肌动蛋白并将线粒体重塑为富铁簇,包绕含菌区,同时削弱宿主的氧化防御。这种对细胞形态、能量利用和金属平衡的精细调控有助于C. jejuni在变形虫内存活,并可能促进其在环境中的持久化及随后感染人类。通过揭示这场微观拉锯战的关键参与者,研究指出了潜在的新靶点——例如Cia蛋白、肌动蛋白与线粒体接触点或铁处理通路——可以被干预以减少污染和疾病。
引用: Nasher, F., Wren, B.W. A two-step actin-mediated strategy enables Campylobacter jejuni to promote mitochondrial aggregation and iron homeostasis, for intracellular survival and persistence. Commun Biol 9, 431 (2026). https://doi.org/10.1038/s42003-026-09713-9
关键词: 弯曲菌属, 变形虫, 线粒体, 肌动蛋白细胞骨架, 铁稳态