Clear Sky Science · zh
长期无饲养细胞的猫肠类器官培养,用于研究弓形虫(Toxoplasma gondii)的有性发育
为什么这种微小寄生虫很重要
弓形虫是一种能感染几乎所有恒温动物(包括人类)的显微寄生虫。大多数人类感染轻微或无明显症状,但对未出生的胎儿和免疫功能低下者可能造成严重伤害。其生命周期中的一个关键环节只在猫的肠道中发生,寄生虫在此进行有性繁殖并形成可在环境中传播的耐久卵囊。由于在活体猫身上实验既困难又具伦理敏感性,科学家们正在寻找可在实验室培养的猫肠组织以替代真实器官。本研究报告了朝这一方向迈出的重要一步,并检验了这类组织是否能诱导弓形虫进入其有性阶段。
在培养皿中构建猫肠
研究人员首先从家猫的小肠分离干细胞,并将其培养成三维“类器官”——模拟肠上皮关键特征的微小中空球体。此前其他团队的尝试常在短期后停止生长,而本研究组通过优化温度和生长信号,使这些微型肠道在没有辅助“饲养”细胞的情况下能够存活并分裂数月之久。类器官还能从生长状态切换到更成熟、类肠的状态,展现出与不同肠上皮细胞类型相匹配的结构变化和基因表达转变。
将类器官拉平成便于感染的单层 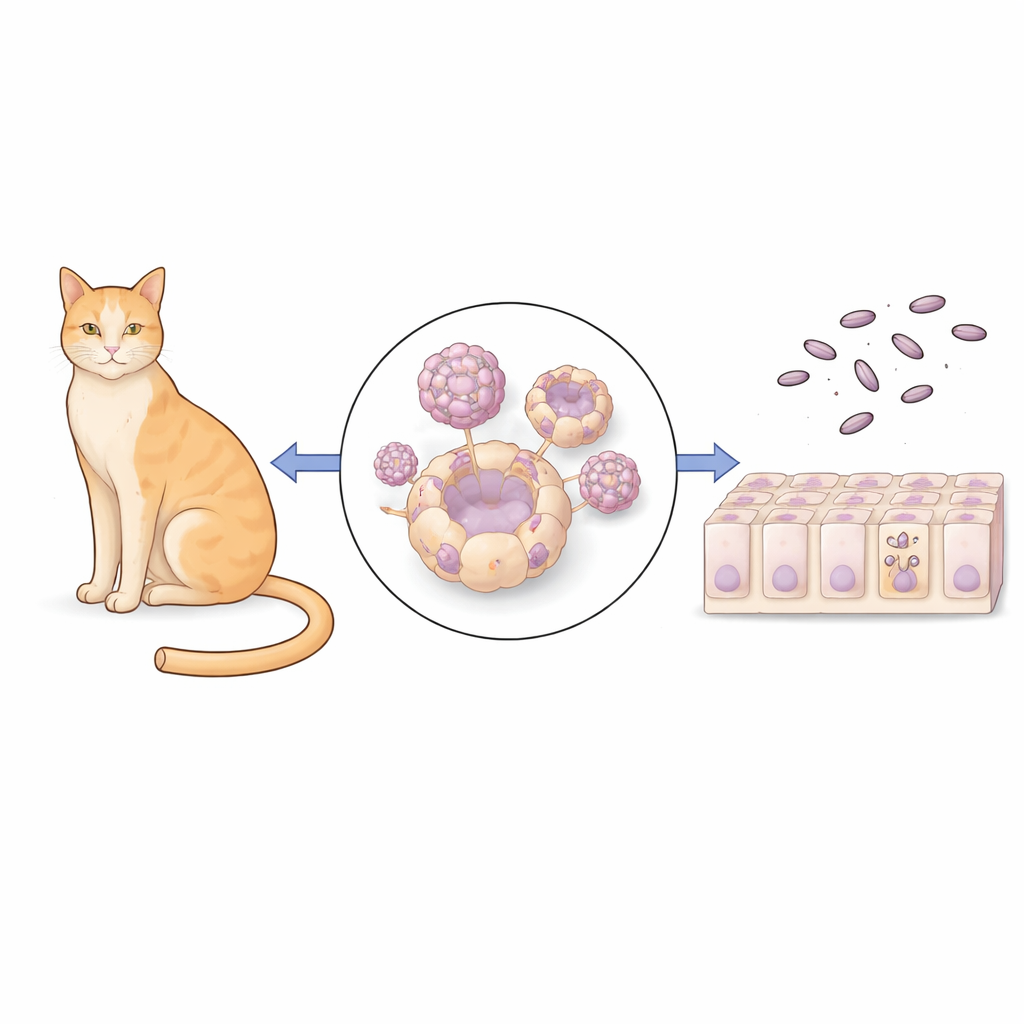
Figure 1.

为更好地控制感染实验,科学家们将三维类器官转化为称为类器官衍生单层的平面细胞层。他们将类器官解离为单个细胞,铺展在多孔膜上,让它们重新形成类似肠上皮的连续层。显微镜观察和电学测量显示,这些单层紧密封闭、具极性(有明显的顶端和底端),在结构上类似猫十二指肠组织。尽管细胞类型的范围有限并偏向于发育较不成熟的细胞,该体系仍提供了可重复的、猫特异的表面,寄生虫可以从“肠道”侧接触到它,类似于真实肠道的情形。
挑战寄生虫促其转变
有了这一平台,团队探问猫源环境是否能促使弓形虫进入难以捉摸的有性阶段。他们使用了一株经过基因工程改造的寄生虫,该株中两个调控蛋白AP2XII-1和AP2XI-2可以通过化学方法去除。先前在人类细胞中的工作显示,同时去除这两个因子会将寄生虫从其常见的快速生长形态(速殖子)推向一种称为裂殖前期(merozoite-like)的前有性阶段,但这一转变止步于此。在猫细胞单层中,去除这些调控因子同样推动寄生虫向裂殖体样形态转变。超微结构成像显示出与该转变一致的分裂形态,同时标准速殖子的数量减少。
有性线索,但未见完全转化 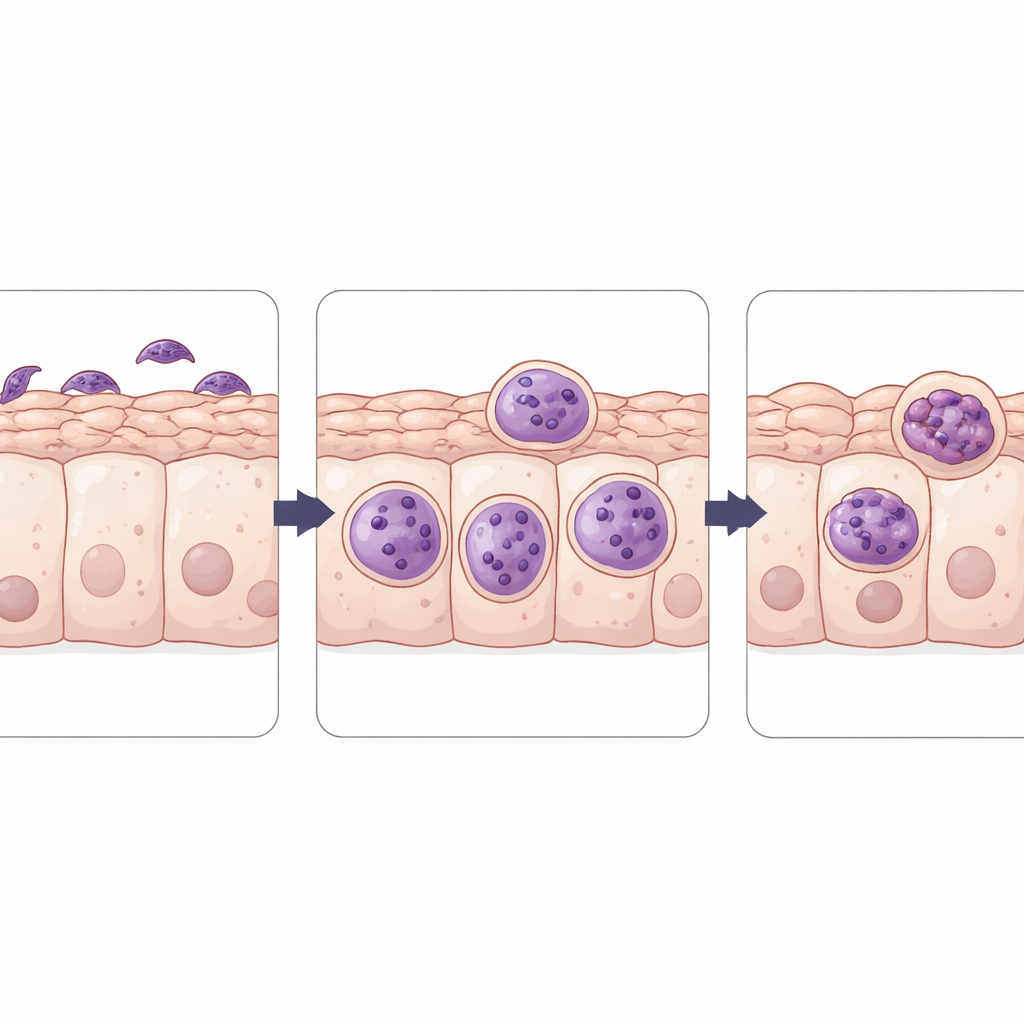
Figure 2.

为寻找真正的有性发育,研究人员追踪了通常在雄性和雌性配子以及卵囊壁中开启的寄生虫基因。在猫单层中,这些性阶段标志基因在去除AP2后比在常规人类细胞培养中更明显地上调,表明猫细胞提供了一些正确的信号提示。然而,精细的电子显微镜观察并未发现成熟配子或卵囊的形成,即便将培养基补充了被认为在猫体内重要的营养物质和脂肪酸(如亚油酸、牛磺酸以及一种猫特有的化合物——费林宁)。另一株天然具备产卵囊能力的寄生虫菌株也仍停滞在无性状态,这进一步说明仍然缺少促其完全发育的适当信号组合。
对理解和控制弓形虫病的意义
这项工作提供了一个稳健、长期存活的实验室猫小肠模型,并表明该模型能在一定程度上推动弓形虫朝有性繁殖路径前进。对非专业读者而言,关键结论是:科学家们现在拥有一种强有力的猫特异性组织体系,既避免使用活体动物,又复现了自然宿主的许多特征。尽管本研究中的寄生虫尚未完成其有性周期,性相关基因活性的上升强烈暗示该模型已接近真实情况。通过在这些类器官中系统地调整营养成分、氧气水平和寄生虫遗传背景,未来研究可以精确定位那些“仅在猫体内”出现、允许弓形虫产生具有感染力卵囊的关键线索。这些知识最终可能为阻断环境污染、减少全球人畜暴露提供新的策略。
引用: Warschkau, D., Hoffmann, T., Laue, M. et al. Long-term feeder cell-free cat intestinal organoid cultures to study Toxoplasma gondii’s sexual development. Commun Biol 9, 379 (2026). https://doi.org/10.1038/s42003-026-09710-y
关键词: 弓形虫(Toxoplasma gondii), 肠类器官, 猫肠模型, 寄生虫生命周期, 宿主–寄生虫相互作用