Clear Sky Science · zh
成瘾性药物滥用与抑郁——聚焦表观遗传学
这项研究与日常生活的关系
成瘾性药物与抑郁常被视为不同的问题,但它们经常在同一人群中同时出现。本文综述解释了甲基苯丙胺、可卡因、阿片类和大麻等药物的长期使用如何在大脑中留下持久的“分子伤痕”,从而增加抑郁的风险。通过揭示这些隐蔽的改变,文章指向未来可能用于识别高危人群的检测手段——以及可能逆转损伤而不仅仅掩盖症状的更精确治疗方法。
成瘾与情绪低落如何交织在一起
作者首先概述了药物滥用与抑郁之间密切的临床联系。反复使用成瘾性物质的人更容易报告持续的悲伤、快感丧失、睡眠问题和自杀念头。控制奖赏、动机、记忆与决策的大脑区域——腹侧被盖区、伏隔核、前额叶皮层与海马——在两种状况中都居于核心地位。慢性药物暴露破坏了多巴胺与血清素等神经递质、下丘脑—垂体—肾上腺轴控制的应激激素、免疫信号以及神经元的能量供应。这些变化共同降低了大脑对压力的弹性,使其更易陷入抑郁状态,即便在最后一次用药很久之后仍然如此。
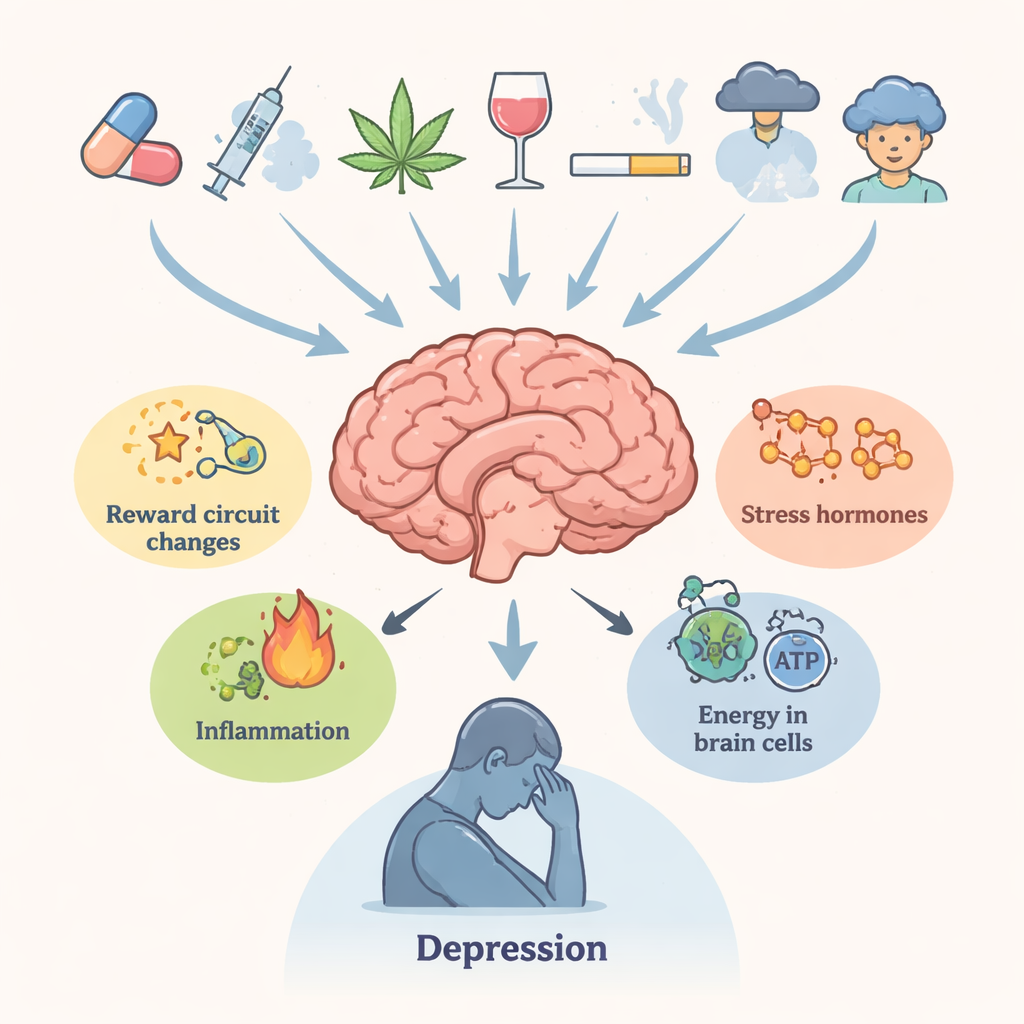
改写大脑化学的药物
综述考察了几类主要药物。安非他命类兴奋剂及其同类(包括合成“浴盐”)引发强烈的多巴胺及其他递质激增,随着时间推移损伤神经末梢、扰乱谷氨酸平衡、增加内质网应激,并推动细胞进入有害的自噬过程。青春期使用大麻与日后抑郁和自杀风险相关,可能通过对大麻素受体、白质结构和多巴胺回路敏感性造成长久改变。阿片类在缓解疼痛的同时,会引发炎症、线粒体功能衰竭以及诸如脑源性神经营养因子(BDNF)等生长支持信号的减少。可卡因反复激活应激系统并改变关键调节因子如 FKBP5,促成戒断期间的焦虑与情绪低落。每一种情况下,生物学扰动往往持久存在,有助于解释为何情绪症状可超出生理中毒的明显时限。
表观遗传学:暴露的记忆
为理解药物效应为何持久,作者聚焦于表观遗传学——不改变 DNA 字母但调节基因活性的化学标签与分子开关。成瘾性药物改变 DNA 甲基化(在胞嘧啶碱基上的标记)、修饰包装 DNA 的组蛋白上的化学基团,并改变那些微调蛋白质产生的非编码 RNA。例如,甲基苯丙胺和可卡因会在奖赏相关脑区改变甲基化模式,进而改变添加或去除这些标记的酶的水平。阿片类与兴奋剂重塑控制谷氨酸受体、应激信号与突触结构基因的组蛋白乙酰化与甲基化。数十种 microRNA、长非编码 RNA 和环状 RNA 随药物暴露升高或下降,联合影响炎症、神经生长与突触强度。这些表观遗传改变像分子“记忆”一样记录了药物暴露的历史。
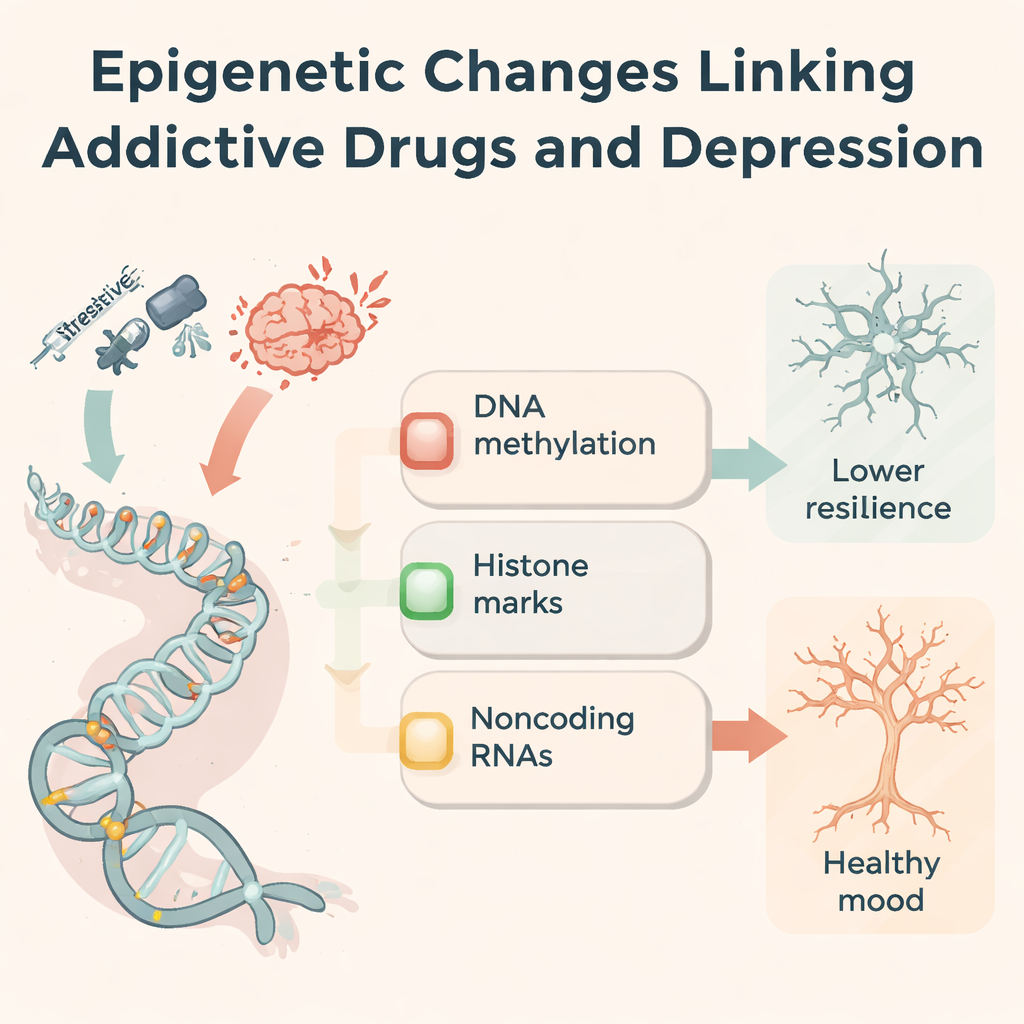
抑郁与成瘾的共同分子通路
相同的表观遗传机制也出现在未曾用药的抑郁患者与动物模型中。应激经历可以改变应激激素受体(如 NR3C1 和 FKBP5)的甲基化,降低有益的生长因子如 BDNF,并重塑免疫与谷氨酸通路。许多被药物改变的非编码 RNA 在抑郁中也出现失调,影响新生神经元的产生、小胶质细胞对炎症的反应以及突触连接的强度。作者提出了一个三部分框架:应激反应调节、奖赏回路重塑与突触可塑性。在这些轴线上,成瘾与抑郁反复汇聚于一小组基因与标记,这为两种疾病常共存提供了生物学解释。
对未来预防与治疗的意义
结论部分认为,表观遗传改变可能成为早期预警生物标志物和下一代治疗的靶点。已经有广谱作用、能够抹去表观遗传标记的药物在动物中显示了一些类抗抑郁效应,但对人类常规使用而言过于粗糙。新的工具——例如基于 CRISPR 的表观基因组编辑器以及调控特定 microRNA 或长 RNA 的疗法——未来或可在保留其他细胞功能的同时,针对特定脑细胞调整有问题的基因。作者也警示说,目前大部分数据来自啮齿动物和整体脑组织,人类生物学更为复杂。尽管如此,通过揭示成瘾性药物和抑郁如何在同一本分子“笔记”上留下痕迹,这项工作为更个体化且持久的治疗路径提供了希望。
引用: Zhang, W., Xu, M., Wang, C. et al. Addictive drug abuse and depression-a focus on epigenetics. Commun Biol 9, 297 (2026). https://doi.org/10.1038/s42003-026-09705-9
关键词: 成瘾与抑郁, 表观遗传学, 药物滥用, DNA 甲基化, 非编码 RNA