Clear Sky Science · zh
Med13通过PlxnA4参与皮层神经元的放射迁移和对侧投射
单一基因如何助力构建思维大脑
大脑并非简单生长,而是逐个细胞被精确组织成层次和连接模式地建造。本研究探讨了一种名为Med13的基因如何帮助皮层中的幼年脑细胞迁移到正确位置并跨半球建立连接。因为构建过程中的细微错误越来越多地与自闭症和智力障碍等疾病相关,理解Med13提供了一个窗口,帮助我们洞察早期大脑发育如何出错。
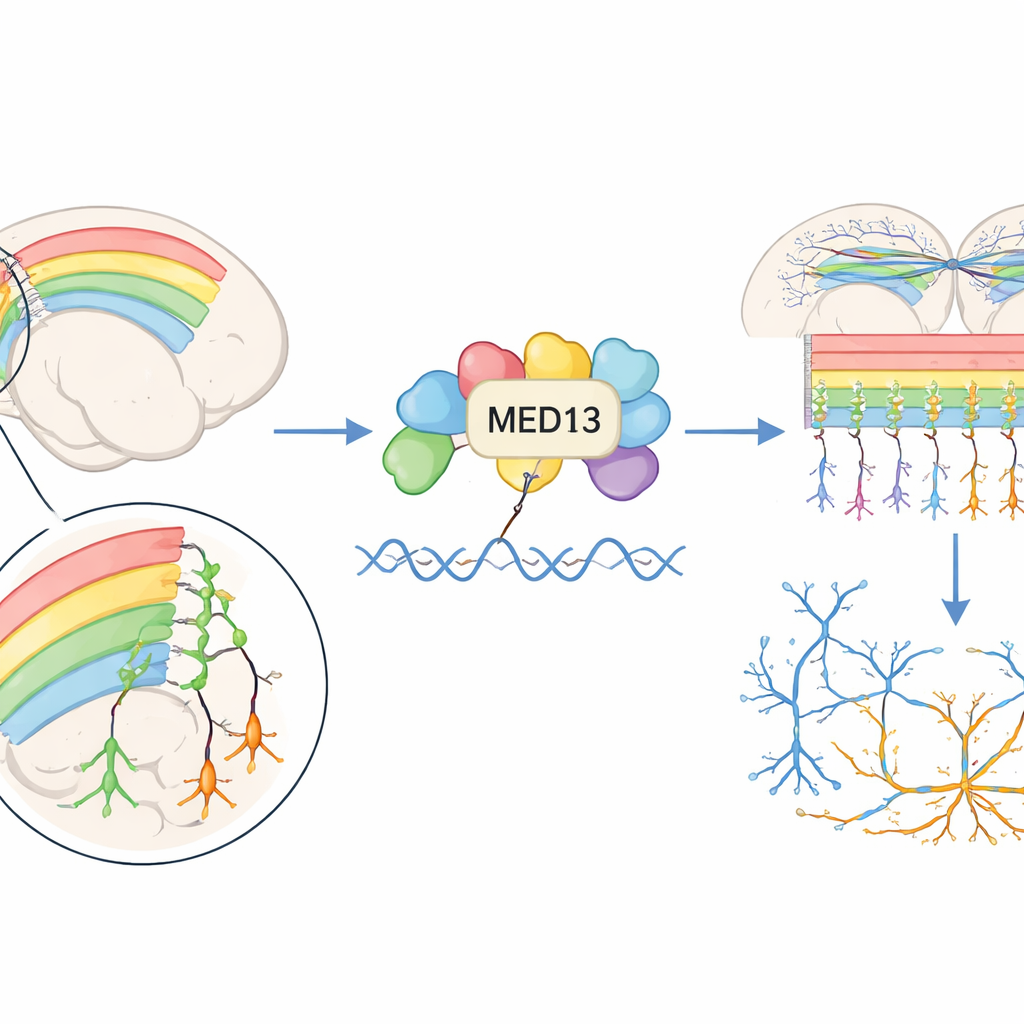
构建大脑的六层“邻里”
大脑皮层是大脑皱折的外层,胚胎期形成时组织成六层神经细胞。新生神经元在脑深处产生,然后以“由内向外”的顺序迁移形成这些层次。作者首先询问Med13在此过程中何时何地活跃。在小鼠胚胎中,Med13在神经干细胞分裂的区域和年轻神经元迁移的区域表达较高,尤其是在中期妊娠的关键时间点——许多皮层神经元产生之时。Med13既存在于分裂的前体细胞中,也存在于正在成熟的神经元中,表明它在塑造皮层方面具有广泛作用。
当神经元迷失方向
为测试Med13的实际功能,研究团队在发育中的小鼠皮层神经元中有选择性地降低其水平,使用一种向胎脑引入定制DNA的技术。被标记的缺失Med13的神经元随时间被追踪。与对照神经元相比,许多缺乏Med13的细胞在迁移途中停滞,未能到达它们所属的上层皮层。即便出生数日后,也有大部分细胞散落在更深的组织或皮层下的白质中。这些错位细胞还显示出未完全成熟的特征:部分未表达典型完全部分化上层神经元的标志物,但它们也未转变为其他细胞类型,如下层神经元或胶质细胞。这表明Med13不仅对神经元到达目的地很重要,也对其完全获得正确身份至关重要。
半球之间的桥梁断裂
正常的大脑功能依赖于神经元之间的长程连接,包括穿过胼胝体中线将左右半球连接起来的纤维。研究人员发现,缺乏Med13的神经元对对侧大脑的投射明显较差。穿透到对侧皮层适当区域的轴突减少,且这种缺陷随着发育进程愈发明显。与此同时,接收输入信号的树突“树”明显更为简单:缺乏Med13的神经元分支更少,总树突长度也更短。综合这些变化,表明Med13是决定神经元定位以及它们与配偶神经元如何丰富连接的关键组织者。
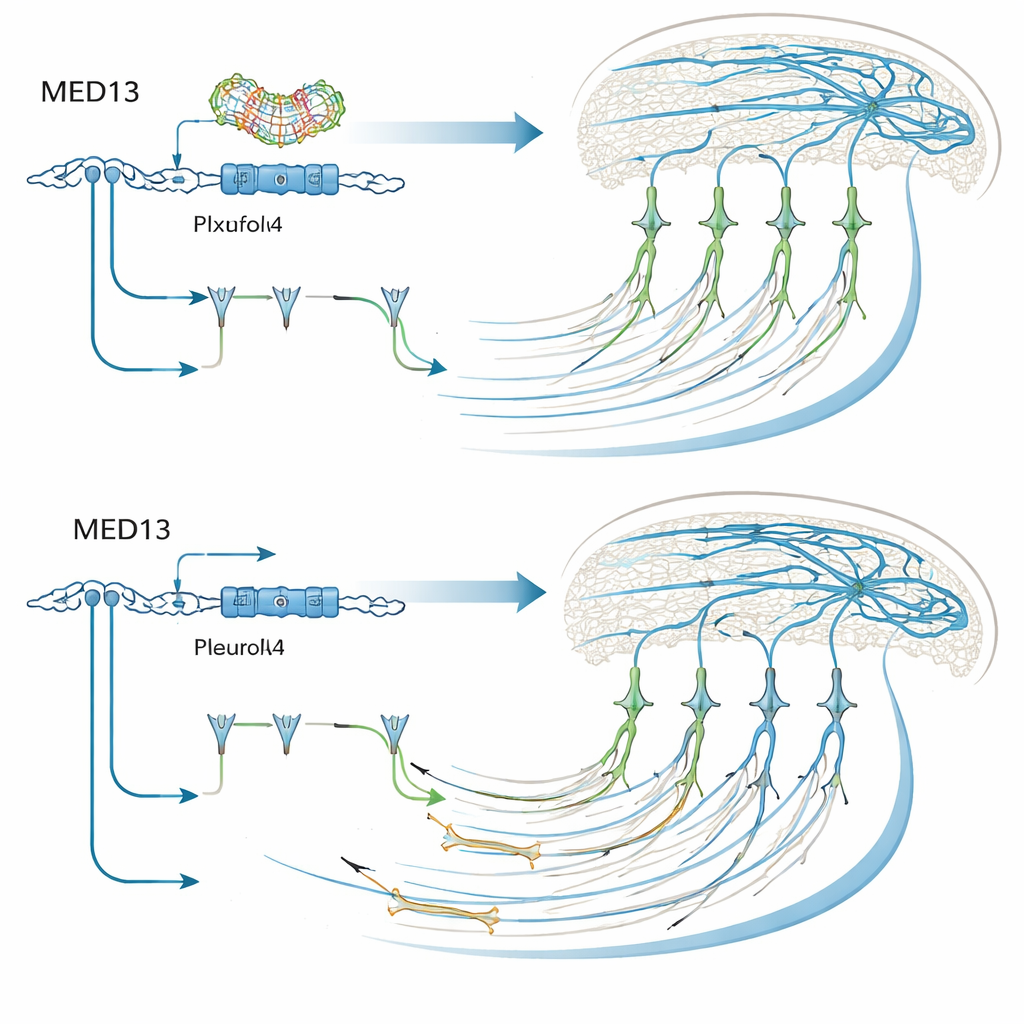
从基因控制到引导信号
Med13是一个大型蛋白复合体的一部分,该复合体控制许多其他基因的开关状态,因此作者接着寻找可能解释其效应的下游因子。在缺失MED13的人类类神经细胞中,他们编目了数千种蛋白并发现一百多种蛋白水平发生变化。许多蛋白参与神经元形态、运动和皮层发育,且若干与已知的神经发育疾病风险基因有重合。其中一个尤为显著:PlxnA4,这是一种帮助神经元对迁移和轴突延伸过程中的引导线索作出反应的受体。无论是在培养的人类细胞中还是在Med13减少的小鼠神经元中,PlxnA4水平均下降。值得注意的是,强制让神经元额外表达PlxnA4在很大程度上可以挽救它们的迁移问题并恢复多数胼胝体投射,即使在沉默Med13的情况下也是如此。然而,这并未修复简化的树突结构,暗示Med13还通过其他靶点作用以塑造神经元分支。
这对脑疾病意味着什么
综合来看,这些发现显示Med13帮助幼年皮层神经元迁入正确层次并形成长距离连接,部分机制是维持引导分子PlxnA4的表达。当Med13受损时,神经元错位、分支发育不足并向胼胝体跨送的纤维减少——这些变化与某些神经发育疾患中观察到的大脑改变相呼应。虽然显然还有许多其他基因和信号参与其中,但将Med13置于一个中心调控因子的地位,有助于更清晰地描绘早期基因改变如何向外扩展、改变大脑连线并最终影响行为的图景。
引用: Li, ZX., Tu, SX., Li, YW. et al. Med13 is involved in the radial migration and contralateral projection of cortical neurons via PlxnA4. Commun Biol 9, 394 (2026). https://doi.org/10.1038/s42003-026-09704-w
关键词: 皮层发育, 神经元迁移, 胼胝体, 神经发育障碍, 基因调控