Clear Sky Science · zh
在环境相关浓度下氯化镧暴露通过依赖PPARα的ApoB抑制在斑马鱼幼体中诱导肝脂肪变性
日常用水中的隐性风险
稀土元素为现代技术供能,从智能手机到绿色能源设备都离不开它们。其中一种元素镧,正越来越多地出现在世界各地的河流、湖泊乃至饮用水中。本研究提出了一个简单但重要的问题:在发育中的动物暴露于现实水体中检测到的镧氯化物水平时,其主要负责处理脂肪和毒素的器官——肝脏,会发生什么?研究人员利用透明且体型微小、与人类共享许多肝脏特征的斑马鱼,揭示了早期暴露如何悄然编程肝脏,导致长期的脂肪堆积和损伤。
从看似清澈的水到脂肪肝
研究团队将斑马鱼胚胎暴露于与受污染河流和水库中测得浓度相当的镧氯化物中。乍看之下,幼鱼似乎正常:它们孵化、生长并游动,几乎与未暴露的鱼无异。但当科学家放大观察肝脏时,问题显而易见。肝脏区域明显变小,显微图像显示出空泡样间隙和组织紊乱——早期损伤的典型特征。特殊的脂染色显示,暴露组鱼类肝脏中脂滴明显增多,这一状态被称为肝脂肪变性或脂肪肝。
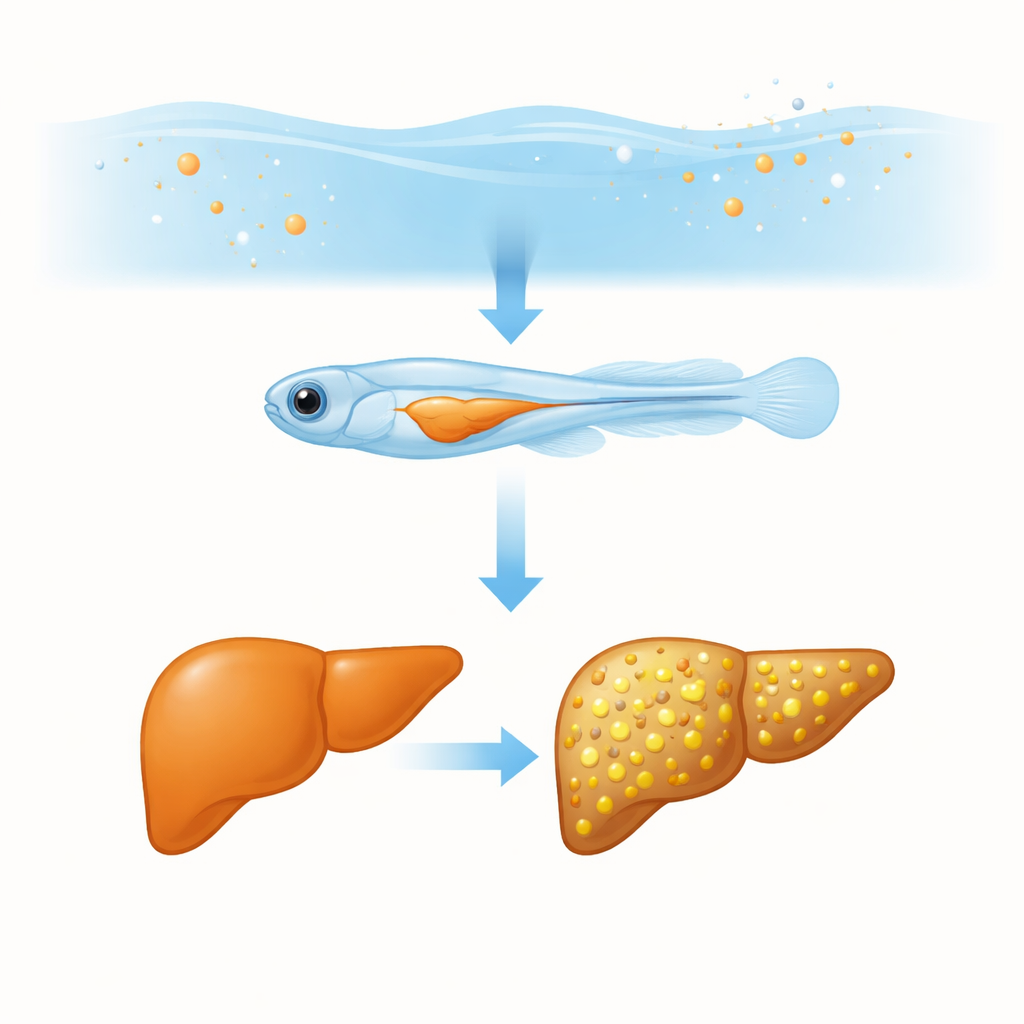
不会自行消失的损伤
最引人注目的发现之一是这种损伤的持久性。在含镧水中暴露五天后,研究者将鱼移回清水并养至成年。数月后,它们的肝脏仍显示异常脂肪积累和较低的肝体重比,尤其是在早期遭受较高镧水平的鱼中。身体的其他部分,包括总体长度和体重,表现正常。这表明发育中的肝脏特别敏感,短暂的早期暴露可能留下无法完全愈合的代谢性“伤痕”,这可能反映出人类早期化学暴露提高成年脂肪肝风险的情形。
肝脏“脂肪输出系统”如何崩溃
为了解肝脏内部出了什么问题,研究人员测量了数百种小分子和基因表达模式。他们发现一条关键的脂肪输出通路被扰乱。正常情况下,肝脏将三酰甘油——其主要储脂形式——包装进称为极低密度脂蛋白的小颗粒中,运送到身体其他部位。在镧暴露的鱼中,这些颗粒及其下游分解产物的水平下降,而三酰甘油堆积。基因表达结果指出一个核心调控因子PPAR‑α,它帮助肝脏决定何时燃烧脂肪、何时将其打包输出。镧暴露抑制了PPAR‑α的活性,并降低了构建可输出脂质颗粒所需的两个关键助剂MTTP和ApoB的水平。
肝细胞内的分子连锁反应
后续实验描绘出一条连锁反应。当科学家化学性增强PPAR‑α或在斑马鱼中人工增加MTTP时,肝脏的大小和结构有所改善,三酰甘油水平下降,携脂颗粒部分恢复——这些证据表明该通路不仅受影响,而且在病理中具有因果作用。细胞培养研究进一步放大观察。在类人肝细胞中,镧导致过量脂滴在内质网上聚集,内质网是组装脂蛋白的细胞“装配线”。同时,ApoB蛋白量下降,且更多ApoB与伴侣蛋白HSP70并列出现,后者负责将受损蛋白送往细胞的废物处理机制。阻断蛋白酶体——主要的蛋白质降解机器——可以防止ApoB减少并减轻脂肪堆积,表明镧促使ApoB过早被降解,从而在其能协助输出脂肪之前将其消耗掉。
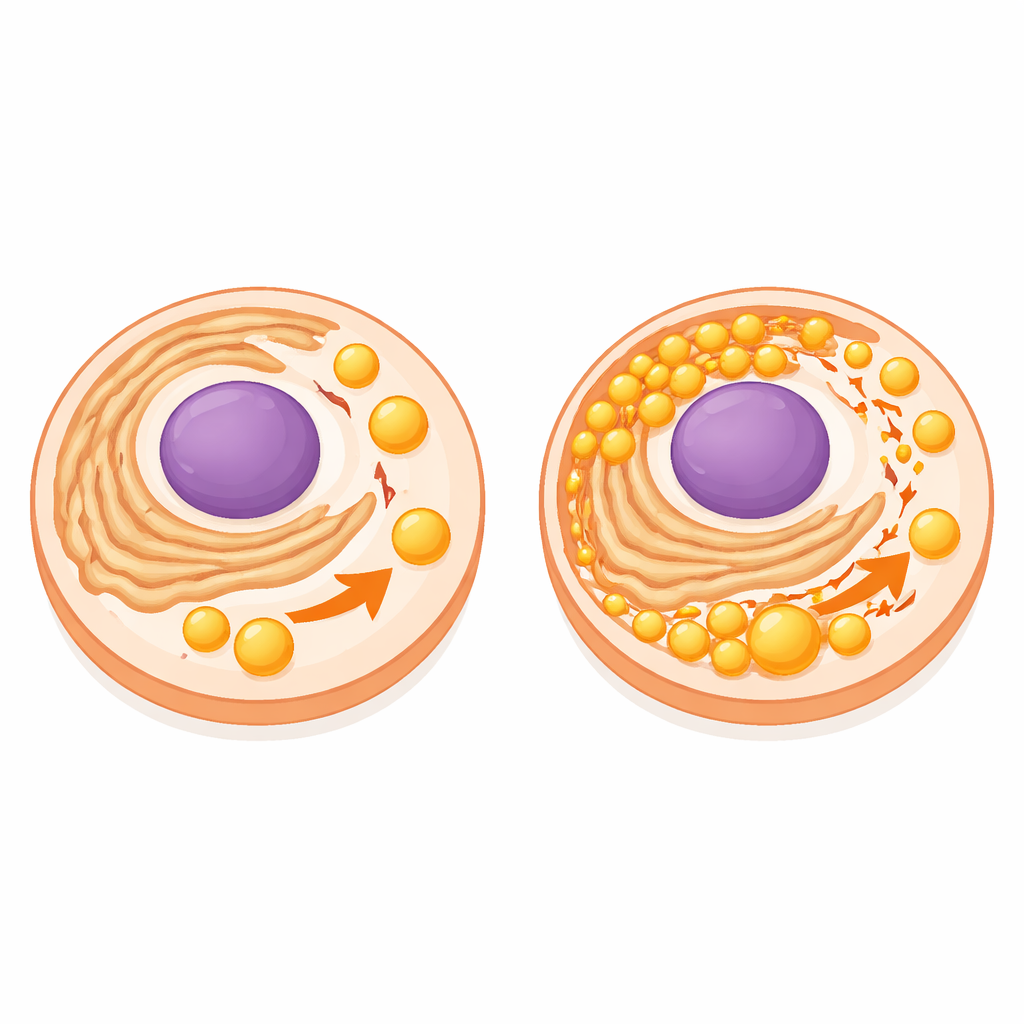
对人类与地球意味着什么
综合来看,这些发现表明,镧氯化物在一些天然水体中已经测得的浓度下,能够悄然且持久地重塑发育中肝脏处理脂肪的方式。通过削弱PPAR‑α并促进细胞内膜处ApoB的降解,镧减缓了肝脏将三酰甘油输出的能力,导致脂肪堆积并为代谢性肝病奠定基础。虽然斑马鱼并非人类,但它们与我们共享许多肝脏通路,这项工作凸显了不断上升的稀土污染可能通过此类路径增加全球脂肪肝病负担的合理性。该研究不仅将镧标记为环境与饮用水监管中值得关注的化学物质,也指向了PPAR‑α–MTTP–ApoB轴,作为未来旨在保护易感发育中肝脏的潜在治疗目标。
引用: Li, K., Zhao, X., Xie, Z. et al. Environmentally relevant lanthanum chloride exposure induces hepatic steatosis in zebrafish larvae via PPARα-dependent ApoB suppression. Commun Biol 9, 390 (2026). https://doi.org/10.1038/s42003-026-09697-6
关键词: 镧污染, 脂肪肝, 斑马鱼, 稀土元素, 脂质代谢