Clear Sky Science · zh
在丛状神经纤维瘤异种移植小鼠模型中证明 NF1 基因疗法的原理性可行性
这项研究为何重要
患有 1 型神经纤维瘤病(NF1)的人常会出现大型、致残性的神经肿瘤,称为丛状神经纤维瘤。这些肿物会导致疼痛、运动障碍并带来严重的美容问题,而现有治疗手段有限,手术常常不可行。由于 NF1 是由单个基因的改变引起,许多研究人员希望通过基因疗法——修复或替换有缺陷的基因——有朝一日使这些肿瘤缩小甚至消失。该研究在小鼠中对这一设想进行了早期但有力的检验,提出了一个简单却意义重大的问题:如果在已形成的肿瘤中恢复缺失的 NF1 基因,肿瘤会消失吗?
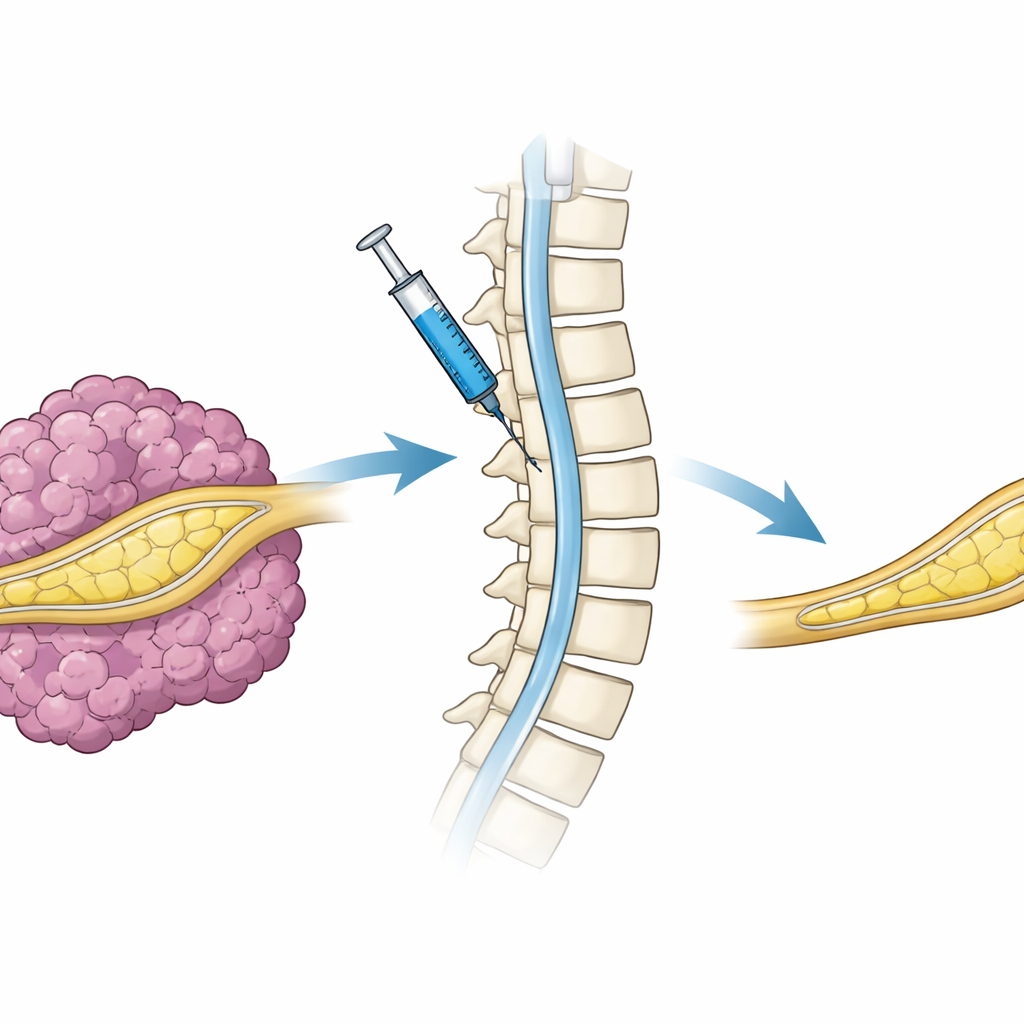
在小鼠中构建逼真的肿瘤模型
研究者首先需要一种在实验室中尽可能模拟人类丛状神经纤维瘤的体系。他们使用了来源于一位患者的人的施万细胞(Schwann cells),这些细胞已丧失了两份功能性 NF1 拷贝。研究者将这些细胞置于免疫受损小鼠的坐骨神经受伤部位附近。数周内,受试神经稳定地出现增厚、高细胞密度、结构紊乱并伴有致密胶原带的组织——这正是丛状神经纤维瘤的特征。对照手术(未植入 NF1 缺失细胞,或使用仅有一份 NF1 损伤的细胞)未能可靠地形成肿瘤。这表明,完全丧失 NF1 的人类细胞在驱动肿瘤生长方面起主导作用,并建立了一个稳健且快速的疾病模型。
在肿瘤细胞中重新开启 NF1
有了这一模型,研究团队将形成肿瘤的施万细胞工程化,使其携带一种可开关的鼠源 NF1 基因。该开关响应常用抗生素多西环素:当小鼠饮用含多西环素的水时,植入细胞中的额外 NF1 基因被激活。小鼠先被允许发展肿瘤,随后才开启该基因。结果十分显著:在 NF1 保持关闭的动物中,多数坐骨神经仍保留神经纤维瘤。相比之下,当 NF1 被重新激活时,大多数神经在显微镜下呈现正常外观,与过度活跃的生长信号相关的化学标记显著降低。本质上,重新开启 NF1 将肿瘤组织推回到更接近健康神经的状态。
以第二种方式逆转 NF1 丧失
为证明这一效应并不限于一种工程手段,科学家构建了第二种互补模型。这一次他们从仅有一份受损 NF1 拷贝的人施万细胞开始——这与 NF1 患者体内所有细胞的遗传状况相似。他们加入了一个遗传开关,使得在多西环素存在时可以暂时降低剩余的 NF1 活性。当小鼠饮用多西环素时,NF1 水平进一步下降并容易形成肿瘤。关键在于,当肿瘤形成后撤去多西环素,NF1 水平回升,许多神经向正常结构恢复。同样,那些恢复正常的神经中与生长相关的信号指标下降。两种相反的开关策略——重启 NF1 或解除对其的抑制——得出相同结论:在肿瘤细胞中恢复 NF1 可以逆转已建立的疾病。
测试更现实的递送方法
除了在体外构建在细胞内的遗传开关之外,真正的治疗需要将功能性 NF1 基因递送到活体患者的神经系统中。为探讨这一步骤,研究者将完整的 NF1 基因装入慢病毒载体,并注射到患肿瘤小鼠脊髓周围的脑脊液空间,这一途径称为蛛网膜下或池内递送(intrathecal delivery)。动物随后接受多西环素以激活所递送的基因。与接受对照病毒的小鼠相比,接受携带 NF1 病毒处理的动物形成的肿瘤明显更少,且其神经组织外观更接近正常。尽管这是一次短期、单剂量的实验,但结果表明通过脊髓液递送 NF1 基因可以到达周围神经并显著减轻肿瘤负担。
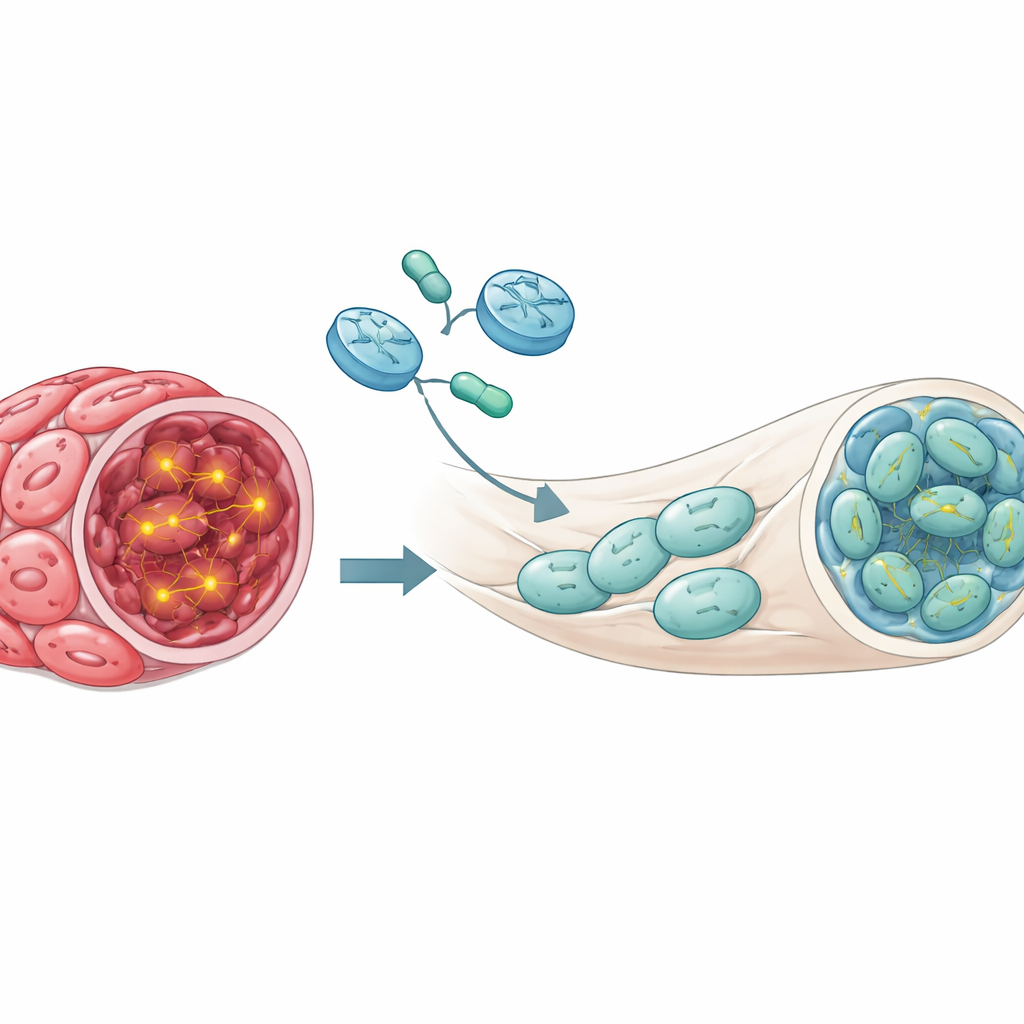
这项工作对 NF1 患者意味着什么
该研究尚不能直接为患者提供可用的治疗方案,但它回答了一个关键问题:在仔细设计并与人类丛状神经纤维瘤高度相似的小鼠模型中,在肿瘤细胞中恢复 NF1 可以使已形成的肿瘤缩小或恢复正常。该工作为 NF1 基因疗法作为一种切实可行的策略提供了原理性证据,而不仅仅是理论上的希望。仍存在许多挑战——需要寻找更安全、更高效的递送载体,确定多少 NF1 活性才足够,以及在更自然的模型中测试长期效应等。但这些结果为未来基于基因的治疗奠定了科学基础,可能有一天为 NF1 患者带来持久缓解丛状神经纤维瘤的希望。
引用: Hewa Bostanthirige, D., Plante, C., Caron, M. et al. Proof-of-principle of NF1 gene therapy in plexiform neurofibroma xenograft mouse models. Commun Biol 9, 419 (2026). https://doi.org/10.1038/s42003-026-09695-8
关键词: 1 型神经纤维瘤病, 基因疗法, 丛状神经纤维瘤, 施万细胞, 慢病毒递送