Clear Sky Science · zh
线粒体能量衰竭是FLVCR1相关感觉性神经病变的病因
当疼痛神经耗尽能量时
有些人生来几乎感觉不到疼痛。乍看之下这似乎是福气,但很快会变成祸端:没有疼痛这一预警信号,他们会不断累积烧伤、骨折、感染甚至失明。本研究调查了一种罕见的失痛疾病,并揭示了一个出人意料的罪魁祸首:神经细胞内体积微小的“发电厂”——线粒体,其能量产生出现严重紊乱。
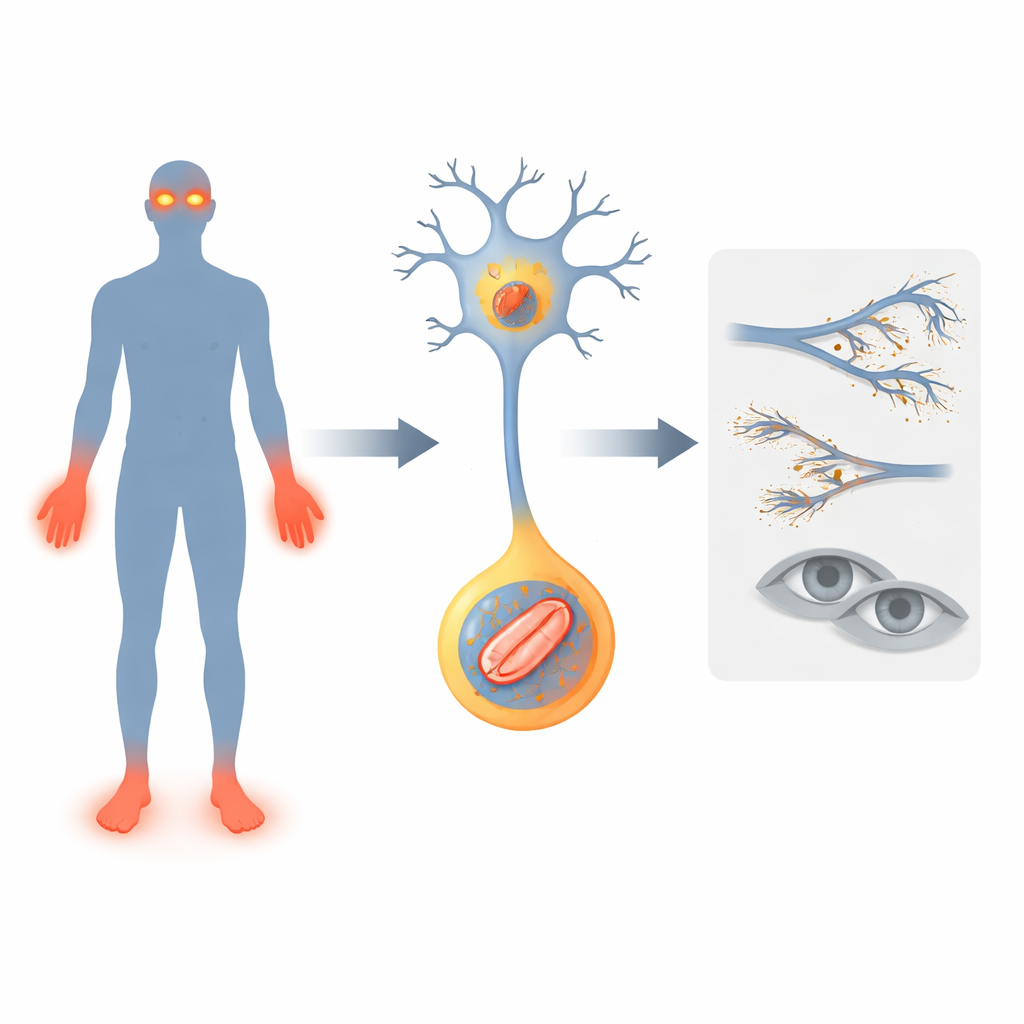
让警报沉默的基因
研究者聚焦于一个名为FLVCR1的基因,该基因已与罕见的失痛性疾病相关联,这些疾病表现为痛觉丧失、步态不稳,有时伴随进行性视力丧失。文章描述了两例新的FLVCR1变异患者。两名儿童均出现早期问题:运动发育迟缓、频繁跌倒、反复严重感染以及由于感觉缺失导致手指和脚趾的截伤。一名患者还出现了称为视网膜色素变性(retinitis pigmentosa)的进行性眼病,导致夜盲。这些病例拓宽了FLVCR1缺陷在人类中的表现谱,并强化了该基因对维持痛觉神经和视网膜光感受细胞存活的重要性。
在小鱼中模拟疾病
为探查FLVCR1如何影响发育中的感觉神经,团队转向斑马鱼,其透明胚胎便于直接观察神经细胞。研究者用基因手段降低了鱼类对应基因flvcr1a的表达。flvcr1a下降的鱼类背根神经节(检测触觉和疼痛的一组脊柱旁神经元簇)数量减少。在行为上,这些鱼自主活动减少,尾部轻触时只游动短距离,提示感觉反应减弱。由于早期小鼠模型在分析感觉神经前即早逝,斑马鱼为首次在活体系统中详细追踪FLVCR1相关的神经缺陷和行为提供了可能。
三条受损通路在细胞“发电厂”处交汇
FLVCR1位于细胞膜上,管理多种关键物质。既往研究提示其在胆碱(构成膜类脂分子的前体)、血红素(许多酶的含铁辅基)和细胞器间钙流动的处理上发挥作用。研究者从四名携带不同FLVCR1突变的患者采集皮肤成纤维细胞,并与健康个体和无症状携带者的细胞比较。结果显示,患者细胞胆碱水平下降、细胞膜更流动,这些改变可能扰乱线粒体所需的精细脂质环境。他们还发现,线粒体内合成血红素的关键酶ALAS1活性降低,尽管总体血红素含量看起来几乎正常。同时,内质网与线粒体之间的物理接触位点变短且减少,线粒体的钙摄取也减少。胆碱短缺、血红素合成迟缓和钙传递受弱化这三方面的问题都指向线粒体功能受损。
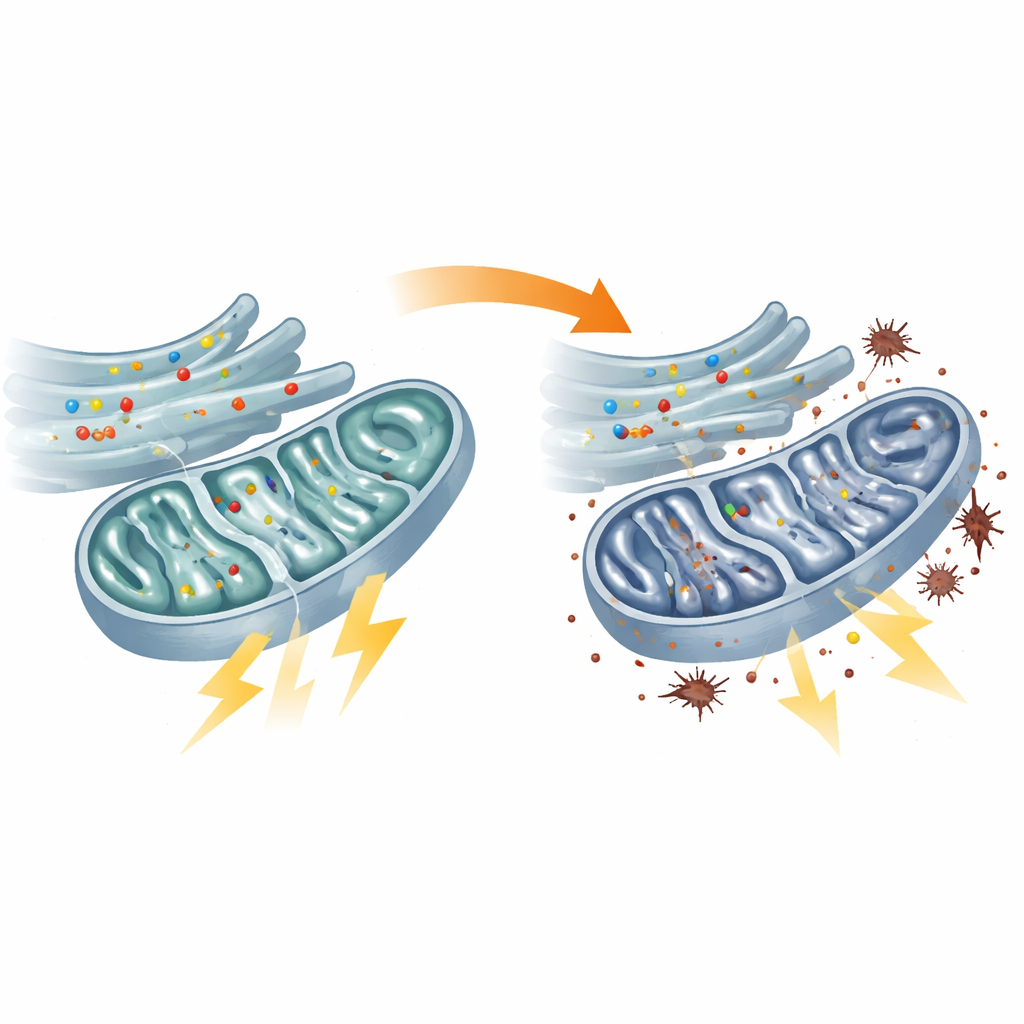
被饿扁的线粒体与过劳的备用系统
对能量代谢的直接检测证实患者成纤维细胞中的线粒体功能不佳。被称为三羧酸(TCA)循环的核心燃料处理枢纽运行减慢,其若干关键酶活性下降,通常将燃料转化为ATP(细胞能量货币)的呼吸链反应受抑。结果,线粒体内ATP水平下降。细胞试图通过提高无氧糖酵解(线粒体外较低效的糖类代谢途径)来补偿。这一能量策略的转变带来了代价:受压的线粒体机械中电子泄漏,触发更高水平的脂质过氧化——对细胞膜的氧化损伤。在flvcr1a表达降低的斑马鱼中也观察到了类似缺陷,将线粒体功能衰竭直接与该感觉性神经病的动物模型联系起来。
通过增强细胞能量的潜在治疗线索
令人鼓舞的是,在实验室中部分缺陷可以被缓解。当研究者通过过度表达一种名为MCU的通道蛋白来人为增加线粒体内的钙进入时,患者细胞的能量产生恢复,氧化损伤迹象下降。向细胞补充血红素前体5-氨基乙酰丙酸(ALA)也改善了TCA循环活性、呼吸链功能和ATP水平,尽管既往研究提示长期暴露于ALA可能有害。额外的胆碱可以使膜流动性恢复正常并有助于减少脂质损伤,但对能量产出的短期提升仅属有限。这些“救援”实验表明并无单一通路独立负责;相反,胆碱、血红素和钙处理网络的协同紊乱使线粒体陷入长期低效状态。
这些发现为何对患者重要
通过将FLVCR1突变的影响从分子层面追溯到细胞再到整体生物体,这项工作提出线粒体能量衰竭是该型失痛性神经病及其相关视力问题的推动力。感觉神经和光感受器因需维持长轴突或不断更新光敏结构而对能量需求异常高,这使得当线粒体产能下降时它们尤为脆弱。该研究所建立的斑马鱼模型与患者来源细胞为测试增强线粒体代谢的治疗方案提供了可行平台。尽管诸如胆碱补充、受控的血红素提升或增强线粒体钙摄取的药物等治疗策略仍需在动物模型和临床试验中谨慎评估,但核心信息明确:恢复脆弱神经的能量供应,或许有一天能帮助保护那些天生缺乏自然最重要警示信号——疼痛的人们。
引用: Bertino, F., Zanin Venturini, D.I., Grasso, E. et al. Mitochondrial energetic failure underlies FLVCR1-related sensory neuropathy. Commun Biol 9, 429 (2026). https://doi.org/10.1038/s42003-026-09691-y
关键词: 感觉性神经病变, 线粒体功能障碍, FLVCR1, 疼痛迟钝, 神经能量代谢