Clear Sky Science · zh
在新冠猴模型中观察SARS-CoV-2变体的病理特征及诱导的免疫反应
这项研究与日常生活的关联
导致COVID-19的冠状病毒不断变化,先后引发了由Alpha、Delta、Omicron及其他变体主导的流行浪潮。许多人即使在接种疫苗或既往感染后,仍然出现重复感染。本研究使用类COVID-19疾病的猕猴模型,直面两个与人类直接相关的问题:不同变体在体内如何表现,以及早期与病毒的接触如何影响对后续变体的免疫反应?
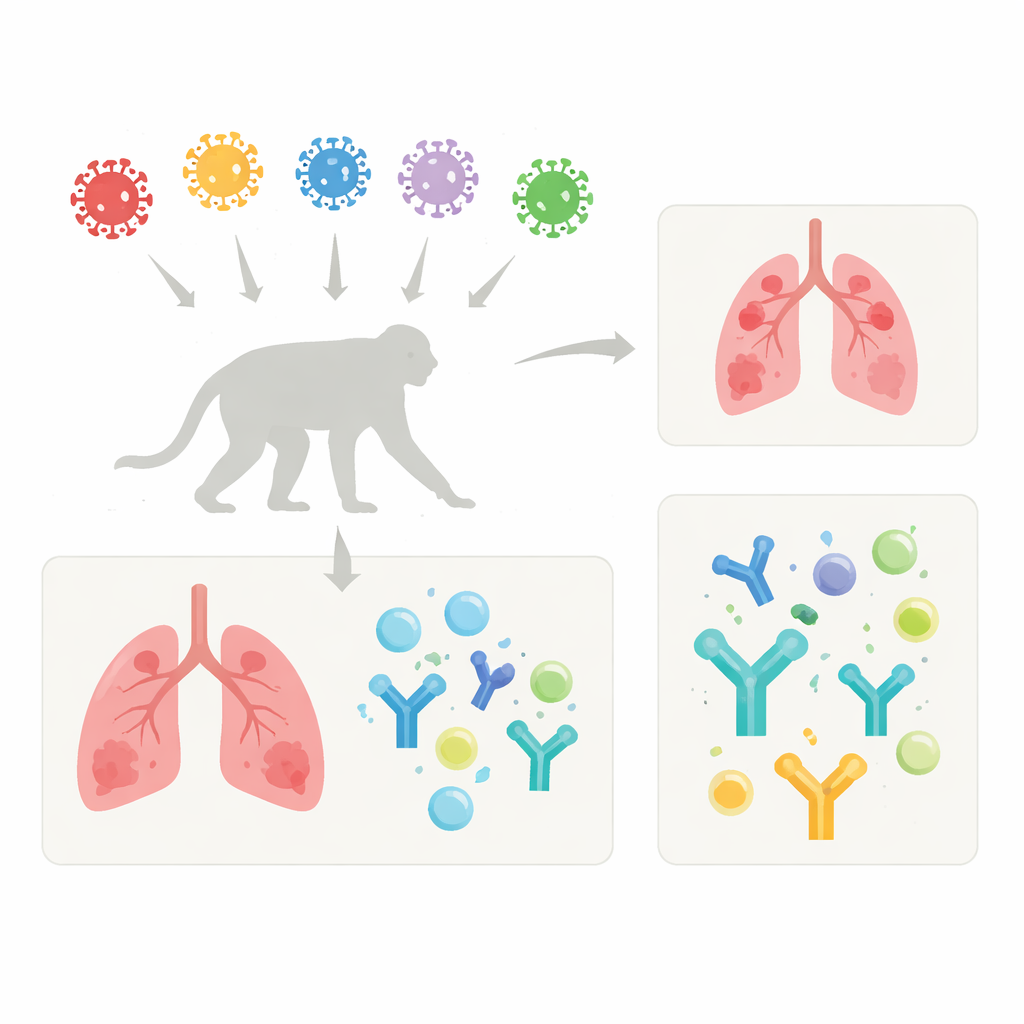
追踪变体在体内的表现
研究者用原始武汉株和六个主要变体(Alpha、Beta、Gamma、Delta,以及Omicron BA.1和BA.2)感染了长尾猕猴,这种猴子的COVID-19样症状类似于人的轻症。所有动物都接受了相同剂量的气管内给药,以便公平比较感染情形。猴子仅表现出轻微且短暂的病征,如短暂发热和食欲变化,体重保持稳定。炎症血液标志物C反应蛋白在感染后升高,但在Omicron感染时通常较低,提示这些更近期的变体相比早期变体引起的全身炎症程度较小。
病毒复制速度与肺部受影响程度
研究组反复采集猴子的鼻拭子和咽拭子,追踪病毒排放量及持续时间。Delta尤为显著:其达到最高的病毒水平并持续时间最长,尤其在反映下呼吸道病毒增长的咽拭子中。相比之下,Omicron BA.1和BA.2在鼻拭子中几乎难以检测,总体复制显著较低,支持Omicron不太适合感染深部肺组织的观点。胸部CT扫描证实了这一模式。早期变体,特别是Gamma和Delta,经常产生清晰的肺炎斑片,而Omicron感染则引起更轻、更局限的肺部改变,与临床上人群中通常观察到的较轻疾病一致。
二次感染与意外的肺炎
为了模拟现实世界的再感染情形,部分猴子在首次感染近三个月后再次暴露于相同或不同的变体。当第二次暴露使用Delta时,所有动物短暂地在PCR检测中再次呈阳性,表明可发生再感染,但没有动物发展为肺炎;既有免疫似乎限制了损害,即便不能完全阻止病毒。Omicron的表现则不同。再次暴露于Omicron时只有大约一半的猴子PCR呈阳性,然而在第二次暴露后出现肺炎的动物全都在第二次接触时接触到了Omicron毒株。在这些病例中,组织中几乎找不到或完全找不到可培养的活病毒,提示肺部炎症不仅由体内病毒载量决定,也与免疫系统先前如何被致敏有关。
免疫记忆与首发株的牵引力
科学家们仔细检查了抗体和T细胞——适应性免疫的两大支柱。感染武汉原株或Delta后,猴子产生了强有力的抗体,这些抗体能识别原始毒株及若干早期变体。然而,即使Omicron本身引起了感染,针对Omicron关键表面区域的高亲和力抗体也较弱且出现较慢。相反,免疫系统反复倾向于产生针对原始武汉样刺突蛋白的反应,这种模式被称为“原始抗原印记”(original antigenic sin),即机体首次遇到的病毒版本会对后续反应留下持久印记。对Omicron的T细胞反应总体也弱于对早期变体的反应,尤其在仅经历一次Omicron感染后,这进一步描绘出一种尽管传播能力强但炎症性和免疫可见性较低的变体形象。
对未来疫苗与保护的意义
简而言之,这项研究显示并非所有COVID-19变体在体内表现相同。Delta在体内强烈复制并能引起严重肺部疾病,但也能诱导强劲且交叉反应的免疫。Omicron在肺内复制较差、致病性较轻,但对免疫系统的教育作用也较差,尤其当早期接触过武汉样病毒使抗体反应不断回归到原始株时。从长远看,这种印记效应和Omicron低免疫原性可能有助于解释为何Omicron浪潮及其子变体持续出现。这些来自经过严格对照的猴模型的发现,支持以当前流行的暴发株为重点的疫苗策略,同时也须认识到全球大多数免疫记忆仍指向病毒的首个版本。
引用: Urano, E., Okamura, T., Higuchi, M. et al. Pathological characteristics of SARS-CoV-2 variants and immune responses induced in a COVID-19 macaque model. Commun Biol 9, 426 (2026). https://doi.org/10.1038/s42003-026-09684-x
关键词: SARS-CoV-2变体, Omicron免疫, COVID-19再感染, 原始抗原印记, 猴模型