Clear Sky Science · zh
赖氨酸丙二酰化调控人类精子运动能力
为什么精子的运动很重要
对于许多面临不明原因不育的夫妇来说,一个关键的隐藏问题是精子游动能力不足,无法到达并受精卵子。本研究探讨了精子蛋白上一种微妙的化学“标签”——赖氨酸丙二酰化,这种修饰似乎像看不见的刹车一样抑制精子的运动。通过揭示这种标签如何改变精子的能量供应和细胞内信号,该研究指向了新的诊断方法和潜在治疗途径,针对与精子运动能力差相关的常见男性不育类型。
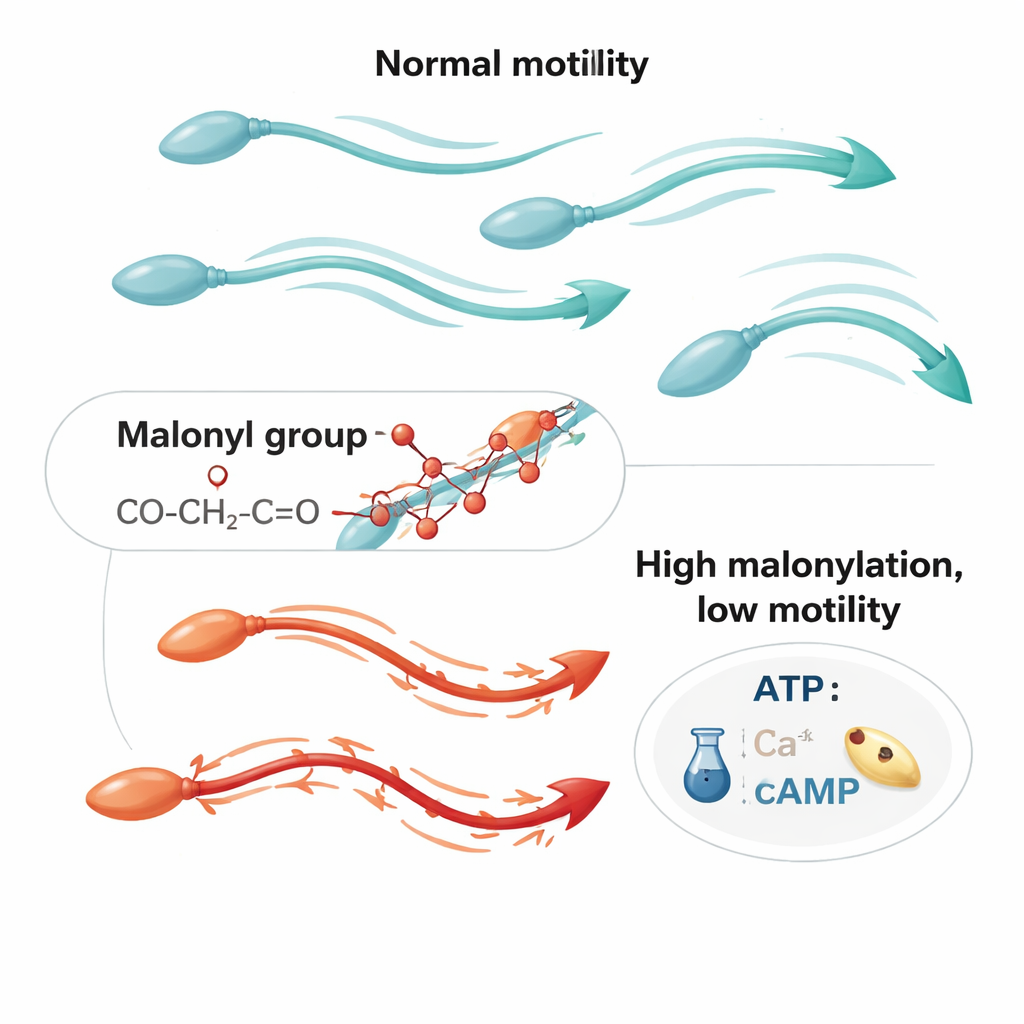
精子蛋白上的新化学标签
细胞内的蛋白质在合成后常常会被修饰,附加小的化学基团以开启或关闭其活性。其中一种修饰——赖氨酸丙二酰化于2011年被发现,并已在多种细胞类型中与能量代谢相关联。作者此前发现人类精子携带大量丙二酰化蛋白,但其对生育力的意义尚不清楚。在这项新研究中,他们绘制了该标签在精子中的分布图,发现其在精子尾部高度富集——尾部是通过节律性摆动驱动前进的长鞭状结构。结合生化检测与高分辨率显微镜,他们显示丙二酰化蛋白在尾部的线粒体及其周围液体中尤其丰富,这些区域是能量产生和运动控制的关键位点。
谁添加与移除这个“刹车”
研究团队接着探究哪些分子在人体精子中安装和去除这一丙二酰标签。他们发现一种称为P300的酶可能充当“写入者”,帮助将丙二酰基转移到赖氨酸残基上,而另一种酶SIRT5则充当“擦除者”,将其去除。当他们用化学抑制剂阻断SIRT5时,整体丙二酰化水平上升;抑制P300则使丙二酰化下降。他们还表明,马来酸钠(一种小分子,可被精子摄取并转化为丙二酰辅酶A)能在不扰动其他相似化学标记的情况下提高丙二酰化。总体上,这些结果勾画出一个调控体系:丙二酰辅酶A提供标签,P300将其附着,SIRT5将其去除——精细调控那些控制运动的精子尾部蛋白。
活动能力差的精子具有更高的丙二酰化水平
为了解该化学变化是否与临床不育有关,研究人员比较了正常精液指标男性与被诊断为弱精子症(以进行性运动能力差为特征)男性的精子。弱精子症组的精子显示出明显更高的赖氨酸丙二酰化水平和更低的SIRT5水平。在所有样本中,丙二酰化越多与向前游动能力越差以及细胞ATP(主要能量货币)减少高度相关。在一部分丙二酰化特别高的男性样本中,精子显示出明显减弱的糖酵解——这是为人类精子运动提供大量燃料的燃糖途径。这些模式表明,过度的丙二酰化与能量产生受损和游动性能下降有关。
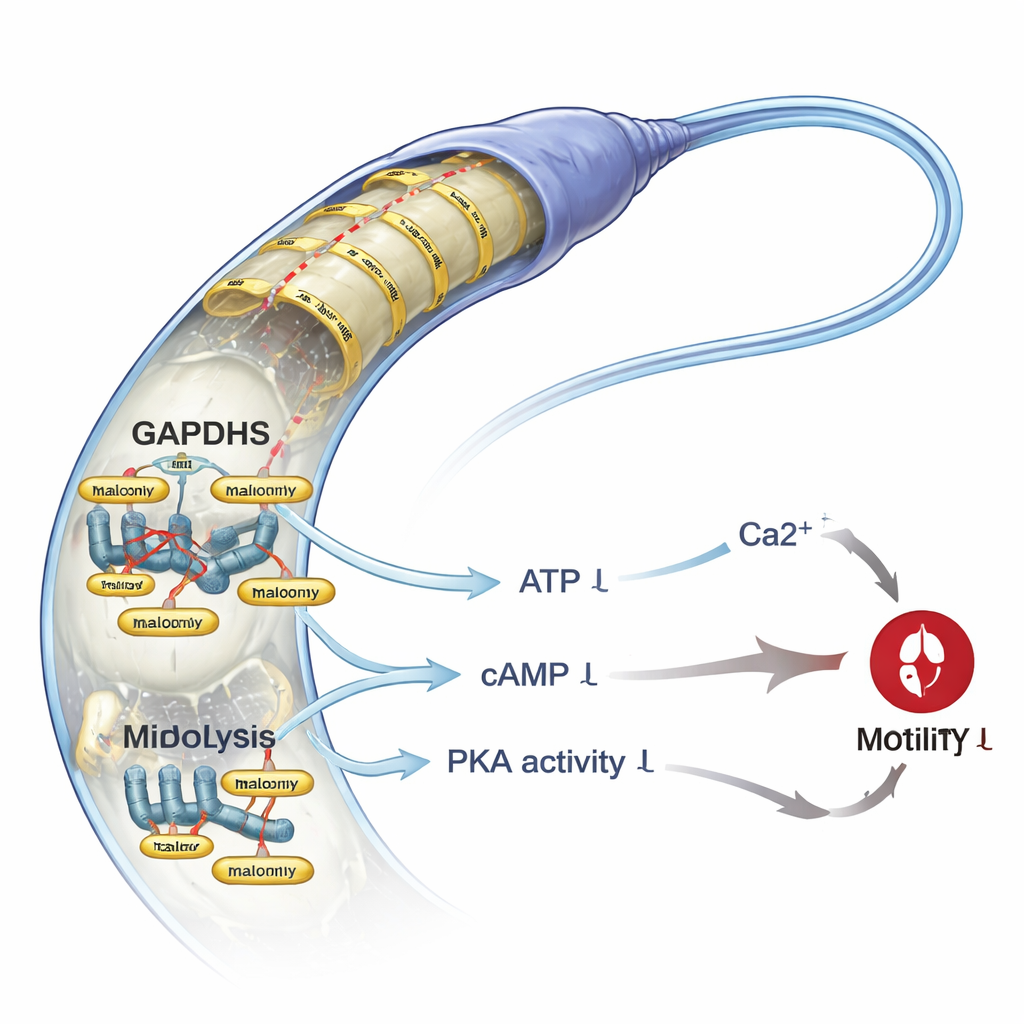
实验性地加大“刹车”
科学家们接着探问,如果在本来健康的精子中故意提高丙二酰化会怎样。用马来酸钠处理来自精液参数正常男性的样本,确实增加了丙二酰化水平,但并未杀死细胞。然而,这样处理显著降低了总运动率和进行性运动率,并使精子穿透模拟女性生殖道的高粘度介质变得更困难。机制学检测揭示了原因:马来酸钠处理的精子糖酵解产出减少、ATP下降、以及cAMP(一种激活关键酶PKA的信使)含量减少。PKA活性下降,下游支持运动的蛋白磷酸化水平也随之下降。与此同时,精子内钙浓度约降低一半,尽管主要的精子钙通道CatSper并未被直接影响。这种能量不足、信号减弱和钙减少的组合,为观察到的运动力丧失提供了连贯的解释。
从分子标签到男性生育力
综合所有发现,该研究提出赖氨酸丙二酰化作为人类精子运动能力的负调控因子。当丙二酰化水平上升——无论是因为SIRT5低、丙二酰辅酶A偏高或相关通路受扰——推动糖酵解和钙处理的关键蛋白,如GAPDHS和VDAC3,会被过度标记。这抑制了能量产生和精子尾部的关键信号级联,导致游动缓慢和穿透高粘度液体的能力下降。对非专业读者来说,信息是:精子不仅需要充足的数量;它们还依赖精细调控的化学控制系统来驱动游动。像丙二酰化这样小而可逆的标签受扰,可能助长本应不明原因的男性不育,并最终为开发恢复精子活力的生物标记物或治疗靶点提供新途径。
引用: Cheng, Y., Tian, Y., Chen, H. et al. Lysine malonylation regulates human sperm motility. Commun Biol 9, 178 (2026). https://doi.org/10.1038/s42003-026-09683-y
关键词: 精子运动能力, 男性不育, 翻译后修饰, 赖氨酸丙二酰化, 能量代谢