Clear Sky Science · zh
蝙蝠受体被SARS-CoV-2及其蝙蝠SARS2样冠状病毒识别的结构基础
为什么这个蝙蝠—病毒故事仍然重要
新冠疫情始于六年多前,尽管如此,科学家们仍在拼凑导致引发疫情的病毒(SARS-CoV-2)如何变得如此善于感染人的全貌。一个核心难题是,这种病毒及其在蝙蝠中发现的近缘病毒如何附着在细胞表面的ACE2蛋白上——这是感染的第一步,也是至关重要的一步。理解这些微观的“钥匙—锁”相互作用有助于弄清病毒的来源、它如何适应新宿主,以及将来相关病毒若进入人类可能会发生什么。
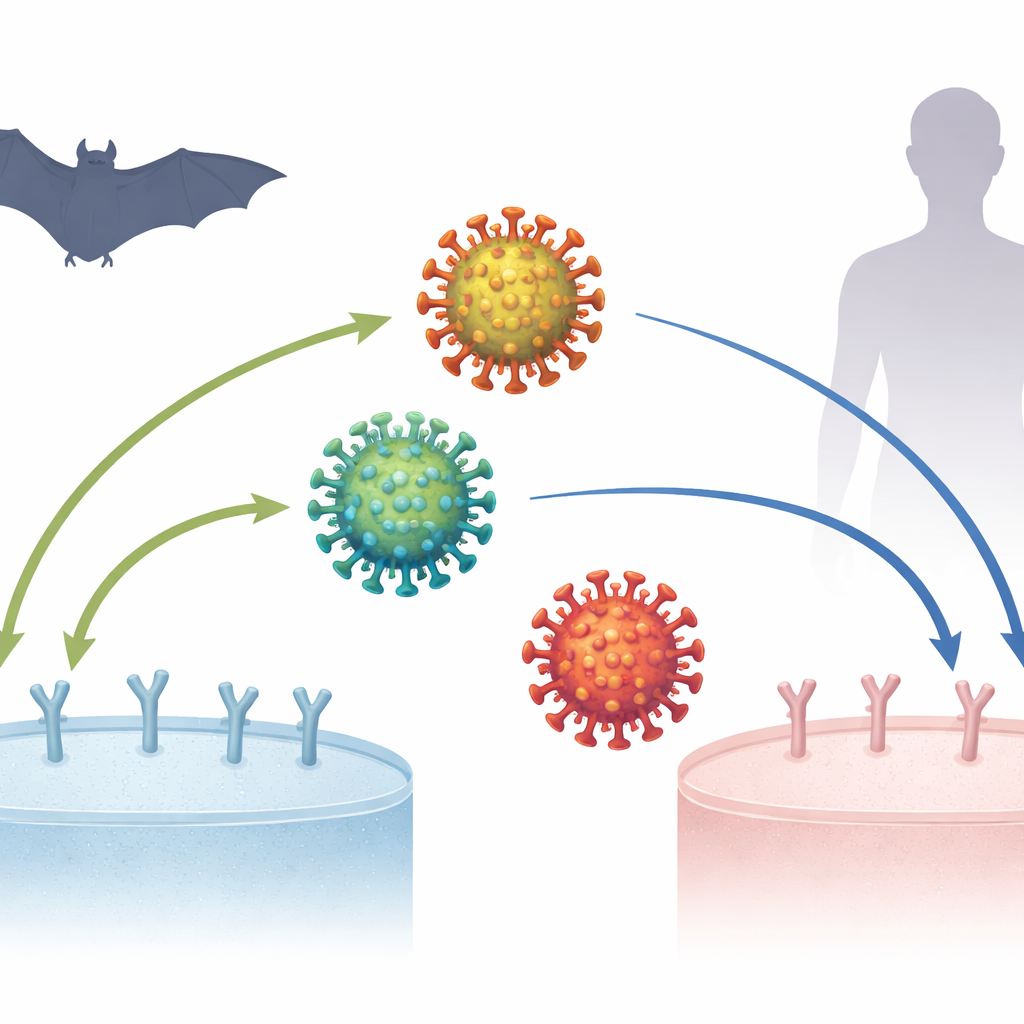
观察病毒的“握手”
研究聚焦于刺突蛋白——覆盖在病毒表面的冠状结构,用以抓住ACE2。刺突上的一个小片段,称为受体结合域(RBD),像指尖一样紧握ACE2这把“门把”。先前的工作表明,当冠状病毒跨物种传播(例如从蝙蝠到灵猫再到人)时,RBD通常会获得一些突变,从而改善它与新宿主ACE2的结合能力。但SARS-CoV-2带来了一道谜题:其原始形式在很短的时间内就已经能非常有效地结合人ACE2,有些与SARS-CoV-2相关的蝙蝠病毒似乎对人ACE2的结合甚至比对蝙蝠ACE2更强。这引发了有人怀疑SARS-CoV-2是否是对常规进化规则的例外。
将蝙蝠与人受体放在显微镜下检验
为了解开这一谜团,研究者检查了两种与SARS-CoV-2密切相关的蝙蝠冠状病毒,称为BANAL-52和BANAL-236。他们比较了这些病毒及SARS-CoV-2的RBD与来自人类及若干蝙蝠物种的ACE2结合强度。通过细胞结合测定、高精度生物传感器测量以及使用无害“伪病毒”的感染试验,他们发现了一个明确的模式。BANAL-52的RBD与一种蝙蝠(Rhinolophus sinicus)的ACE2结合最强,与人ACE2结合略弱。相比之下,SARS-CoV-2的RBD对人ACE2表现出对人类受体的适度偏好。总体而言,BANAL-52的RBD对蝙蝠和人受体的结合都比SARS-CoV-2更紧密,但它对该特定蝙蝠ACE2的适配最为精细。
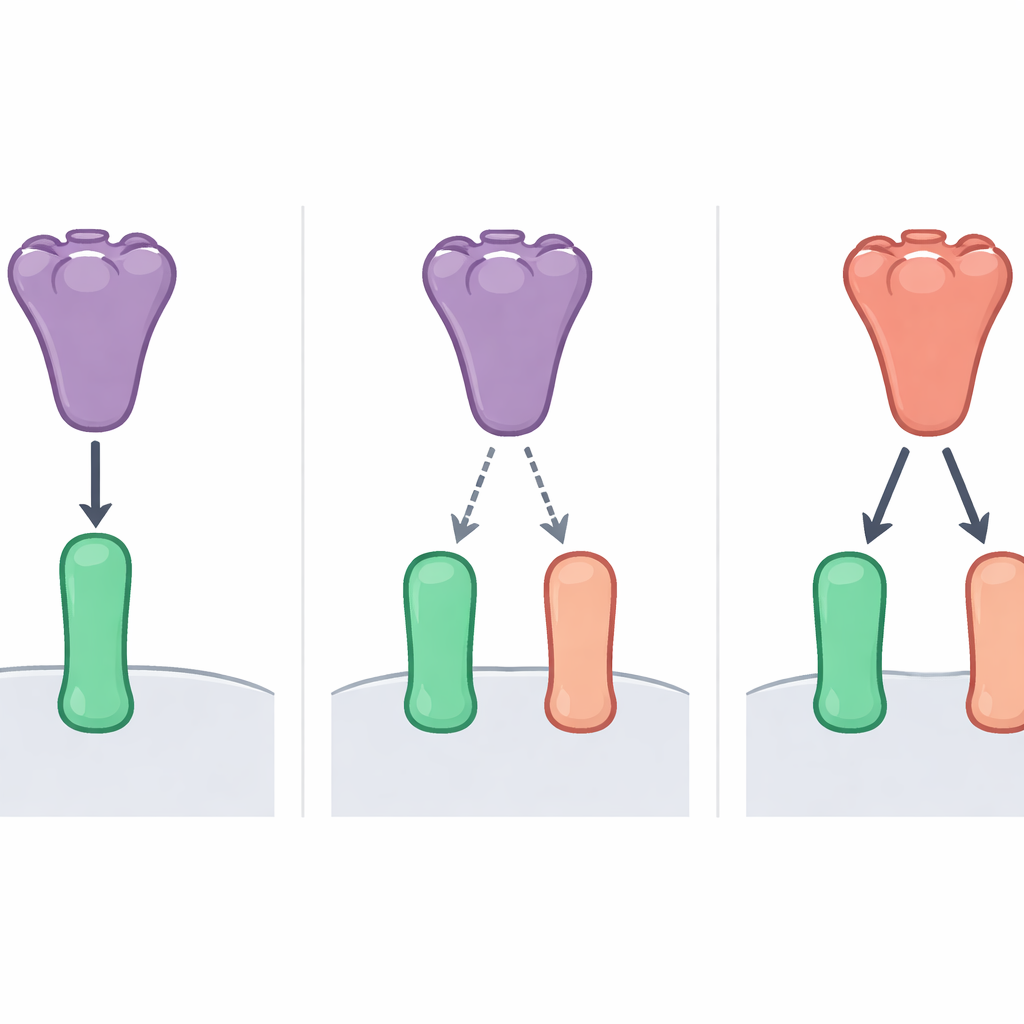
单个原子尺度微调如何改变天平
团队随后使用X射线晶体学(可揭示原子级结构)来查看病毒“指尖”与ACE2“门把”如何接触。他们关注两个关键位点:病毒RBD上的一个位点(称为残基498)和ACE2上的一个位点(残基41)。在BANAL-52中,病毒位点与蝙蝠ACE2位点均用的是同一种构件组分——组氨酸,这允许一种非常紧密的层叠相互作用——像两枚叠放的硬币,并且还能形成氢键。在人ACE2中,同一位置为结构相近但略有不同的酪氨酸,它虽然仍能与BANAL-52的组氨酸发生层叠,但缺少额外的氢键。SARS-CoV-2在该病毒位点上则使用谷氨酰胺,这种氨基酸无法以相同方式层叠,因而导致与蝙蝠和人ACE2的结合更弱。通过有意替换蝙蝠ACE2中的这些氨基酸,研究者证实增强或削弱这一接触点就能翻转对哪种病毒或宿主更有利。
为何人ACE2是如此“欢迎”的门径
除了这一单一接触点外,作者还探究了为何总体上人ACE2是冠状病毒如此高效的入口。将蝙蝠和人ACE2并列比较,他们锁定了几处人类特有的特征,这些特征改善了病毒的“握手”。人ACE2的两个位点含有组氨酸(34位)和蛋氨酸(82位),它们形成更强的氢键和疏水性的“补丁”,有助于RBD更牢固地嵌入。另一处人类残基(27位的苏氨酸)实际上使结合较之蝙蝠版本略微变弱,但总体上更多有利接触占上风。这些细节与早期工作一致,表明人ACE2具有多个“热点”,天然地使其成为对多种冠状病毒有吸引力的受体。
重新审视起源叙事
综合所有数据,这项研究认为SARS-CoV-2及其蝙蝠近缘仍然遵循常见的进化剧本。BANAL-52的刺突似乎最适合某些蝙蝠的ACE2,同时也能兼容人ACE2;而SARS-CoV-2的刺突反过来更偏向于人ACE2,这受到人类受体上若干特殊接触点的帮助。少数位点的微小变化——尤其是病毒残基498及其相邻位点——就能改变哪个宿主更受青睐。对于非专业读者而言,结论是没有必要诉诸离奇的解释:蛋白质—蛋白质相互作用的标准、可理解的结构学原理足以解释这些病毒如何识别蝙蝠和人类细胞,并且支持SARS-CoV-2与相关蝙蝠冠状病毒之间的紧密进化联系。
引用: Hsueh, FC., Shi, K., Aihara, H. et al. Structural basis for bat receptor recognition by SARS-CoV-2 and bat SARS2-like coronaviruses. Commun Biol 9, 398 (2026). https://doi.org/10.1038/s42003-026-09682-z
关键词: SARS-CoV-2 进化, 蝙蝠冠状病毒, ACE2 受体, 病毒宿主范围, 刺突蛋白结合