Clear Sky Science · zh
非洲猪瘟病毒编码蛋白 MGF 505–3R 通过泛素介导的 MyD88 降解损伤先天免疫
为何这对动物健康及更广泛领域重要
非洲猪瘟已席卷全球猪场,威胁粮食供应并造成巨额经济损失。该病病毒致命的部分原因是它能绕过机体的早期警报系统。本研究揭示了一种名为 MGF 505–3R 的病毒蛋白如何悄然破坏细胞内的关键报警开关,并表明这段蛋白的一个微小片段在小鼠中也可被转化为一种强效的抗炎工具。
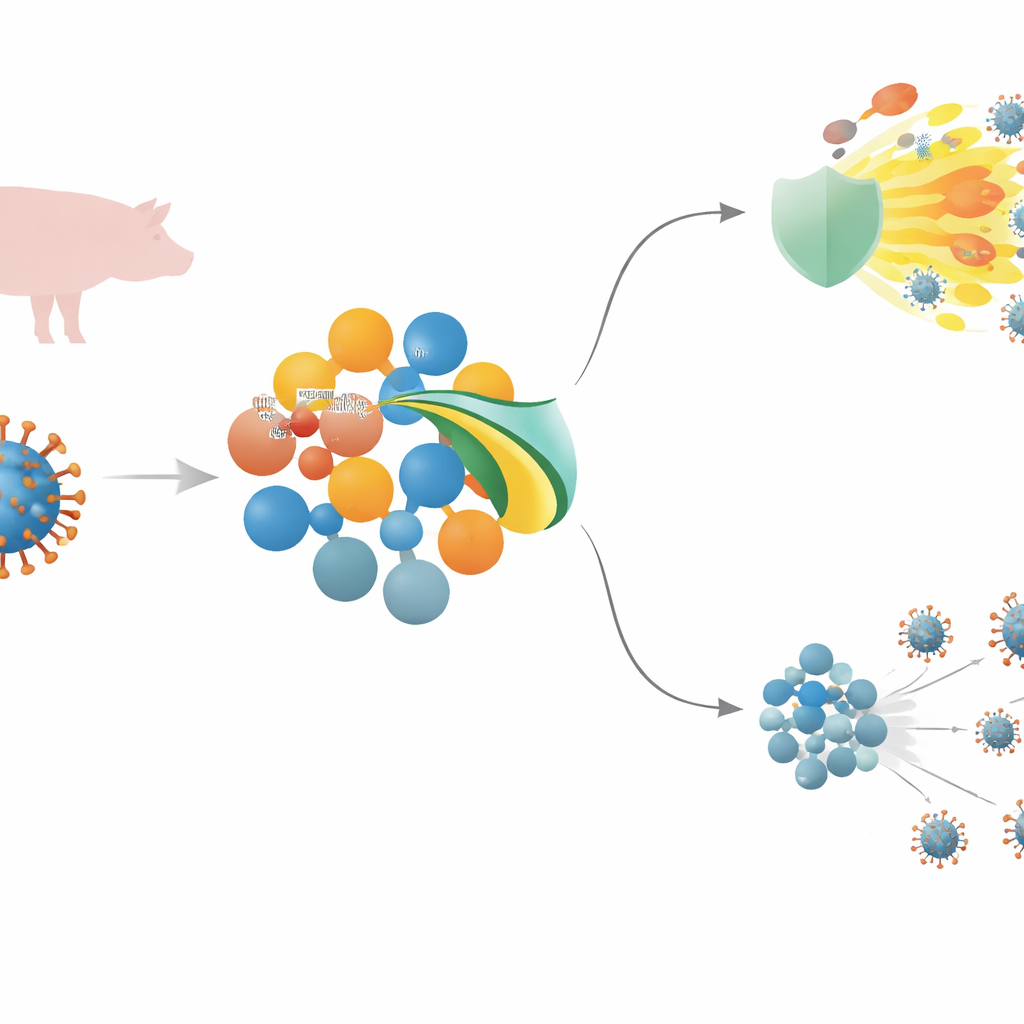
一种致死的猪病毒与机体的第一道防线
非洲猪瘟病毒(ASFV)是一种大型 DNA 病毒,几乎能致死所有被感染的猪。为了立足,病毒必须智胜先天免疫——这是快速的前线防御,用以检测入侵者并触发炎症和抗病毒分子。这一反应的核心是一条信号链,包含细胞表面的感受器、一个称为 MyD88 的中继蛋白,以及被称为 NF–κB 的主控开关,它们共同驱动炎性介质和抗病毒干扰素的产生。ASFV 携带许多被认为干扰这些信号的基因,但其中若干,包括 MGF 505–3R,其具体作法尚不清楚。
病毒如何剪断免疫警报的线路
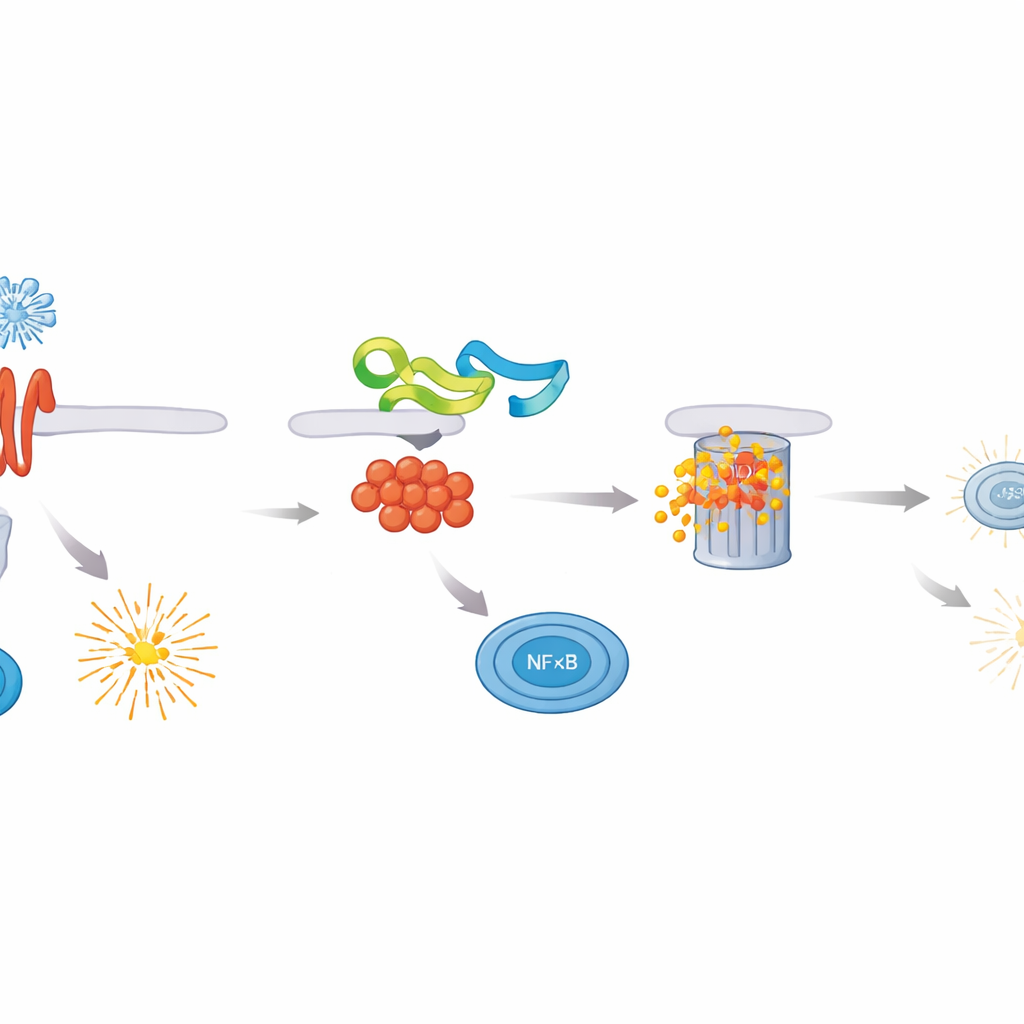
研究者筛选了 ASFV 蛋白对 NF–κB 活性的抑制能力,发现 MGF 505–3R 是一个特别强的抑制因子。当该病毒蛋白存在时,暴露于不同免疫刺激的细胞产生的炎性细胞因子大幅减少,I 型和 III 型干扰素的水平显著降低。进一步观察表明,MGF 505–3R 是直接作用于连接多种免疫感受器与 NF–κB 的中心适配子 MyD88。MGF 505–3R 与 MyD88 结合,并通过细胞的蛋白降解机制将其标记并送去销毁,这一标记形式为 K48 连结的泛素化。随着 MyD88 被降解,NF–κB 无法进入细胞核并启动保护基因,使细胞更易于被病毒复制占据。
聚焦一个微小但强效的蛋白片段
为明确 MGF 505–3R 的关键部分,团队制作了该蛋白的截短版本并测试其效应。他们发现氨基酸 89–277 段既是必要的又足以结合 MyD88、促进其泛素化并阻断 NF–κB 激活。基于蛋白质结构的计算预测,他们从该区域切割出两段短肽。其中一段,pep3R–1,尤为显著:它显著降低 NF–κB 活性,阻断 NF–κB 亚基 p65 的磷酸化与核转位,并在受到多种危险信号刺激的免疫细胞中降低炎性细胞因子与干扰素的表达。在细胞培养中,完整的 MGF 505–3R 与 pep3R–1 不仅减弱了抗病毒信号,还使测试用病毒复制更为高效,凸显了该通路在控制感染中的强大作用。
将病毒伎俩转化为潜在药物
接着团队探索是否可以将该肽用于抑制有害炎症而非助长病毒。在用化学物质 DSS 诱导的结肠炎小鼠模型中,正常情况下动物会体重下降、出现血性腹泻,并在结肠中出现严重的组织损伤和免疫细胞浸润。接受 pep3R–1 治疗的小鼠情况显著改善:疾病评分更低,结肠更长更健康,显微检查显示组织结构得到保存且炎性细胞显著减少。结肠组织和血液中关键炎性分子如 TNF–α、IL–1β、IL–6 以及与白细胞浸润相关的酶水平均有所下降。在另一组实验中,pep3R–1 也减轻了对系统性细菌毒素的炎性反应,表明它能抑制局部和全身性的炎症风暴。
对猪、人类和未来疗法的意义
这项工作表明,ASFV 蛋白 MGF 505–3R 通过拆解关键免疫中继 MyD88 帮助病毒繁殖,从而关闭了炎症和干扰素防御。与此同时,这段病毒蛋白的小片段 pep3R–1 可被重新利用,在小鼠中安全地缓解过度炎症,包括肠道疾病模型。尽管仍需大量工作——例如改善稳定性、递送方式并在更多疾病模型中测试——该研究既揭示了可供抗病毒策略瞄准的关键薄弱环节,也为基于肽的抗炎药物设计提供了受病毒免疫逃逸启发的有希望的蓝图。
引用: Liu, H., Sun, L., Wang, F. et al. African swine fever virus–encoded protein MGF 505–3R impairs innate immunity via ubiquitin–mediated degradation of MyD88. Commun Biol 9, 407 (2026). https://doi.org/10.1038/s42003-026-09681-0
关键词: 非洲猪瘟, 先天免疫, NF-kappaB, MyD88, 抗炎肽