Clear Sky Science · zh
异常的铁稳态导致Gprasp2缺失小鼠耳蜗毛细胞受损和听力丧失
这对日常听力为何重要
听力丧失常被认为是简单的“磨损”,但对许多人来说,它源于隐藏的基因缺陷。这项研究揭示了一个鲜少研究的基因GPRASP2如何帮助保护内耳那些脆弱的声感受细胞免受铁驱动的损伤。通过精确展示在该基因缺失时发生的病理过程,这项工作为遗传性听力问题的更精确诊断以及未来潜在疗法打开了大门,并可能对相关的情绪障碍有所启示。
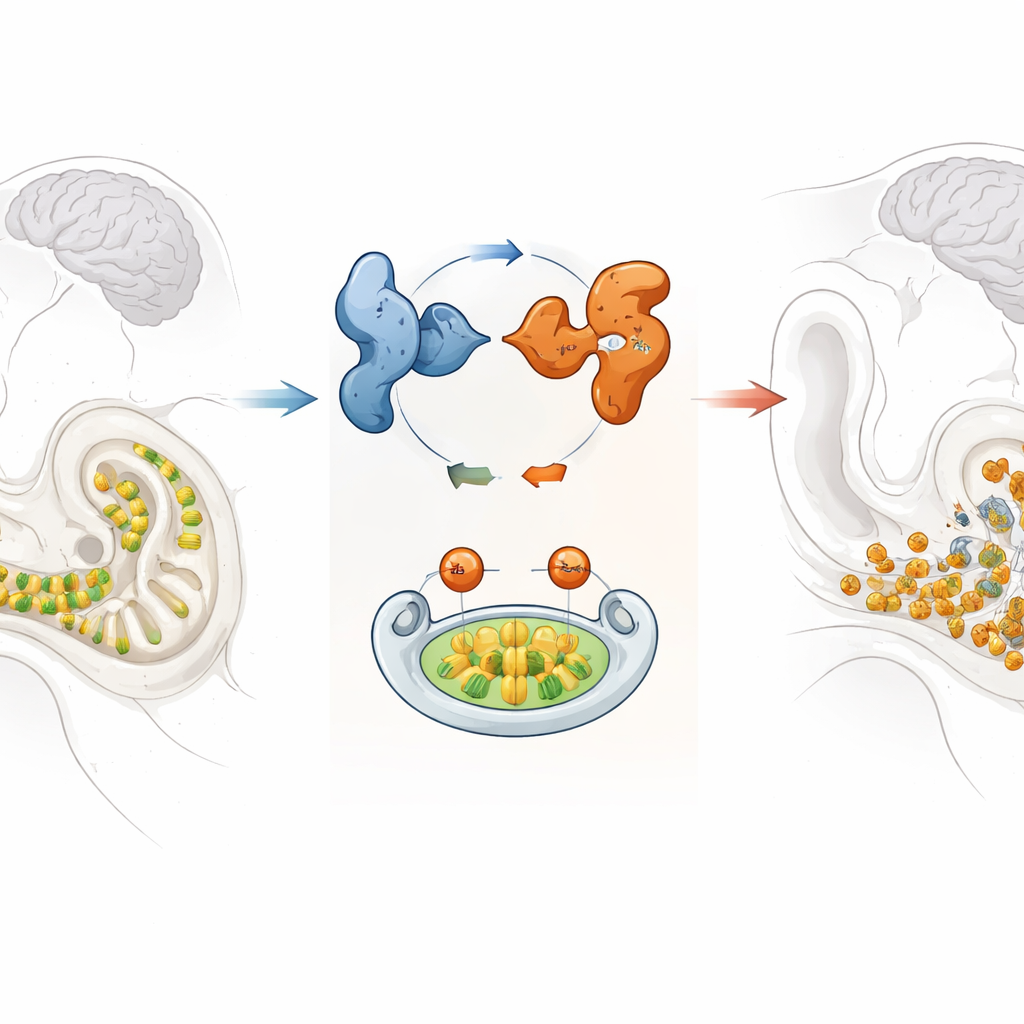
内耳中脆弱的声感受器
在内耳蜷曲的耳蜗内排列着成行的毛细胞,它们将微小的振动转化为大脑可以理解的电信号。一旦这些毛细胞丧失,它们不会再生,因此维持其健康对于终生听力至关重要。研究者将焦点放在GPRASP2——一个在一例伴X连锁综合征性耳聋家系中发现突变的基因。虽然已知GPRASP2在大脑和内耳有表达,但其在听力中的具体功能仍不清楚。
基因缺失时发生了什么
为模拟人类病情,研究团队使用CRISPR基因编辑制造出缺失功能性Gprasp2基因的小鼠。这些动物在用敏感的听神经电记录测试时,显示出不同声频范围内的明显听力下降。它们对突发响声的反应被削弱,但平衡和运动能力大致正常,表明问题特异于听觉而非广泛的运动障碍。有趣的是,这些小鼠在几项标准行为测试中也表现出类似抑郁的行为,提示该基因通过在耳朵和大脑中的作用将听力与情绪联系起来。
耳蜗内部的损伤
当科学家检查Gprasp2缺失小鼠的内耳时,发现许多外毛细胞丢失或错位,存留的细胞常有畸变的纤毛束——这些纤毛通常像音叉一样工作。他们还观察到维持听觉所需特殊液体和电环境的高活性组织——纹状层发生改变。在显微水平上,外毛细胞及其邻近的神经细胞中,细胞死亡和氧化应激的标志物升高,表明这些结构受到活性分子的严重攻击,更容易发生细胞死亡。
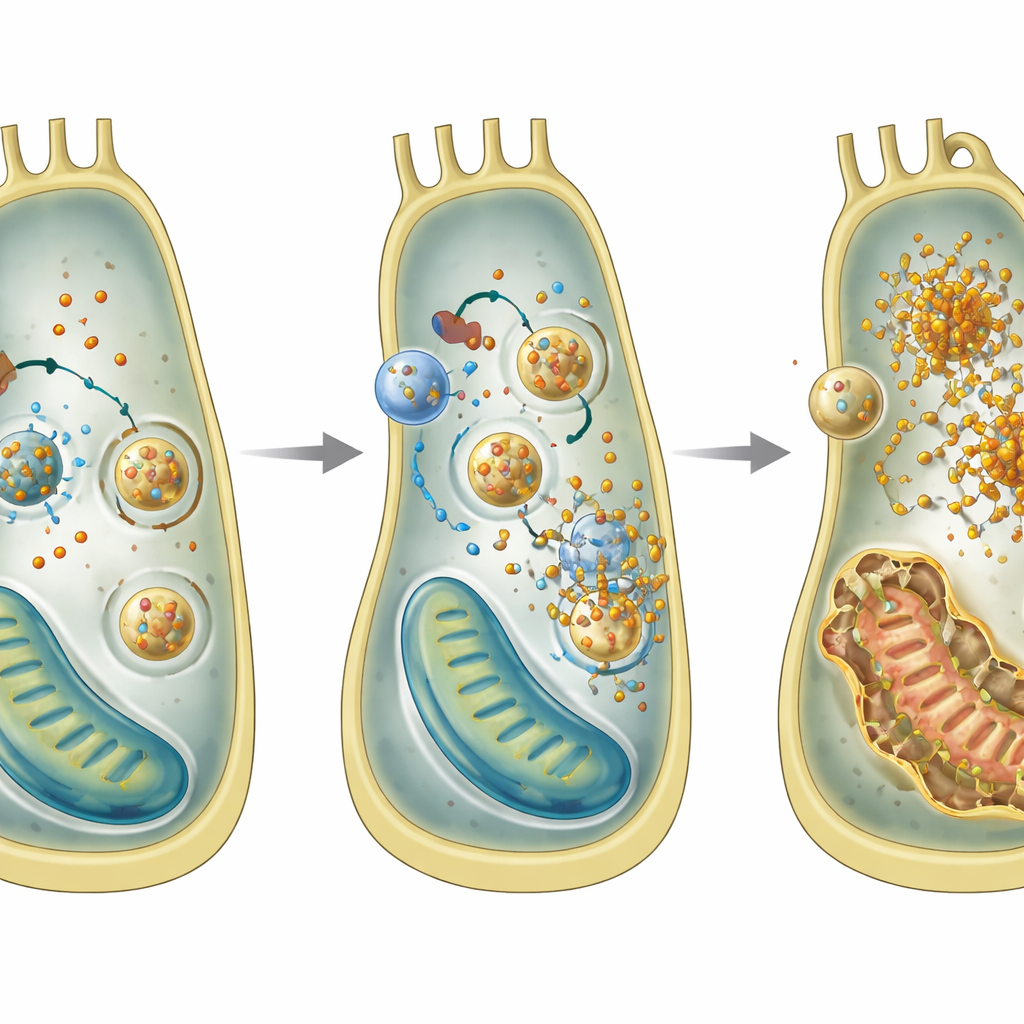
铁过载与失控的回收
进一步研究中,团队使用内耳细胞系来探索单个细胞在缺乏GPRASP2时的变化。他们发现了一种典型的铁驱动细胞死亡形式——铁死亡的特征模式。缺失Gprasp2的细胞积累了更多的亚铁离子,产生更多活性氧,抗氧化剂谷胱甘肽水平降低,并显示线粒体受损。基因和蛋白分析指向铁蛋白自噬(ferritinophagy)增加,即将铁储存颗粒送往回收隔室并被分解,释放出额外的铁进入细胞。阻断这一回收步骤可降低铁的积累,支持过度铁蛋白自噬是导致损伤的核心观点。
保持铁平衡的关键伴侣蛋白
研究者接着探问GPRASP2如何控制这一铁处理机制。通过绘制与GPRASP2相互作用的蛋白质,他们鉴定出NCAM1——一种以在学习、记忆和情绪中的作用著称的细胞粘附分子。他们证明GPRASP2与NCAM1存在物理结合,并且GPRASP2缺失会导致毛细胞及培养的听觉细胞中NCAM1水平下降。NCAM1降低与铁蛋白自噬增加和铁过载相关。在Gprasp2缺失细胞中恢复NCAM1能降低铁水平并抑制关键的铁蛋白自噬调节因子,尽管总体自噬仍然活跃。这提示GPRASP2通过NCAM1微调一条特定的铁回收通路,而不是全面开启或关闭整套回收系统。
对听力及更广范围的意义
简而言之,这项工作表明GPRASP2像耳蜗毛细胞内铁的安全管理员。当GPRASP2存在时,它与NCAM1协作,防止过多储存的铁被重新释放回细胞,从而控制氧化损伤。基因被破坏时,铁处理失衡,细胞从内部“生锈”,关键毛细胞死亡,导致听力丧失。由于GPRASP2和NCAM1也在大脑中发挥功能,相同的通路可能有助于解释某些患者出现的情绪改变。理解这种基于铁的失效模式为未来针对GPRASP2相关或类似遗传疾病的药物或基因疗法提供了明确的靶点,以期保护人类的听力。
引用: Lu, Y., Sheng, F., Yao, J. et al. Abnormal iron homeostasis mediates cochlear hair cell impairment and hearing loss in Gprasp2-deficient mice. Commun Biol 9, 425 (2026). https://doi.org/10.1038/s42003-026-09679-8
关键词: 遗传性耳聋, 耳蜗毛细胞, 铁稳态, 铁死亡, GPRASP2