Clear Sky Science · zh
ZIKV包膜蛋白是神经谱系早期定向分化的强烈阻断因子
为何这对发育中的大脑重要
寨卡病毒最初成为头条,是因为它会导致婴儿出生时头颅异常偏小并伴有严重脑损伤。但母体内的感染如何如此强烈地干扰胚胎大脑构建的最早步骤?本研究聚焦于单一病毒成分——包覆寨卡病毒颗粒的包膜蛋白——并探讨仅凭该蛋白是否能误导神经细胞的形成。通过用小鼠干细胞在体外重建早期大脑发育,研究者揭示了该病毒蛋白如何在不显山不露水的情况下强烈阻断神经回路的正常构建。
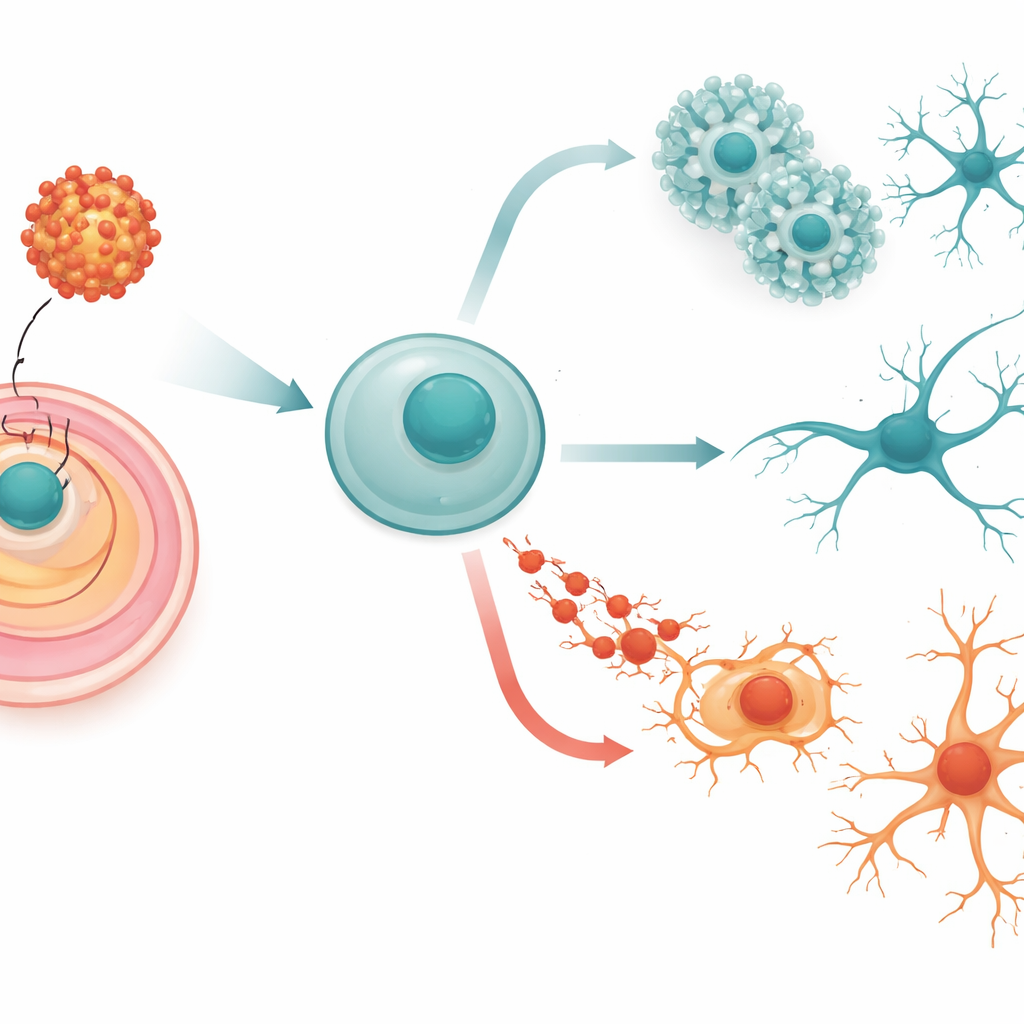
从可塑的起始细胞到未来的神经元
我们的大脑起始于一种简单且高度可塑的细胞,称为胚胎干细胞。这些细胞可以分化为机体的任何组织,但在适当的条件下,它们沿着一条精心编排的路线走向神经细胞:先决定“神经”方向,然后形成类似早期神经系统的花簇(rosette)结构,最终成熟为通过细长分支相互连接的神经元。研究团队使用小鼠胚胎干细胞作为这些早期阶段的替代模型,并通过改造让它们产生寨卡包膜蛋白,且分别包含或不包含一个已知会影响病毒活性的关键糖基化位点的小变动。
病毒外衣蛋白冻结了大脑构建的第一步
当干细胞产生寨卡包膜蛋白时,它们外观仍然健康,并保留向多种组织分化的广泛潜能。然而,当允许其自由分化时,它们形成代表胚胎三种基本组织层的复杂三维团块的能力显著下降,三胚层的标志物水平均降低。此结果表明,病毒蛋白并非直接杀死干细胞,而是微妙地干扰了它们走上正常发育路径的能力。缺失特定糖基化位点的突变体在这种模式上表现得更不均一,提示蛋白的细微化学修饰会调节其损害发育的方式。
阻断从干细胞到神经元的道路
研究者随后特别关注从干细胞到早期神经元的转变,采用了两种公认的体外模型:平面“单层”培养和模拟早期脑组织的三维“神经球”培养。在两种系统中,对照细胞在数日内平稳上调神经干细胞与神经元标志物的表达,形成有序的花簇并产生大量幼年神经元。与之相反,产生包膜蛋白的细胞生成的神经干细胞显著减少,花簇数量减少,早期神经元数量大幅下降,关键与神经身份相关的基因和蛋白水平降低。去除糖基化的突变体在基因层面通常引起更强的阻断,并触发额外的炎性细胞死亡通路,提示导致更严重损伤的可能机制。
在幼年神经网络中使通讯沉默
为了解细胞内发生了何种变化,研究团队比较了关键分化阶段正常细胞与产生包膜蛋白细胞的全局基因活性。他们发现许多与神经生长、突触形成和树突小棘(记忆存储位点)相关的基因被下调。参与神经递质装载与释放、轴突定向连接目标以及突触组装的通路均受到抑制。与此同时,与钙信号和某些细胞表面受体相关的信号通路被激活,可能使细胞过度兴奋或错误地接收信号。这些广泛变化在平面和三维培养中均有出现,表明包膜蛋白反复将发育中的神经细胞引向远离构建稳健、互联网络的方向。
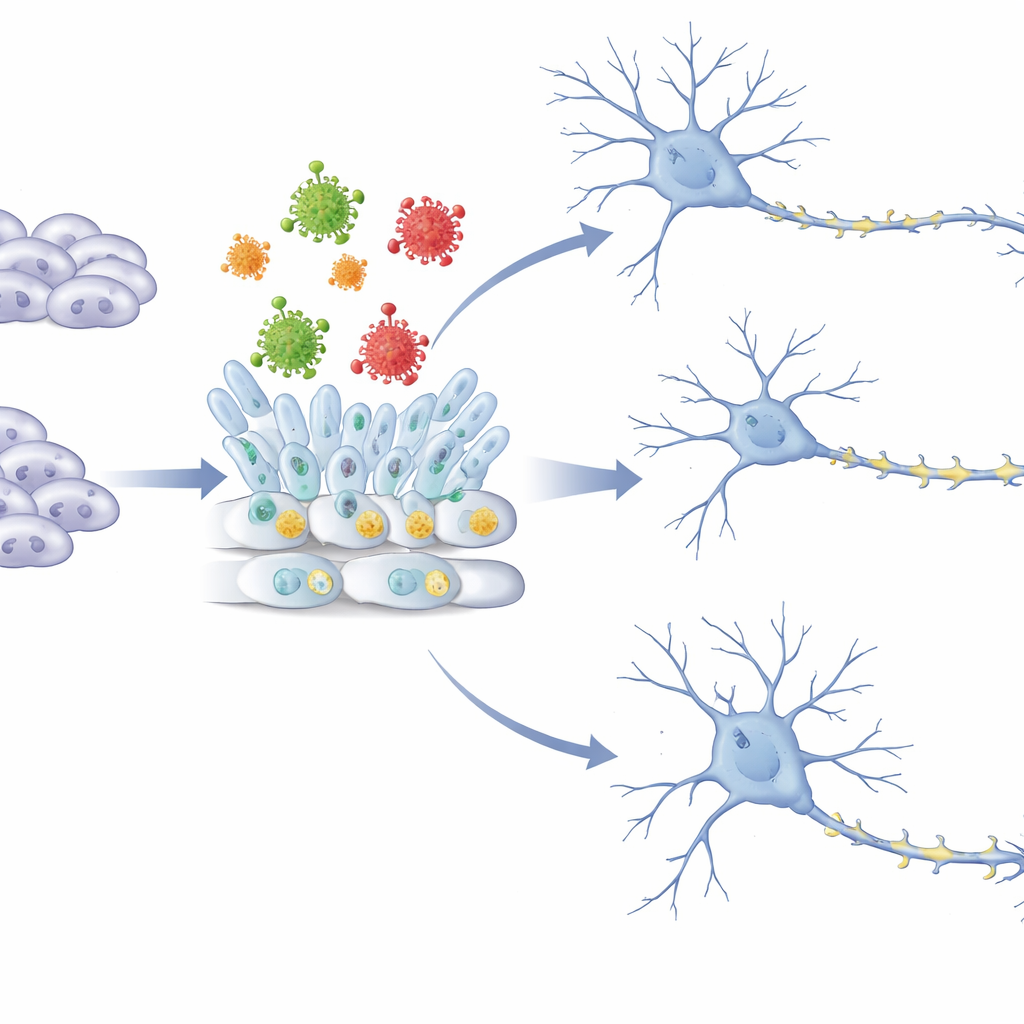
这对寨卡相关出生缺陷意味着什么
对非专业读者而言,关键信息是:寨卡病毒不必通过活跃复制并杀死细胞才能损害发育中的大脑。本研究表明,其外层包膜蛋白本身就能把早期干细胞推离通向神经元的正常路径,并削弱形成健康突触和树突棘所需的基因程序。此类早期、隐蔽的干扰有助于解释在子宫内暴露为何会导致小头畸形和长期认知问题。研究结果也提示,涉及病毒包膜蛋白的疫苗或治疗策略需要仔细评估对大脑发育的潜在影响,即便不存在活病毒。
引用: Ma, ZH., Wang, Y., Hassaan, N.A. et al. ZIKV envelope protein is a strong blocker of early directional differentiation in the neural lineage. Commun Biol 9, 395 (2026). https://doi.org/10.1038/s42003-026-09672-1
关键词: 寨卡病毒, 大脑发育, 神经干细胞, 病毒包膜蛋白, 小头畸形