Clear Sky Science · zh
神经元对反复机械压缩的分子韧性
我们的神经如何抵御日常磨损
每当你弯腰、转头或迈步时,遍布体内的神经都会被轻轻挤压和拉伸。终生累积下来,相同细胞会承受数百万次微小的机械冲击。这项研究提出了一个看似简单但意义重大的问题:神经细胞在反复挤压下能承受多少损伤才会崩溃?在压力不至于极端时,它们是否具有内在的自我修复机制?
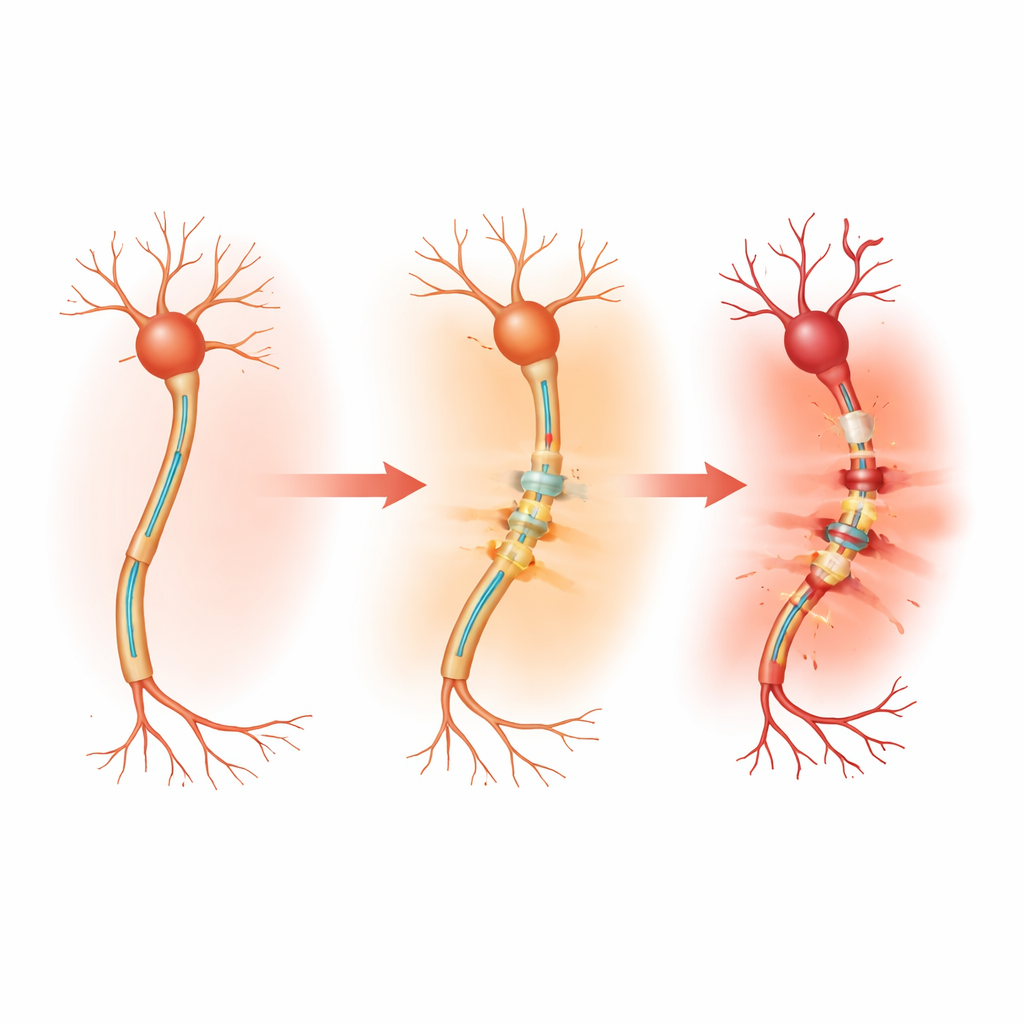
对反复挤压下神经的测试
研究人员使用来自脊柱附近的背根神经节的感觉神经细胞——这些细胞负责传递触觉、疼痛和体位信息。他们将这些神经元培养在一个置于可拉伸橡胶片上的微型实验室腔室中。通过螺杆驱动装置精确移动该橡胶片,研究团队能够对轴突(负责传递神经信号的长而类似电缆的延伸部分)施加受控的循环压缩,同时避免压碎细胞体。本研究测试了三种水平的反复压缩,每种都以20个循环施加:低水平(缩短2.5%)、中等水平(5%)和高水平(10%)。
何时压力变得具破坏性
在最高水平的反复压缩下,神经元状况很差。电子显微镜图像显示严重的内部损伤:细胞核内的DNA凝聚、胞内结构的膜破裂,以及轴突内通常有序的支架解体为无特征的暗区。许多轴突出现退化,细胞死亡率急剧上升。在这些条件下,损伤发生迅速且范围广泛,细胞似乎无法发起有效的修复反应。换句话说,存在一范围的反复机械应力会直接压垮神经细胞,使其走向永久性损伤和死亡。
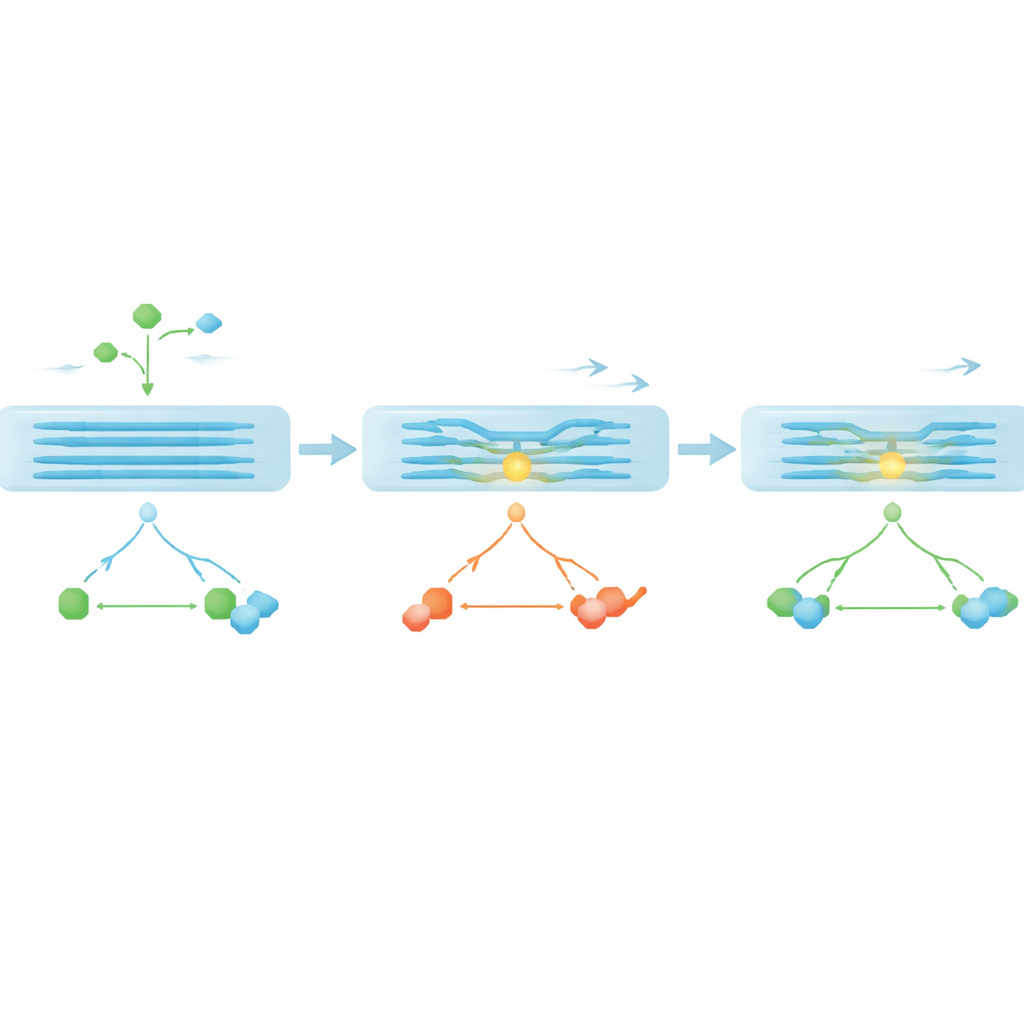
使神经更强韧的轻微挤压
低强度的反复压缩则呈现出不同情况。在此条件下,神经元仍然存活,内部精细结构看起来正常。轴突确实在一段时间内变短,表现为一种短暂的缩回,但没有撕裂或关键内部成分丧失的迹象。相反,研究者在轴突内部发现了强化的化学特征。微管——作为轴突内部主要结构“轨道”的刚性管状丝——显示出与稳定性相关的修饰增加,而与快速周转相关的修饰减少。在压缩循环结束24小时后,轴突长度和微管的化学特征已恢复到基线水平。这表明,温和的机械应激可触发一种保护性反应,稳定神经的内部骨架并帮助其恢复。
中间情况:先受损,后恢复
中等压缩水平(5%)位于这两种极端之间,揭示了神经元如何应对更严重但仍可存活的应力。压缩后不久,轴突变短,内部的微管束看起来被扰乱:丝状结构减少、间距变大,且常常扭曲或错位。化学标记表明微管稳定性下降。然而大多数细胞并未死亡,并且在一天内,微管的结构与化学特性在很大程度上恢复。为探究这种反弹机制,团队分析了压缩后哪些基因的活性发生变化。他们发现以 Ras 蛋白为中心的著名信号通路——一类控制细胞生长、生存和内部支架的分子开关——被激活的强烈迹象。起初,活性 Ras 水平下降,与微管稳定性降低相一致;随后使 Ras 重新激活的分子增加,Ras 活性恢复正常,轴突的内部结构也随之被修复。
这些发现对日常生活的重要性
总体来看,研究表明神经元对反复机械挤压呈剂量依赖性反应。强烈且反复的压缩会导致灾难性崩溃与死亡;温和的压缩则触发一种“训练效应”,促使细胞强化并保护其内部“轨道”;中等压缩则先破坏轴突支架,但神经元可调用如 Ras 信号等分子通路重组其内部结构并恢复长度。通俗地说,我们的神经并非易碎的玻璃纤维;它们是有生命的、可适应的组织,具有内置的安全余量和修复机制,帮助它们在日常生活持续的机械冲击下生存——但有其承受极限。
引用: Coppini, A., Cappello, V., Nasrin, S.R. et al. Molecular resilience of neurons to repetitive mechanical compression. Commun Biol 9, 392 (2026). https://doi.org/10.1038/s42003-026-09661-4
关键词: 神经机械生物学, 轴突压缩, 微管动力学, Ras 信号传导, 神经耐受性