Clear Sky Science · zh
由先天性N端肽激活的巨细胞病毒编码G蛋白偶联受体UL33
一种常见病毒如何重塑我们的细胞
人巨细胞病毒(HCMV)悄然感染地球上大多数人群,通常不引人注意。然而在新生儿、移植患者和其他免疫受损者中,它可导致严重疾病。本研究以分子细节揭示了一种被称为UL33的病毒蛋白如何像内置开关一样持续推动被感染细胞有利于病毒生存。理解这一隐蔽开关有助于解释HCMV如何终生潜伏,并指向无需损害正常细胞信号传导即可解除病毒活性的潜在新策略。
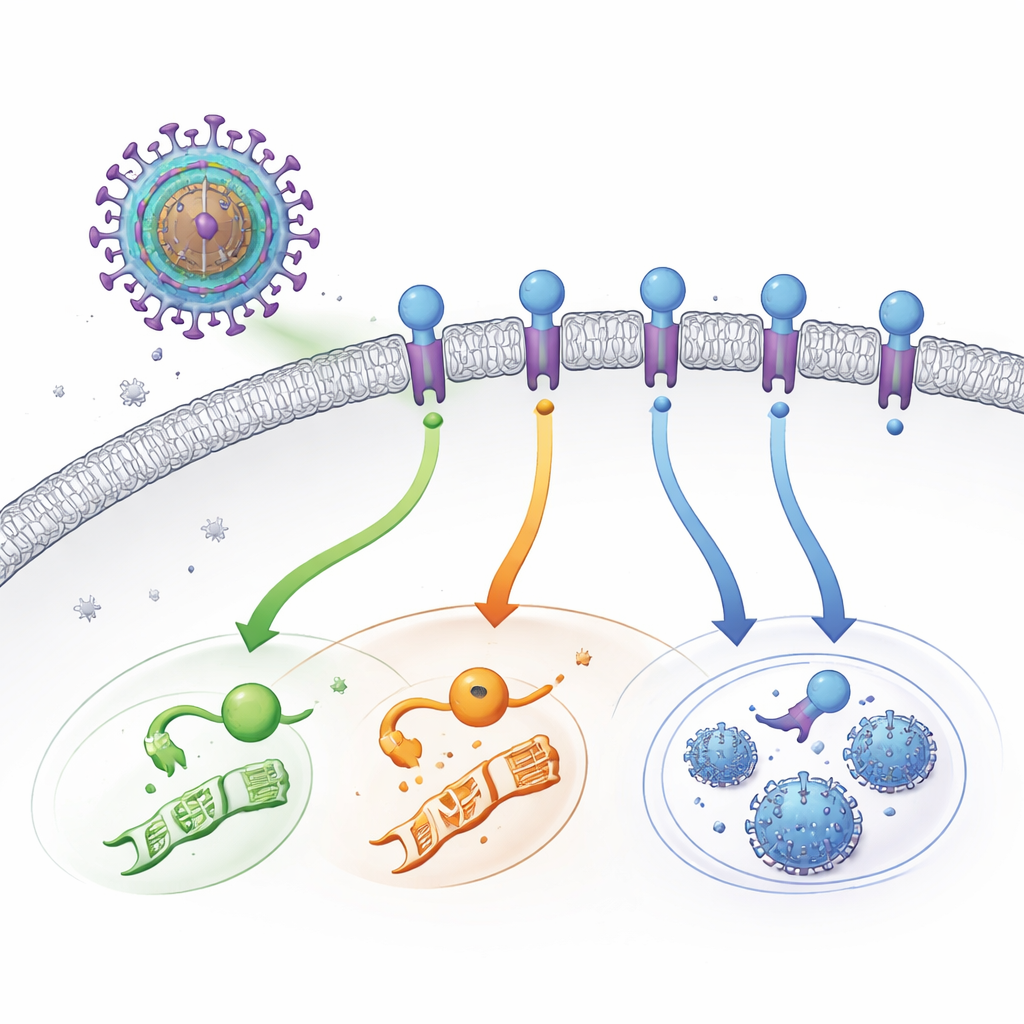
细胞表面上隐秘的病毒开关
HCMV携带自身版本的细胞表面受体——这些蛋白通常用于感知激素或免疫信号。UL33就是此类病毒受体之一。与通常需等待外部信号的受体不同,UL33是“常开”的。一旦被部署到被感染细胞的外膜,它便能同时接入细胞的数条主要通讯通路。这些通路控制基因活性、代谢以及细胞是进入休眠还是产生更多病毒等进程。多年来,科学家们知道UL33具有活性,但不清楚是什么将其开启,尤其因为从未发现任何外源激活分子(配体)。
自启式:为自己带来钥匙的受体
研究者利用先进的冷冻电子显微镜获得了UL33与细胞信号伙伴之一——G蛋白Gs结合的三维快照。图像显示UL33蛋白的起始部分——其短小的N端尾巴——折回到受体自身的一个口袋中,就像一把永远留在锁内的钥匙。这个“系在一起”的尾巴嵌入一个小的侧向口袋,在相关的人类受体中,该口袋通常会接纳免疫信号蛋白(趋化因子)的部分结构。UL33从一开始就占据了这个口袋,阻止外来趋化因子结合,这就解释了为何它表现为一个“孤儿”受体,不对正常宿主信使作出反应。
病毒开关上的关键原子
为证实这一内置尾巴确实是触发元件,团队在人体细胞中系统性地改变了UL33的单个构件。他们专注于尾巴的前几个氨基酸以及口袋内与之配合的位点。当他们将这些关键残基替换为更中性的残基或完全移除其中之一时,UL33的信号传导能力降至接近零——尽管这些改变的受体仍能以正常数量到达细胞表面。换句话说,蛋白质在细胞上存在但无法发声。这表明尾巴不仅是结构性的装饰;它是维持UL33持续开启的必要自激活构件。
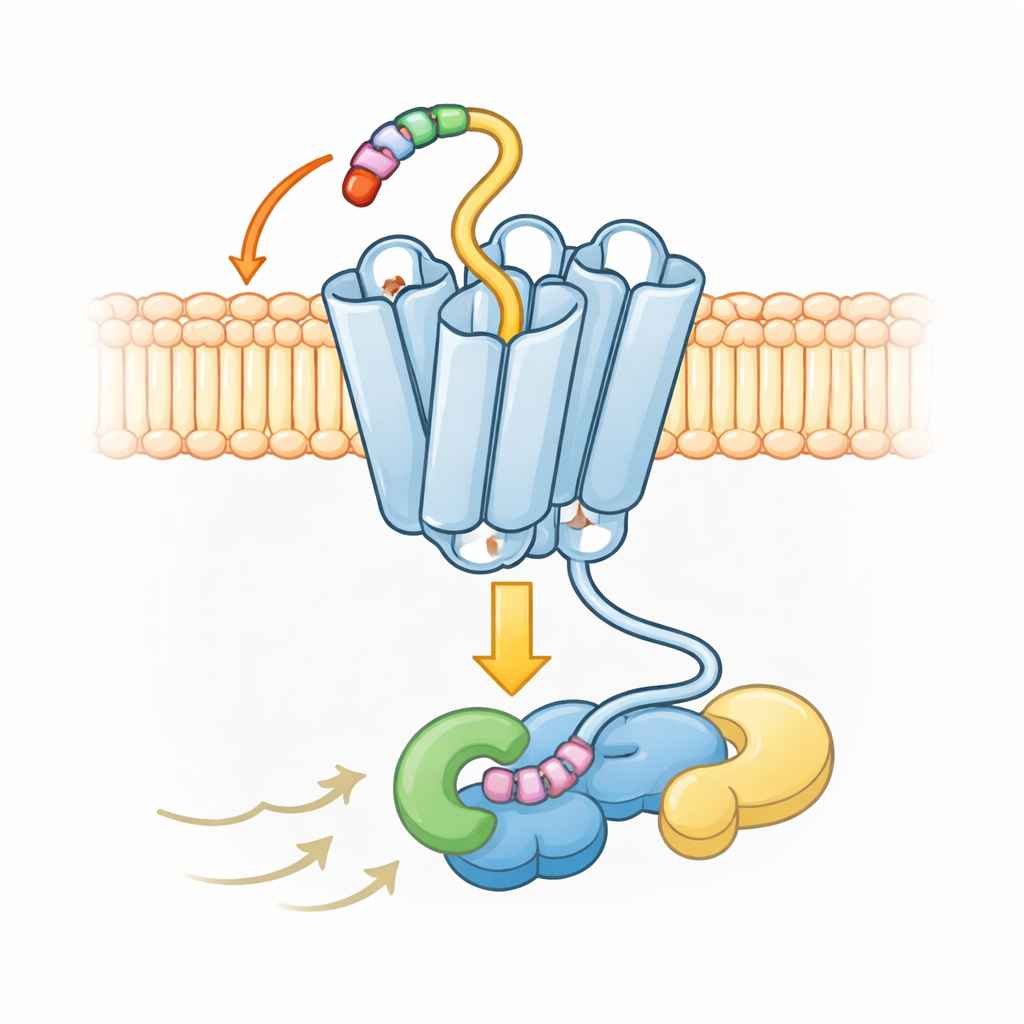
用于广泛但可控信号传导的不同构形
结构图谱还显示,UL33在活化后的构象与典型人类受体略有不同。在该家族的大多数受体中,靠近细胞内侧的七根螺旋之一在受体被激活时会剧烈向外摆动,打开一个让G蛋白对接的大腔体。而在UL33中,该螺旋保持更靠近中心,形成更紧密的配合。尽管如此,UL33仍能通过与插入受体的G蛋白端部形成精确接触来结合多种G蛋白——包括Gs、Gq和Gi。这些接触偏好某些G蛋白并排除其他类型(例如G12/13组),使病毒能够在不释放失控信号的情况下偏置细胞反应。
老病毒的新弱点
通过将结构成像与功能测试相结合,这项研究勾勒出清晰图景:UL33是一个自启动的病毒受体,其自身尾巴充当永久附着的激活子。这一设计让HCMV以温和但持续的方式调整宿主细胞信号以支持病毒复制和重激活,尤其是通过增强启动病毒基因的通路。同时,这项工作暴露了可被药物利用的薄弱环节,例如通向尾巴结合口袋的狭窄通道。设计嵌入该区域或使尾巴脱位的分子可能抑制UL33的活性并减少病毒造成的损害,同时保护机体的正常受体。对于面临HCMV风险的患者,靶向这一病毒“总开关”或有朝一日提供更精确的病毒控制手段。
引用: Drzazga, A.K., Suzuki, S., Wouters, C. et al. Activation of cytomegalovirus-encoded G protein-coupled receptor UL33 by an innate N-terminal peptide. Commun Biol 9, 415 (2026). https://doi.org/10.1038/s42003-026-09660-5
关键词: 巨细胞病毒, 病毒性GPCR, 细胞信号传导, 冷冻电镜结构, 药物靶向