Clear Sky Science · zh
临床前核酸疗法研究中的模型选择
将基因变成药物
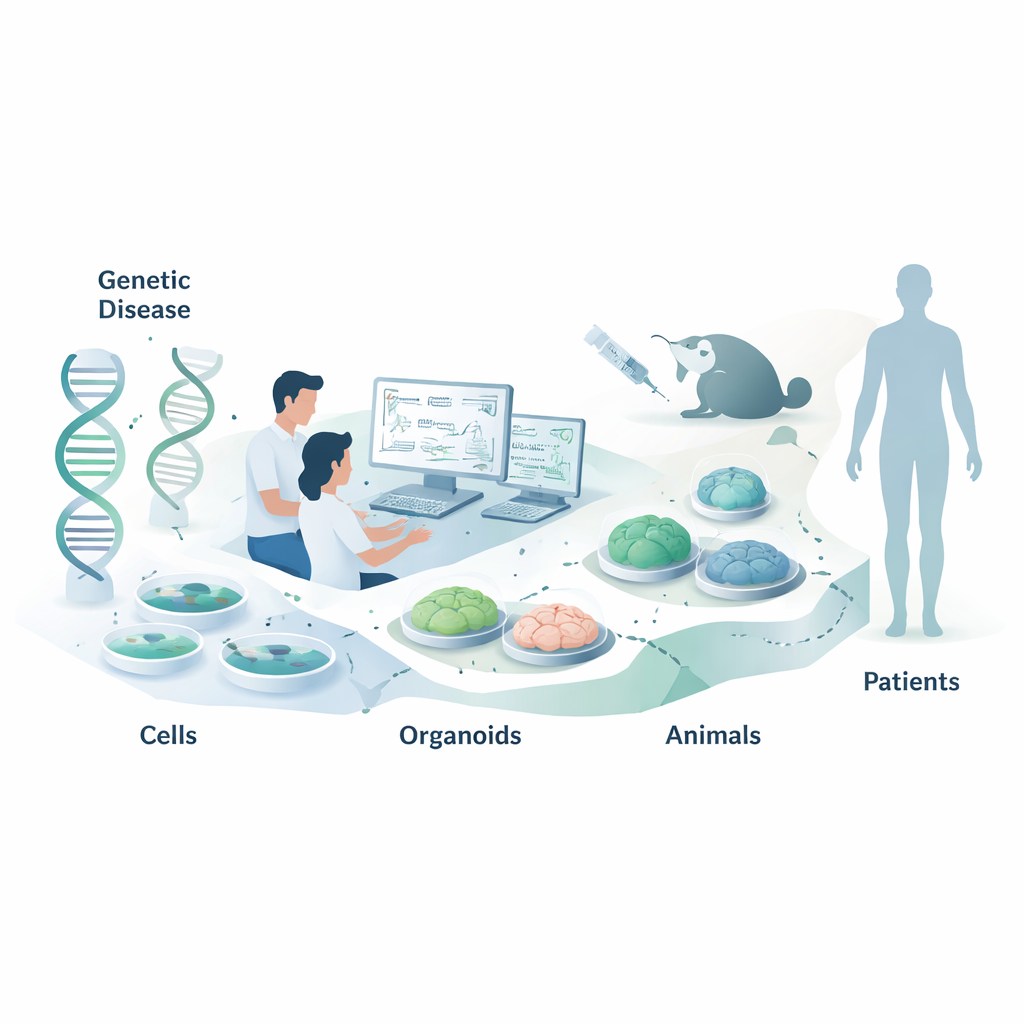
核酸疗法是一类新型药物,它们不通过阻断蛋白质(大多数传统药物的做法)来起效,而是更早一步作用于我们的遗传信息层面。本文综述解释了科学家如何选择合适的体外和动物模型,在这些模型中测试针对RNA的药物以在进入患者前评估效果。对普通读者而言,合理的模型选择意味着更快、更安全且更有效的基因病治疗,包括罕见的儿童疾病以及像心脏病这样的常见病。
这些基因药物有何不同?
核酸治疗(NATs)包括称为反义寡核苷酸(ASOs)和小干扰RNA(siRNA)的短链分子。与依赖蛋白靶点的形状和化学性质不同,这些药物通过碱基配对规则识别其靶标——与DNA相同的A‑T和G‑C配对方式。这使它们具有可编程性:一旦知道要改变的RNA序列,通常可以在不依赖多年传统化学研究的情况下快速设计多种候选药物。难点不再是“我们能否合成活性化合物?”,而是“如何在真实的生物环境中衡量其是否真正有效?”因为序列中哪怕一个碱基的差异都可能影响活性,选择合适的测试系统就至关重要。
简单的细胞检测:快速但不完整
大多数核酸疗法的第一站是一些相对容易培养的细胞系,如HeLa或HEK293,这些细胞已表达目标RNA。研究者加入大规模的ASO或siRNA候选库,然后用PCR、免疫印迹等技术测量目标RNA及其蛋白的下降程度。他们也可能使用来自患者的细胞,这能更好地反映个体的遗传背景,并允许测试仅沉默有害等位基因的“等位基因选择性”药物。当天然基因难以表达时,科学家有时会引入人工的小基因或报告质粒——当RNA被切割或正确剪接时会发光。这些体系在快速比较大量设计上很有用,但可能遗漏诸如天然RNA结构或细胞类型特异性加工等重要细节,因此结果必须在更具真实感的环境中得到确认。
从分子修复到真实细胞行为
许多核酸疗法的目标不仅是销毁有害RNA,还通过改变剪接来修复它。精心设计的ASO可以促使细胞跳过有害外显子、恢复缺失片段,或阻止插入破坏编码的“伪外显子”。为了判断这些改变是否真正改善了细胞功能,研究者会超越单纯的RNA和蛋白读出。在来源于患者的细胞中,他们会测试酶活性是否恢复、肺细胞的离子转运是否正常化、或免疫细胞的信号通路是否正确响应。越来越多的研究使用三维类器官——由患者干细胞培养的迷你组织——可以模拟心跳、脑网络活动或其他复杂行为。这些3D模型更接近真实器官,但更难、耗时且昂贵,因此团队需要在现实性与通量之间权衡。
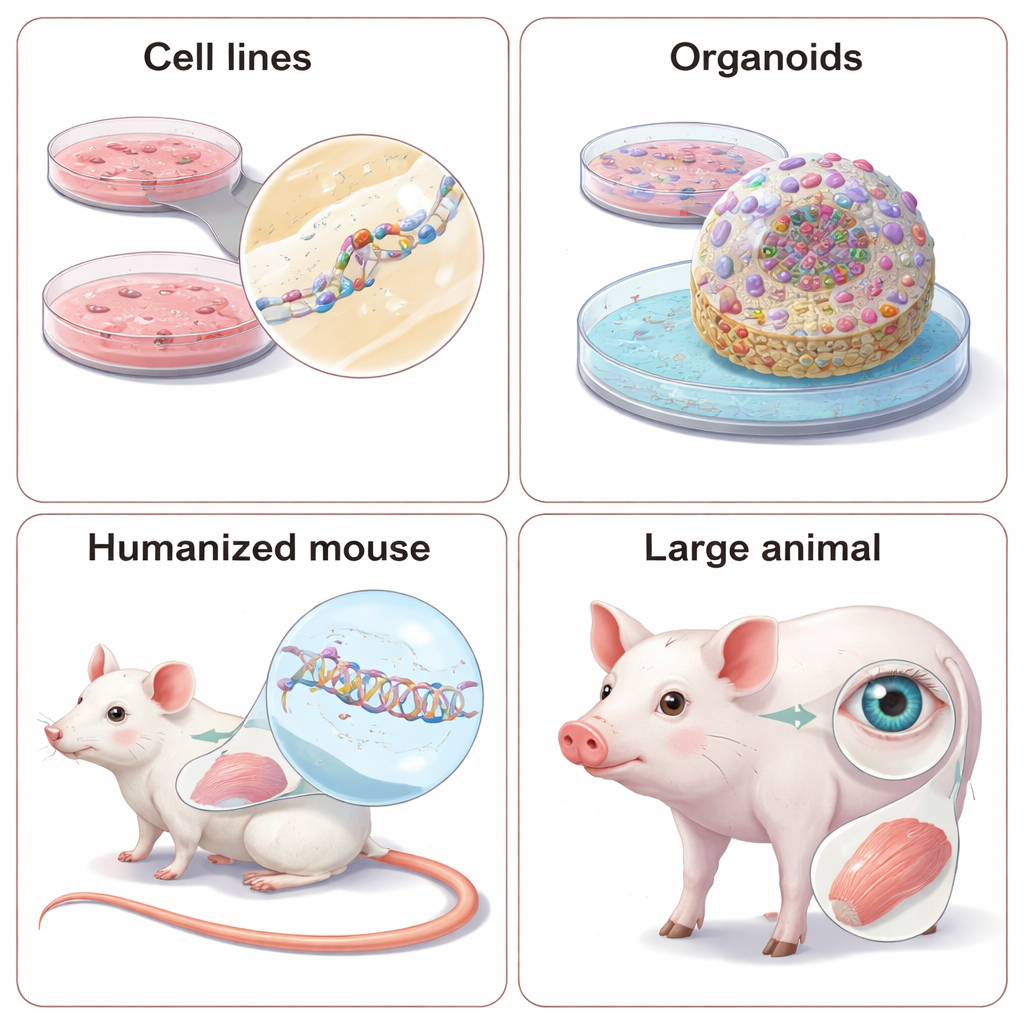
为什么动物仍然重要——以及如何使其“人源化”
一些疾病特征,如全身代谢、器官间相互作用或行为,无法在培养皿中完整呈现。因此需要在活体动物中测试核酸疗法。由于这些药物对精确的RNA序列敏感,科学家面临两种选择:设计与动物基因序列匹配的“替代”药物,或重新工程改造动物以携带人类基因序列。替代ASO和siRNA可以揭示降低某一基因是否能改善在既有小鼠病程模型中的症状,但它们不能完全模拟针对人类靶点的临床候选药物。人源化模型——携带人类基因片段或整段拷贝的小鼠,甚至迷你猪——可以用于测试真实的临床候选物,但构建这些模型需要大量时间和成本,而且物种间基因调控的细微差异仍可能带来意外。综述还强调了大型动物日益增长的应用,特别是在眼和肌肉疾病研究中,其解剖结构更接近人类。
展望:更智能的模型与更少的试错
作者总结指出,对于核酸类药物不存在单一的“最佳”模型;每个项目都需要一条定制化路径,从快速、简单的检测开始,逐步过渡到更复杂、更贴近人类的系统。随着监管机构和资助者推动减少动物使用,复杂的类器官、器官芯片装置和计算模型有望承担更多任务,尤其是与机器学习工具结合时,可预测哪些序列和化学修饰最有可能成功。最终,通过理解每种模型的优势与盲点,并在整个领域内共享最佳实践和数据,研究者能更可靠地将可编程的基因学想法转化为对患者安全有效的药物。
引用: Oliver, P.L., Hill, A.C. Model selection in preclinical nucleic acid therapeutics research. Commun Biol 9, 200 (2026). https://doi.org/10.1038/s42003-026-09650-7
关键词: 核酸疗法, 反义寡核苷酸, siRNA, 临床前模型, 基因疗法