Clear Sky Science · zh
二价阳离子的选择性结合重塑核小体力学并解锁组蛋白尾部动力学
微小离子如何帮助管理我们的 DNA
在每个细胞内,数米长的 DNA 必须被折叠、打包,同时在需要时仍能被访问。本文探讨了细胞内两种常见无机离子——镁和钙——如何微妙地改变 DNA 在蛋白质上的缠绕方式,进而影响遗传物质的包装紧密度以及其可读性。通过对这些相互作用进行原子级别的模拟,作者揭示了离子浓度的变化如何使局部 DNA 结构变得更僵硬或更松弛,并改变那些帮助组织染色体的柔性蛋白尾部的行为。
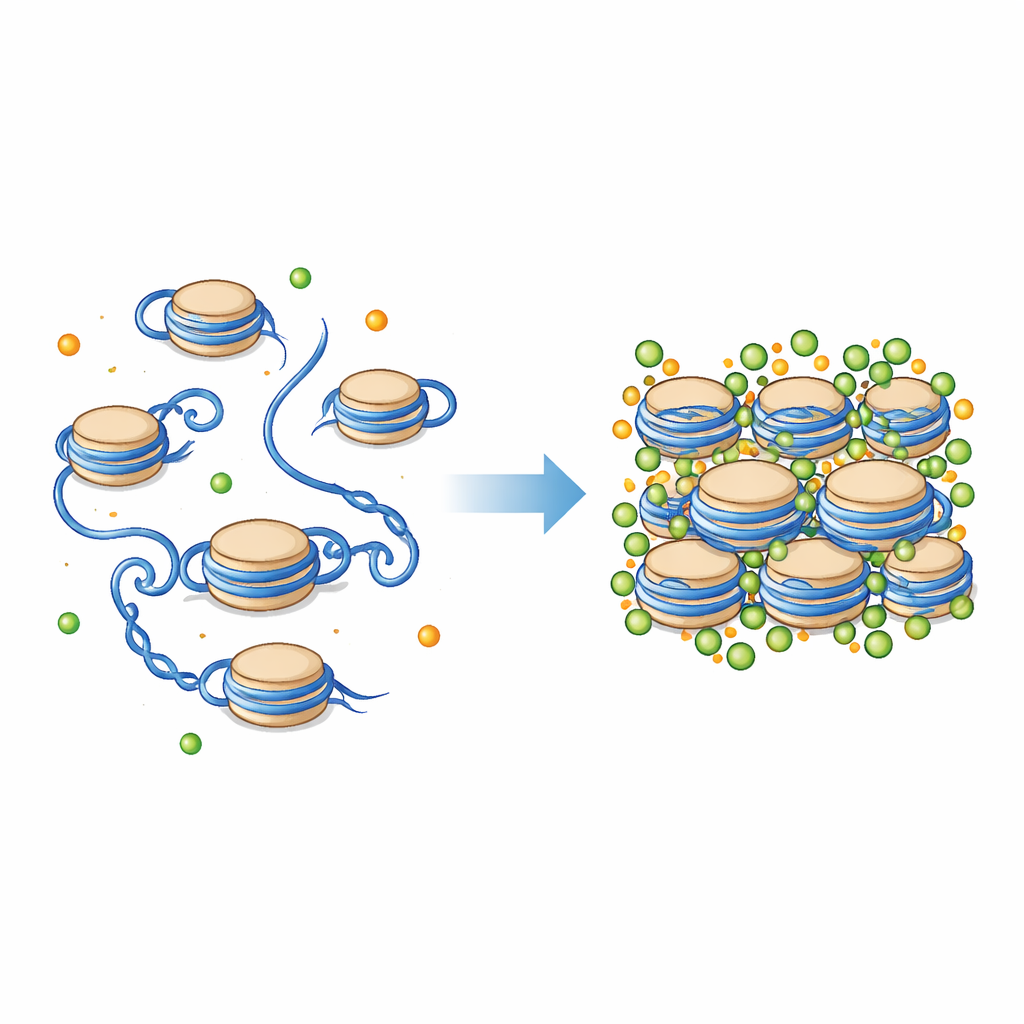
染色体打包核心的“珠子”
细胞中的 DNA 并不是散放的;它绕在被称为核小体的蛋白线轴上。每个核小体是短段 DNA 绕在一簇组蛋白上,组蛋白伸出可弯曲的尾部。这些单元共同形成染色质的基本“串珠”结构,随后可折叠成更紧密的纤维。核小体周围的环境充满带电粒子,包括镁 (Mg²⁺) 和钙 (Ca²⁺)。这些离子已知有助于染色体凝聚,但它们究竟如何影响核小体及其组蛋白尾部的微观力学细节,长期难以直接观测。
在拥挤的原子世界中模拟
为揭示这些细节,作者进行了 81 微秒的大规模计算模拟,在模拟中显式建模了 DNA、蛋白、水和离子的每个原子。他们系统地改变镁和钙的浓度,测试了不同的离子描述方法,并研究了有尾部和无尾部的核小体。通过将模拟得到的离子结合模式与实验测量进行比较,他们确定了一个更精细的模型,该模型最好地匹配了真实核小体吸引这些离子的方式:镁更倾向于停留在 DNA 槽沟中,而钙则更常与 DNA 骨架和某些酸性蛋白位点发生接触。
离子如何挤压 DNA 并使核心变得更刚性
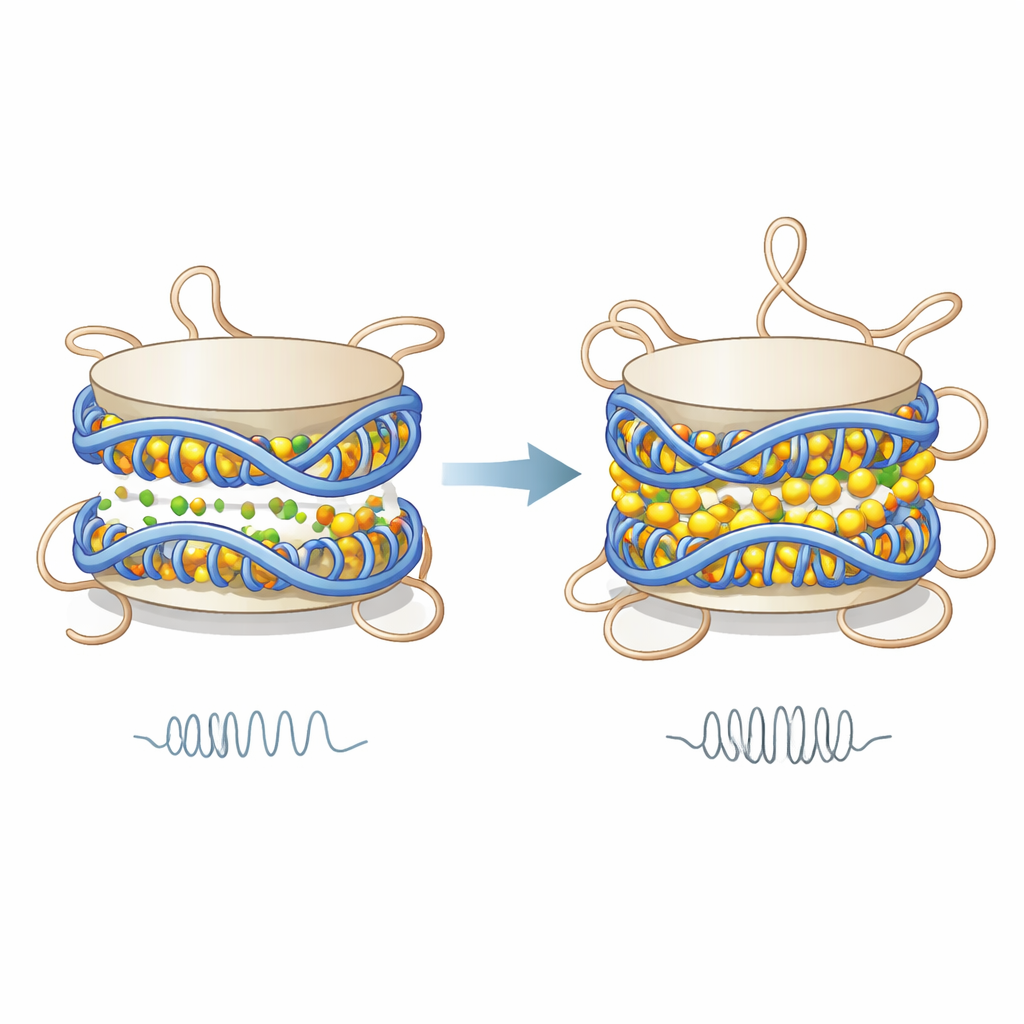
模拟显示,二价离子沿着 DNA 表面以及缠绕每个核小体的两圈 DNA 之间的狭窄空间聚集。通过部分中和 DNA 强烈的负电荷,这些离子减少了相邻 DNA 区段之间的电排斥。结果是两圈 DNA 更靠拢,核小体变得略短,其机械刚性增加——这由将核小体视为微小弹性圆柱的模型所测量。该刚性增加并非来自 DNA 脱落或大规模解缠;而是源于间距的细微变化和特定 DNA 区域更协调的运动,这些区域像更为刚性的整体一起运动。
解放那些柔软的蛋白尾部
当 DNA 核心变得更紧凑和更刚性时,柔性的组蛋白尾部却表现出相反的反应。在低离子条件下,尾部中带正电的氨基酸会紧贴带负电的 DNA,形成许多稳定接触。当镁或钙沿 DNA 结合时,它们屏蔽了这些电荷,削弱了尾部与 DNA 之间的吸引力。作者发现尾部——尤其是来自 H3 组蛋白的尾部——与 DNA 的接触减少,在 DNA 上的停留时间变短,尾部采样的位置范围更广。这意味着尾部与 DNA 的相互作用变得更频繁但更短暂,动力性增强,并可能更自由地接触邻近核小体。
这对基因控制和染色质状态意味着什么
这些发现共同勾勒出镁和钙在染色质中的双重作用。通过加紧 DNA 的缠绕并增加核小体的刚性,它们促进更致密、更不灵活的染色质。同时,通过放松组蛋白尾部与 DNA 的接触并增强尾部运动,它们使关键位点更容易被化学修饰或被调控蛋白识别。由于细胞核中的离子浓度会随信号和能量状态波动,这项工作表明,细胞环境中的微小化学变化可以调节核小体的机械特性和其调控尾部的可及性,从而帮助开启或关闭基因活性的窗口。
引用: Hu, G., Zhang, H., Xu, W. et al. Selective binding of divalent cations reshapes nucleosome mechanics and unlocks histone tail dynamics. Commun Biol 9, 365 (2026). https://doi.org/10.1038/s42003-026-09648-1
关键词: 染色质, 核小体力学, 镁与钙离子, 组蛋白尾部, 基因调控