Clear Sky Science · zh
Wnt11 介导成纤维细胞—平滑肌细胞相互作用,促进大鼠神经源性膀胱纤维化
当神经失灵时,膀胱发生瘢痕
许多脊髓损伤、多发性硬化或帕金森病患者会出现“神经源性膀胱”,即受损的神经无法正常控制尿液的储存与排出。随着时间推移,膀胱壁可能变厚并被类似瘢痕的组织僵硬化,危及肾功能并影响生活质量。这项在大鼠中进行的研究揭示了导致该瘢痕形成的一个关键分子成因,并提示了减缓甚至预防损伤的新途径。
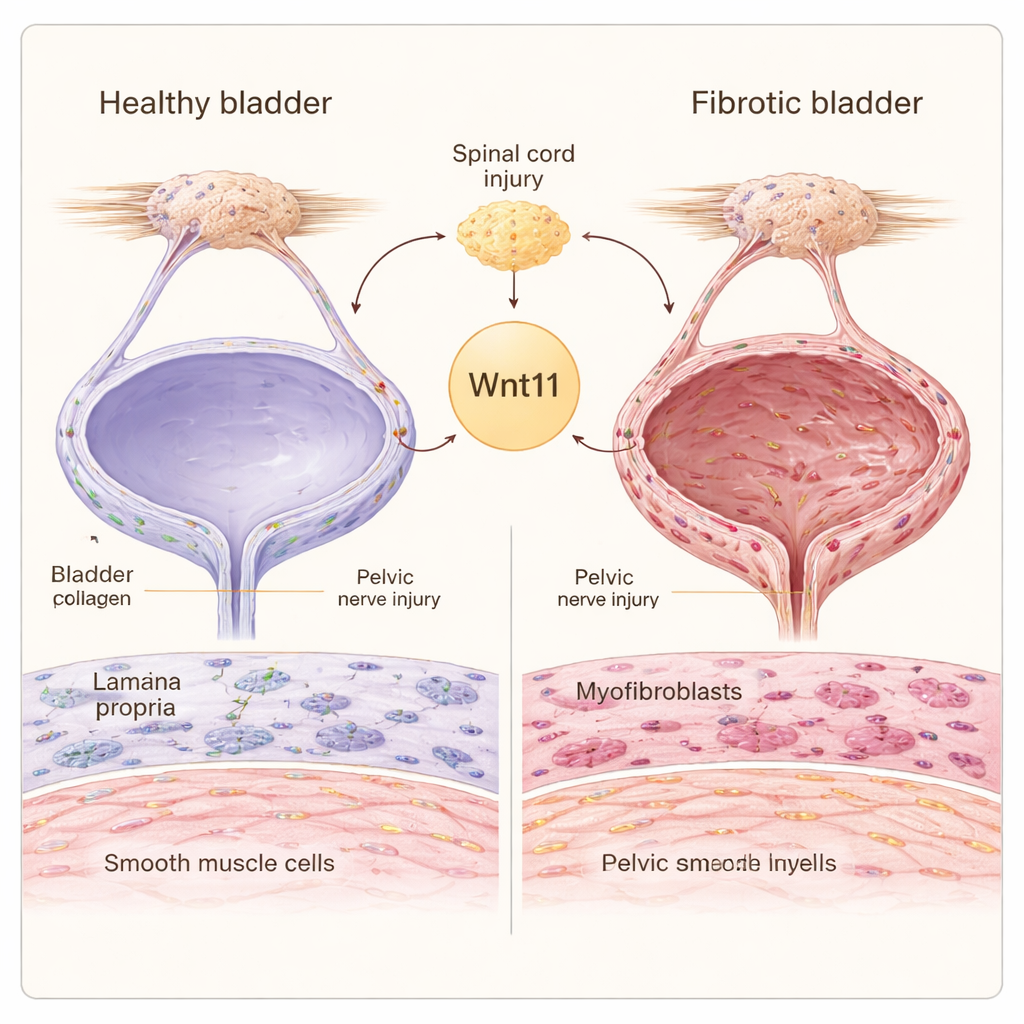
神经损伤的隐性代价
当支配膀胱的神经受损(无论是在脊髓内还是盆腔附近)时,器官必须更努力地处理尿液。膀胱壁包含两种主要的支持细胞类型:产生细胞周围支架物质的成纤维细胞,以及通过收缩将尿液排出的平滑肌细胞。在神经源性膀胱中,成纤维细胞可以转变为高度活跃的“肌成纤维细胞”,大量产生胶原蛋白,而平滑肌细胞则从精瘦的收缩型转为更厚重、更具合成活性的表型。这些变化共同沉积出僵硬的瘢痕组织,降低膀胱的伸展和排空能力。
一种信号分子走到聚光灯下
研究者聚焦于一类被称为 Wnt 配体的细胞间通信蛋白家族,该家族已知在其他器官调控组织生长和纤维化。筛查受神经损伤大鼠的膀胱组织时,他们发现某一成员 Wnt11 在由脊髓损伤或盆神经挤压引起的纤维化膀胱中始终显著上调。Wnt11 在成纤维细胞和平滑肌细胞中都升高,且其水平与膀胱功能障碍的严重程度相关。在培养的正常膀胱细胞暴露于另一种促纤维化因子 TGF-β1 时,Wnt11 的产生也随之增加,提示这两种信号之间可能存在相互强化的回路。
从化学信号到持久瘢痕
为检验 Wnt11 是旁观者还是主动驱动因子,团队在神经损伤大鼠中补充额外的 Wnt11 蛋白,并用一种名为 LGK974 的药物阻断 Wnt 分泌。额外的 Wnt11 使膀胱增大、充盈与排空时的压动力学恶化、肌层增厚并促进胶原沉积。阻断 Wnt 分泌则产生相反效果,缓解尿路问题并减少瘢痕组织。在分离的细胞实验中,Wnt11 促使成纤维细胞向肌成纤维细胞转变,并推动平滑肌细胞走向促纤维化的合成表型。沉默 Wnt11 基因本身能减弱这些变化,由此明确 Wnt11 是膀胱重塑的关键加速器。
细胞如何解读纤维化信号
进一步探究显示,该研究描绘了从细胞表面的 Wnt11 到细胞核基因变化的通路。Wnt11 被发现在膀胱成纤维细胞和平滑肌细胞上与受体 Vangl2 结合。这一配对并未使用经典依赖 β-连环蛋白的 Wnt 路径;相反,它激活了另一条称为平面细胞极性(PCP)的通路。在这里,Wnt11 与 Vangl2 招募了一种适配蛋白 DVL2,随后激活酶 JNK。JNK 反过来激活转录因子 c-JUN 与 NFAT5,它们进入细胞核并帮助启动促纤维化基因。作为已知的瘢痕驱动通路,TGF-β1 在细胞膜和细胞核层面都与这条 Wnt11–Vangl2–JNK 通路发生了物理和功能上的会聚,使两种信号互为强化。
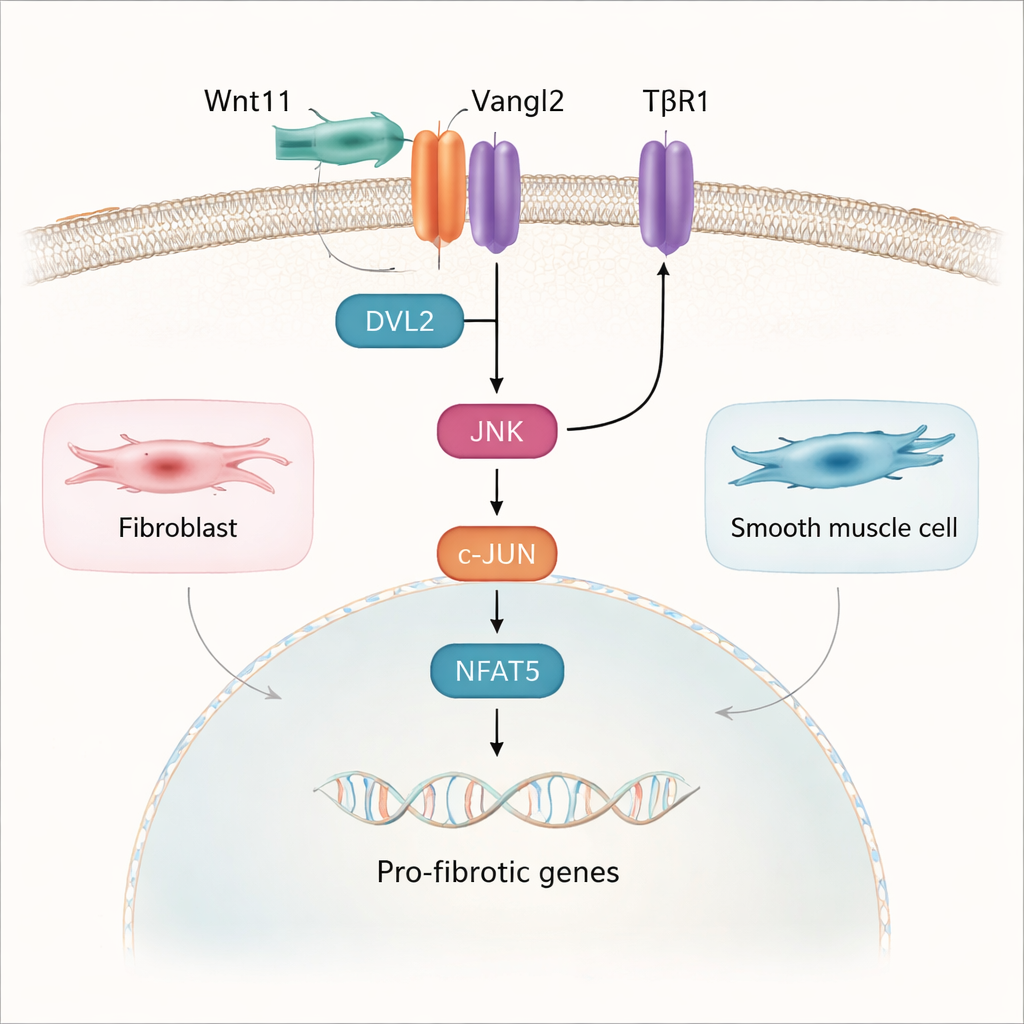
走向更柔软、更健康的膀胱
鉴于 Wnt11 与 TGF-β1 协同促使膀胱僵硬,研究团队测试了阻断两条通路关键步骤的药物。在神经源性膀胱大鼠中,联合抑制 TGF-β 受体 TβR1 与 JNK 酶的治疗效果最佳:膀胱体积更小、肌壁更薄、胶原更少,且尿液的储存与排出功能相比单药治疗有显著改善。对非专业读者而言,结论是:一种由神经损伤诱导的特定信号——Wnt11——有助于将正常的支持细胞和肌细胞转换为形成瘢痕的细胞。中断这一信号,尤其是与经典的 TGF-β 抑制剂联合使用,可能为未来不仅缓解症状而且保护膀胱结构与功能的治疗策略奠定基础。
引用: Ge, Q., Zhang, J., Fan, Z. et al. Wnt11 mediates fibroblast–smooth muscle cell interaction to promote neurogenic bladder fibrosis in rats. Commun Biol 9, 194 (2026). https://doi.org/10.1038/s42003-026-09647-2
关键词: 神经源性膀胱, 纤维化, Wnt11, 平滑肌细胞, TGF-β 信号